Clear Sky Science · ja
FCHo2 は talin ではなく、曲面接着部位でインテグリンɑvβ5のインサイドアウト活性化を可能にする
細胞は周囲の形状をどう感知するか
私たちの体は、周囲をつかんで引っ張り、押し、移動し、分裂し、あるいはその場に留まる細胞によって構成されています。本論文は、細胞が環境の剛性だけでなく形状も読み取っていることを明らかにします。細胞膜が強く曲がった場所でのみ作動する特別な接着システムを見いだすことで、著者らは、細胞が平坦な環境と繊維状の環境で異なる内部の「グリップ」を使い分けていることを示しており、組織形成やがんの浸潤に関する重要な示唆を与えます。
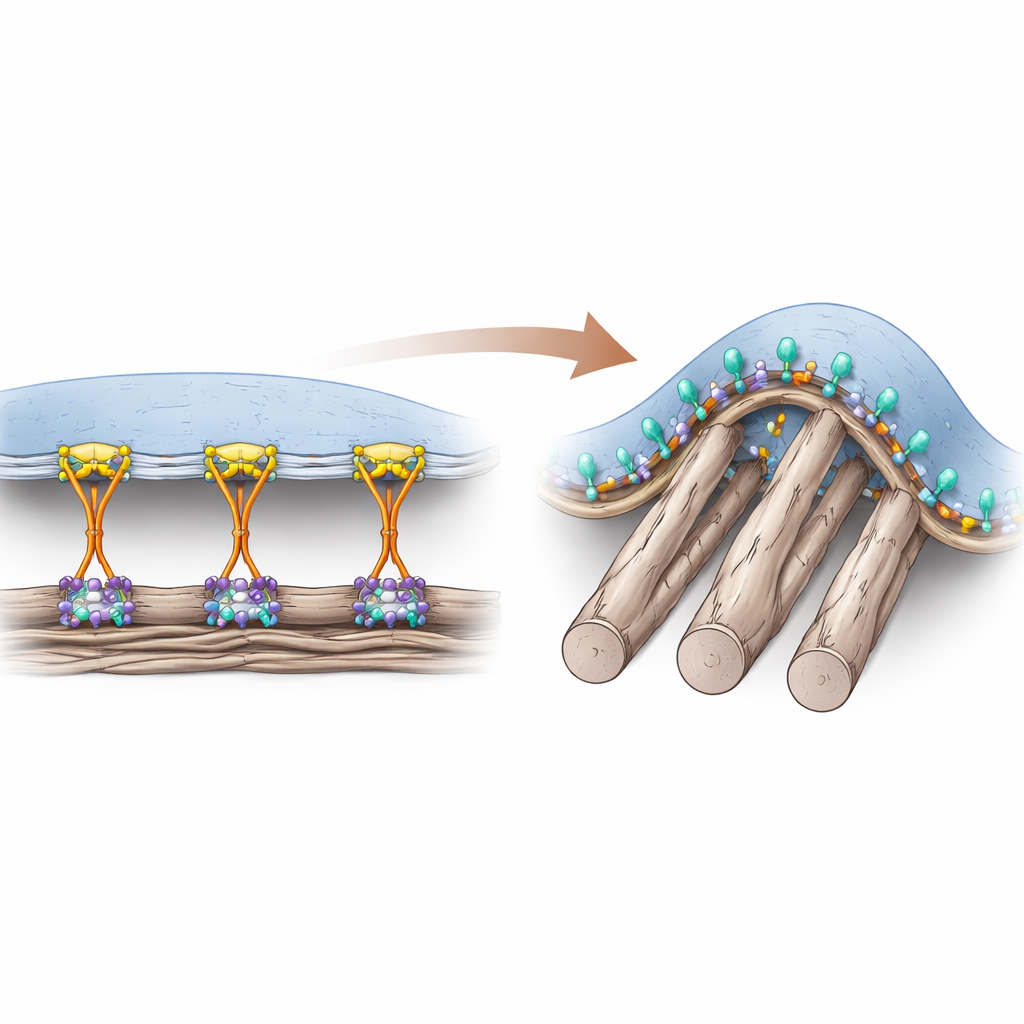
細胞がつかむ方法は二通り
細胞はインテグリンと呼ばれる表面受容体を使って、周囲のタンパク質豊富な基質に付着します。長年、研究者たちは talin という補助タンパク質が、インテグリンを細胞内から“オン”にして強固な結合を可能にするために絶対に必要だと考えてきました。これらの古典的なアンカリング部位、焦点接着(フォーカルアドヒージョン)は主に平坦で剛性の高い面に形成され、細胞骨格を通じて大きな引張力を伝達します。しかし生体組織では、多くの周囲の繊維は柔らかく円筒状であり、曲がった接触点を作るため、こうした大きな力を支える構造は容易に形成されません。著者らは以前、膜が細い繊維に沿って曲がる場所に特有の接着構造、いわゆる“曲面接着”を見いだしており、これは特定のインテグリン αvβ5 に依存することが示されています。
曲面用グリップは異なる補助因子を使う
新しい研究では、talin は局在しているものの、曲面接着におけるインテグリン αvβ5 の主要な活性化因子ではないことが示されました。その代わりに、曲率を感知するタンパク質 FCHo2 がこの役割を担います。ナノサイズのバーや柱を精密に設計して細胞膜を制御された形で曲げる実験により、αvβ5 は曲がった領域に強く集積するが、それは β5 の細胞内尾部のごく短い配列、HDRRE モチーフに FCHo2 が結合できる場合に限ることが観察されました。このモチーフが破壊されると、インテグリンは焦点接着では機能するものの曲面接着は形成できなくなります。FCHo2 をノックダウンすると古典的な焦点接着は概ね残る一方で曲面接着は消失し、逆に talin を除去すると焦点接着が著しく弱くなるが曲面接着にはほとんど影響がない、という結果が得られました。
形状を選ぶ単一アミノ酸スイッチ
ひとつの謎は、β5 の内側尾部が非常に似ているにもかかわらず、近縁のインテグリン αvβ3 がなぜ曲面接着を作れないのかという点でした。二つのインテグリンのドメインを交換したり点変異を導入したりすることで、著者らは talin 結合部位近傍の単一の重要な位置を同定しました。ほとんどの β インテグリンはトリプトファン(W)を持つが、β5 は特異的にチロシン(Y766)を持っています。β5 のチロシンをトリプトファンに置き換えると、そのインテグリンは曲面接着に参与する能力を失い、β3 のように振る舞って焦点接着のみを好むようになりました。逆に β3 由来のキメラにチロシンを入れると曲率感受性が回復しました。このチロシンのリン酸化を模倣する変異や非リン酸化状態を模した変異を使ったさらなる実験は、この残基の化学修飾がインテグリンを平坦で高張力の焦点接着側か、曲面で低張力の接着側かに傾けうることを示唆しています。
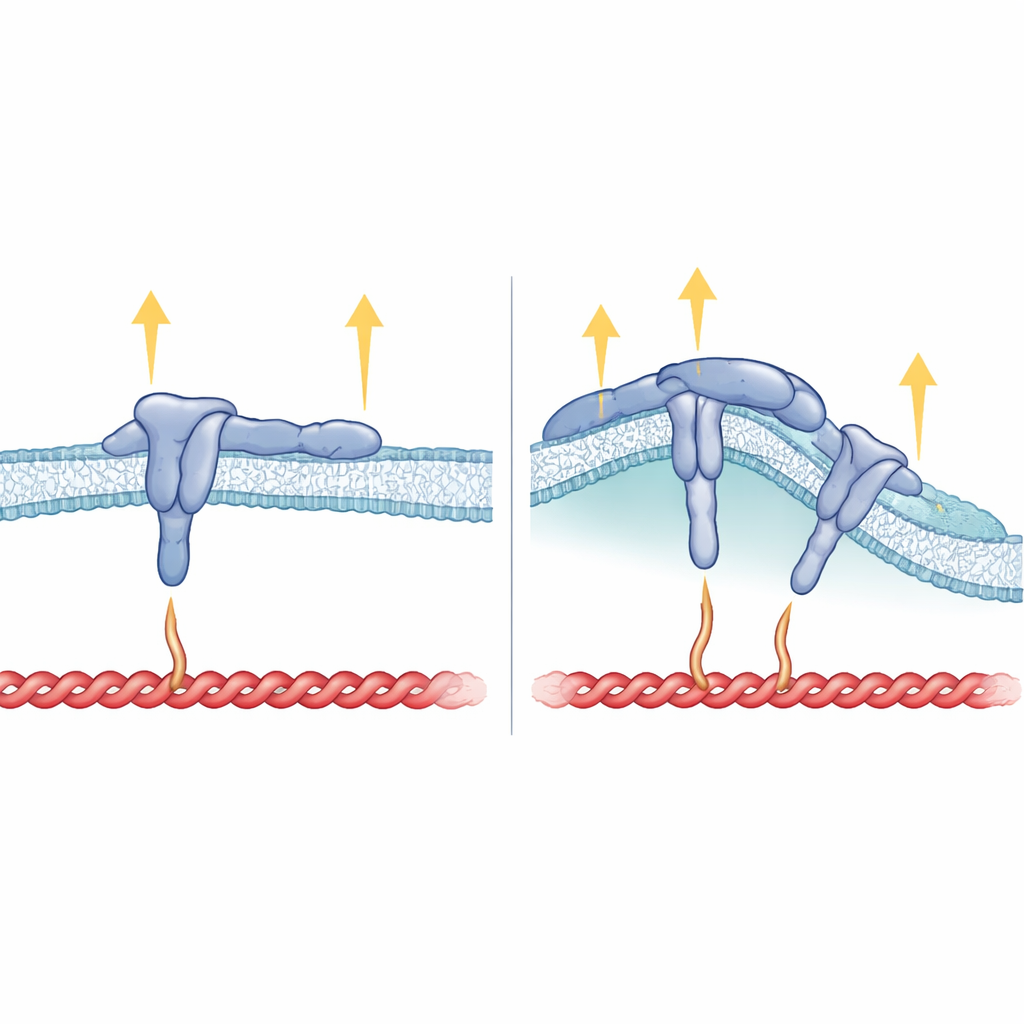
膜の形、インテグリンの構造、力の関係
内側尾部に加えて、膜を貫通する β5 の領域も重要であることがわかりました。研究者らが β5 の膜貫通セグメントを β3 のそれと置き換えると、できたインテグリンは焦点接着は形成できるものの曲がった部位を好まず FCHo2 と同調もしなくなりました。これは、インテグリンの膜中での座り方が HDRRE モチーフの配向を決め、FCHo2 が曲がった領域で結びついてリガンド結合状態の活性 αvβ5 を安定化させることを助けることを示唆します。曲面接着では、talin はインテグリン尾部のより遠位の部分にしか触れておらず高張力を負担していないようで、vinculin、tensin、kindlin といった高張力を必要とする他の成分はほとんど存在しません。一方、焦点接着では talin は尾部と膜の近位・遠位の両方をつかんで強い引張力を支え、そのため FCHo2 が同じ領域にアクセスできないという説明がつきます。
細胞挙動にとっての意味
一般読者にとってこの研究の要点は、細胞が周囲に付着するために二つの別個の「グリップモード」を持っているということです。平坦で剛性の高い領域では talin 駆動の焦点接着を使って強く引っ張ります。柔らかく繊維状で曲がった構造では FCHo2 駆動の曲面接着に切り替え、はるかに低い力でインテグリン αvβ5 を安定化させます。インテグリン配列の小さな変化とその部位の化学修飾の有無が、どちらのモードが使われるかを決める手助けをします。この二重システムにより、細胞は三次元環境における剛性と形状の両方を解釈でき、移動や組織の編成、さらには病的な侵入の仕方に影響を与えます。
引用: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
キーワード: インテグリン, 細胞接着, 膜の曲率, FCHo2, 細胞骨格