Clear Sky Science · ja
フラグメントベースの創薬におけるヒットからの進展と課題
小さな化学片を将来の医薬品へと変える
現代の医薬品発見はしばしば巨大な分子コレクションをふるいにかけることで行われますが、それは時間がかかり高価で、効率が低下しつつあります。本稿はフラグメントベース創薬と呼ばれる新しい手法を取り上げます。これは非常に小さな化学片から出発し、段階的に有望な候補へと組み上げていくアプローチです。ここでは、より賢い設計、自動化、人工知能が明日の治療法の発見をいかに速く、幅広くする可能性があるかを紹介します。
なぜ大量スクリーニングではなく“小さく始める”のか
従来の創薬は比較的大きな分子を数百万単位で試して、疾患関連タンパク質にどれが結合するかを調べることに依存してきました。これに対しフラグメントベースの手法は逆の発想を取ります。より小さな分子群、すなわち「フラグメント」を小規模にスクリーニングし、それぞれが単純な化学形状を表します。これらのフラグメントは結合が弱いものの、非常に小さく多様であるため化学的可能性をはるかに効率的に探索できます。課題は、弱いシグナルは検出や解釈が難しく、フラグメントが実際に結合しているのかアッセイのアーティファクトなのかを確実にするために極めて感度の高い実験と慎重なクロスチェックが必要になることです。X線結晶構造解析やクライオ電子顕微鏡といった構造解析手法はフラグメントがタンパク質ポケット内でどのように位置するかを正確に示し、溶液中の手法(NMR、熱量測定、表面プラズモン共鳴など)は結合の強さや速度を測定します。
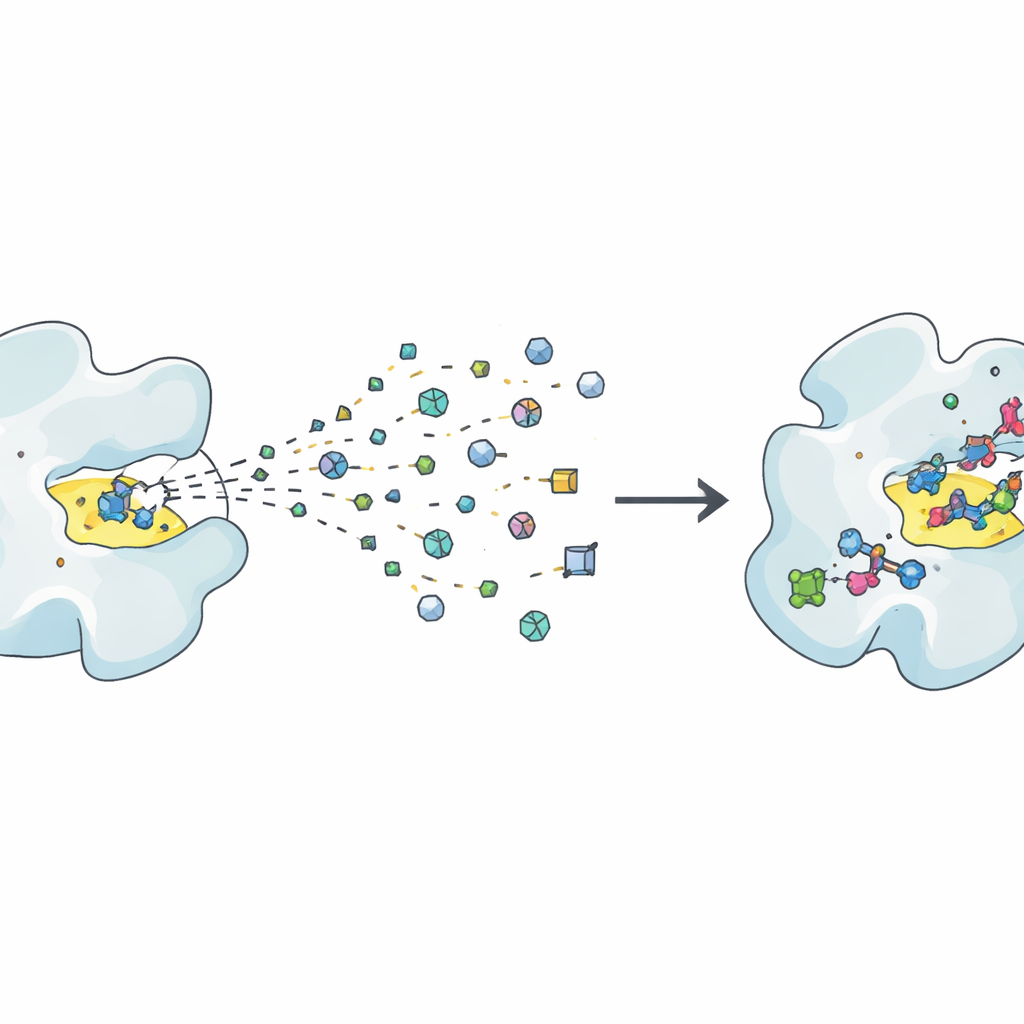
初期ヒットから有望なリードへ
有用なフラグメントが見つかると、本格的な作業が始まります。これらのかすかな「ヒット」を強く選択的な「リード」化合物へと変えることです。本稿はこの過程を繰り返される「設計(Design)、合成(Make)、評価(Test)」のサイクルとして描きます。設計段階では、化学者や計算ツールがフラグメントを成長させる、つなぐ、または統合する方法を提案し、タンパク質ポケットをより埋め、望ましくない反応性を避け、溶解性などの物性を維持することを狙います。合成段階では、これらの設計を合成し、ロボット、高スループット化学、経路設計ソフトウェアの助けを借りて進めます。評価段階では、新しい分子が本当に結合を改善しているか、意図した生物学的機能に作用するか、誤解を招くシグナルを出すパーンアッセイ干渉化合物などの落とし穴を避けているかを測定します。フラグメントは出発点で弱いため、このループを複数回回すことで化合物が実際に薬候補に近づくことが多いです。
新しいツール:自動化、AI、スマートライブラリ
レビューは、このサイクルの各段階を再形成している新世代のツールに光を当てます。フラグメントライブラリは現在、多様性を備えるだけでなく「合成的に扱いやすい(synthetically sociable)」よう設計されており、堅牢な反応を用いて多方向へ容易に展開できます。特定のタンパク質ファミリー、金属含有部位、あるいは特定のアミノ酸と共有結合を形成するものなど、ターゲット特異的なフラグメントセットもあり、従来は「ドラッガブルでない」と考えられたターゲットにも取り組めるようになっています。デジタル面では、人工知能モデルや物理ベースのシミュレーションが、どの化学変化が結合を改善したり毒性を減らしたりするかを示唆し、何十億もの仮想分子空間をふるいにかけるのに役立ちます。こうした予測は、少数の高コストなシミュレーションや実験で学習したモデルが次の設計の波を導く能動学習ループと組み合わされることが増えています。
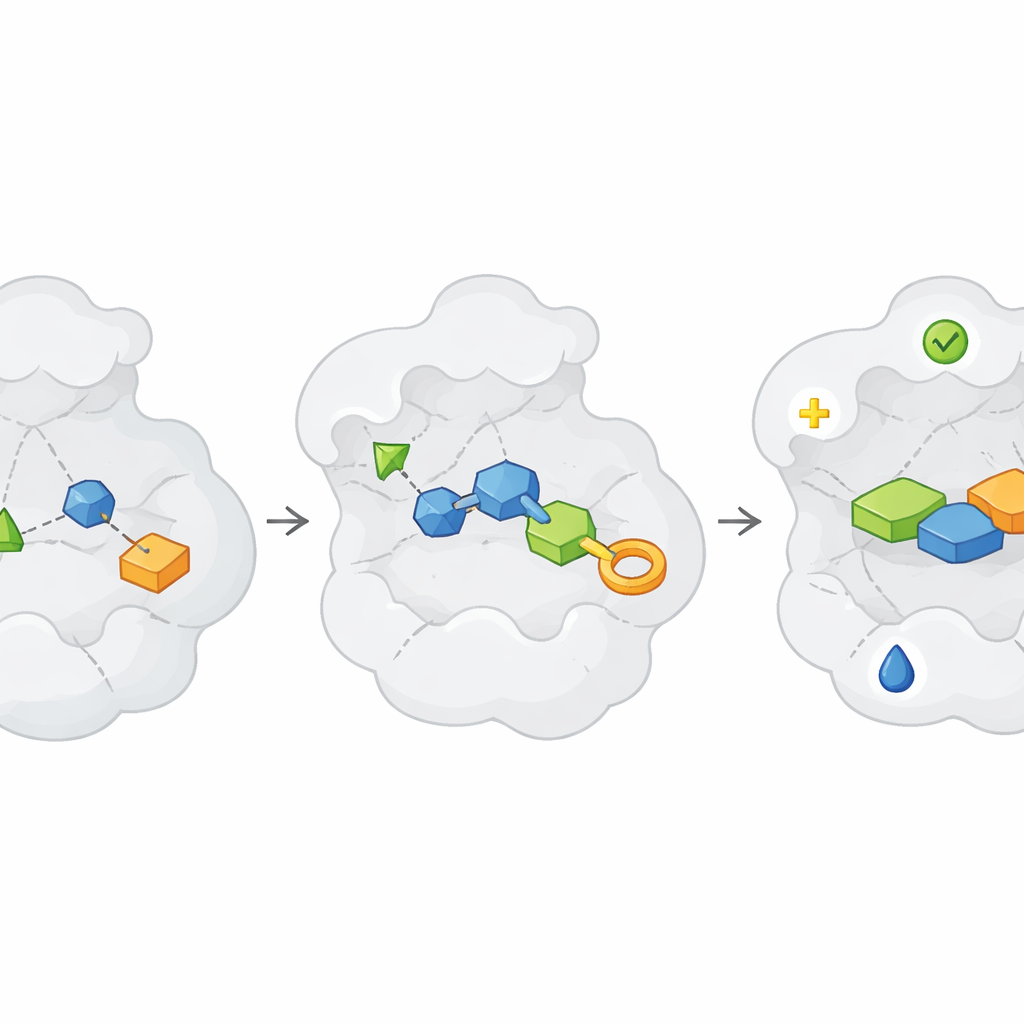
規模を上げても滞らせない合成と評価
創薬における大きなボトルネックは、単に評価するための十分な化合物を合成・精製することです。記事はハイスループット合成ロボット、フローケミストリー、新しい抽出法がフラグメントヒット周辺の数百〜数千の関連分子を生産し得ると説明します。あるアプローチでは当初は完全精製を省き、粗反応混合物を結晶構造解析、動力学測定、NMRなどの感度の高いアッセイで直接テストする、いわゆる「ダイレクト・トゥ・バイオロジー」的手法を採ることもあります。質の管理として質量分析などを並行して用い、どの混合物に意図した生成物が含まれているかを追跡します。データは雑音を含むことがありますが、これらの迅速なテストをスマートな解析と追跡のためのクリーンな合成と組み合わせることで、従来の一件ずつの化学よりもはるかに速く構造—活性相関を描き出すことが可能になります。
将来の医薬品にとっての意義
総じて、記事はフラグメントベース創薬が、特に現代の自動化やAIと組み合わせた場合、新薬を見つけるための強力で柔軟な戦略へと成熟したと結論づけています。小さく効率的なビルディングブロックから出発することで科学者は化学空間をより考察的に探索できますが、出発点のシグナルが弱いため厳密な検証が求められます。著者らは、設計、合成、評価を半自動化されたデータ駆動型のワークフローへ厳密に統合し、フラグメントデータや手法を公開して共有することが、資源の限られたグループにも恩恵をもたらす最大の利得になると主張します。これらの進展が続けば、フラグメントベースのアプローチは研究生産性の長期的な低下を食い止め、より安全で効果的な薬の到来を多くの疾患領域で早める助けになる可能性があります。
引用: Grosjean, H., Biggin, P.C. Developments and challenges in hit progression within fragment-based drug discovery. Nat Commun 17, 2226 (2026). https://doi.org/10.1038/s41467-026-68941-z
キーワード: フラグメントベース創薬, ヒット・トゥ・リード最適化, 設計・合成・評価サイクル, ハイスループットスクリーニング, 計算創薬