Clear Sky Science · ja
実験に基づくポリマーモデルがゲノム座位の高解像度構造を明らかにする
DNAの折りたたみが細胞のアイデンティティを形作る仕組み
体内のほとんどすべての細胞は基本的に同じDNAを持ちながら、脳細胞、皮膚細胞、幹細胞はそれぞれ大きく異なる振る舞いをします。その重要な理由の一つが、核内でのDNAの折りたたみ方とパッキングの仕方です。本研究は、その折りたたみを驚くほど詳細に「見る」新しい手法を示し、DNAの物理的配置が重要な遺伝子のオン/オフにどう結びつくかを明らかにします。実験結果と物理に基づくコンピュータシミュレーションを組み合わせることで、著者らはゲノム組織の基本的構成要素として作用すると思われる隠れた遺伝物質の塊を明らかにしました。
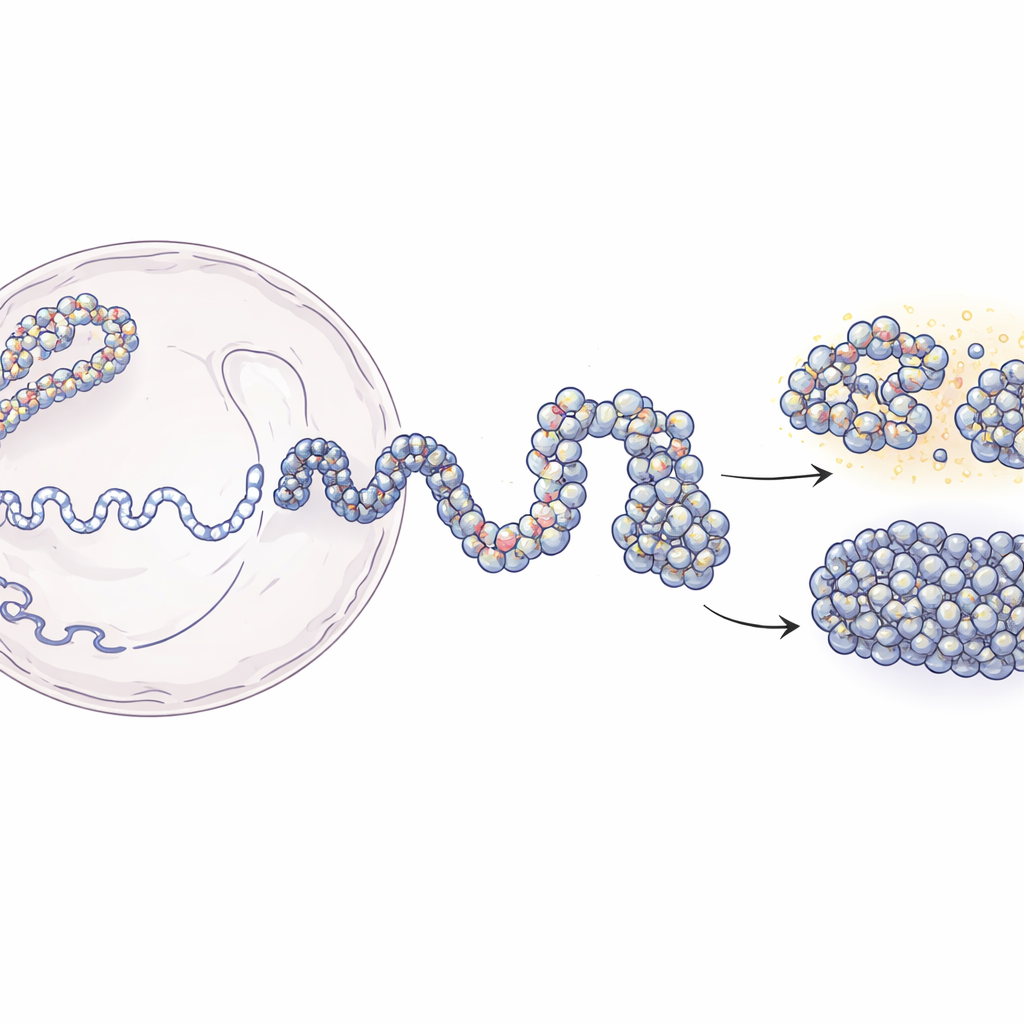
長いDNA糸から3次元ゲノム地図へ
核内ではDNAはヌクレオソームと呼ばれるタンパク質の糸巻きに巻き付いており、ビーズオンア・ストリングと呼ばれる構造、すなわちクロマチンを形成します。Hi-CやMicro-Cのような現代の手法は、どのDNA断片が3次元的に近接しているかを教えてくれますが、通常は集団平均に基づくぼんやりしたスナップショットになります。一方で、個々のヌクレオソームの位置を特定する実験は局所的に鮮明な情報を与えますが、全体構造の把握には限りがあります。本研究はそのギャップを埋めます。著者らは、遠く離れたDNA領域がどれだけ接触するかを報告する低解像度の接触マップから出発し、そこにヌクレオソーム位置の実験マップを組み合わせます。ポリマー物理の原理を用いて、実験データに合致しつつ数十塩基単位まで解像度を上げたクロマチンの3次元アンサンブルを構築します。
クロマチン再構築のための二段階戦略
モデリング手法は主に二つの段階で展開します。まず研究チームはHi-Cデータを使い、20万塩基に及ぶDNA領域の大規模な形状を多数生成します。ここではクロマチンを柔軟な鎖として扱い、5,000塩基ほどのセグメントが実験で観測されたように接触を作るか回避するよう穏やかに導かれます。これらの粗視化構造は、細胞内のタンパク質が作り出す全体的な折りたたみパターンを捉えます。次の段階では、各大きなビーズを個々のヌクレオソームとそれらをつなぐ短いDNAリンクからなるはるかに細かな鎖に置き換えます。ヌクレオソームの位置は、酵素を使ったマッピング法(MNase-seq)から得られる典型的な配置に基づいています。こうして得た微細鎖を、広域構造を尊重しつつ折りたたませます。研究者らが高解像度モデルを実験解像度に再び「ぼかす」と、Hi-CおよびMicro-Cの接触マップを高い精度で再現しました。
構造単位としてのヌクレオソーム・ブロブの発見
シミュレーション構造を詳しく調べると、顕著なパターンが浮かび上がりました。ヌクレオソームは均一に配列されるのではなく、不規則な塊に集まっており、著者らはこれをヌクレオソーム・ブロブと呼びました。これらのブロブは、実際の細胞を超解像顕微鏡で観察したときに見られる塊状の構造に似ています。何千ものシミュレーションスナップショットを解析した結果、ブロブは球形ではなく細長く、通常いくつかのヌクレオソームが密に詰まっていることが示されました。重要なのは、これらのブロブ内部の接触が実験データで観測されるドメイン状の相互作用ブロックと密接に対応していることで、ブロブが単なるランダムな偶然ではなくクロマチン組織の基本的な3次元単位であることを示唆します。シミュレーションはまた、実験では検出が難しい微細なドメイン境界も予測しており、この物理モデルがノイズに埋もれたデータから微小構造を明らかにできる可能性を示しています。
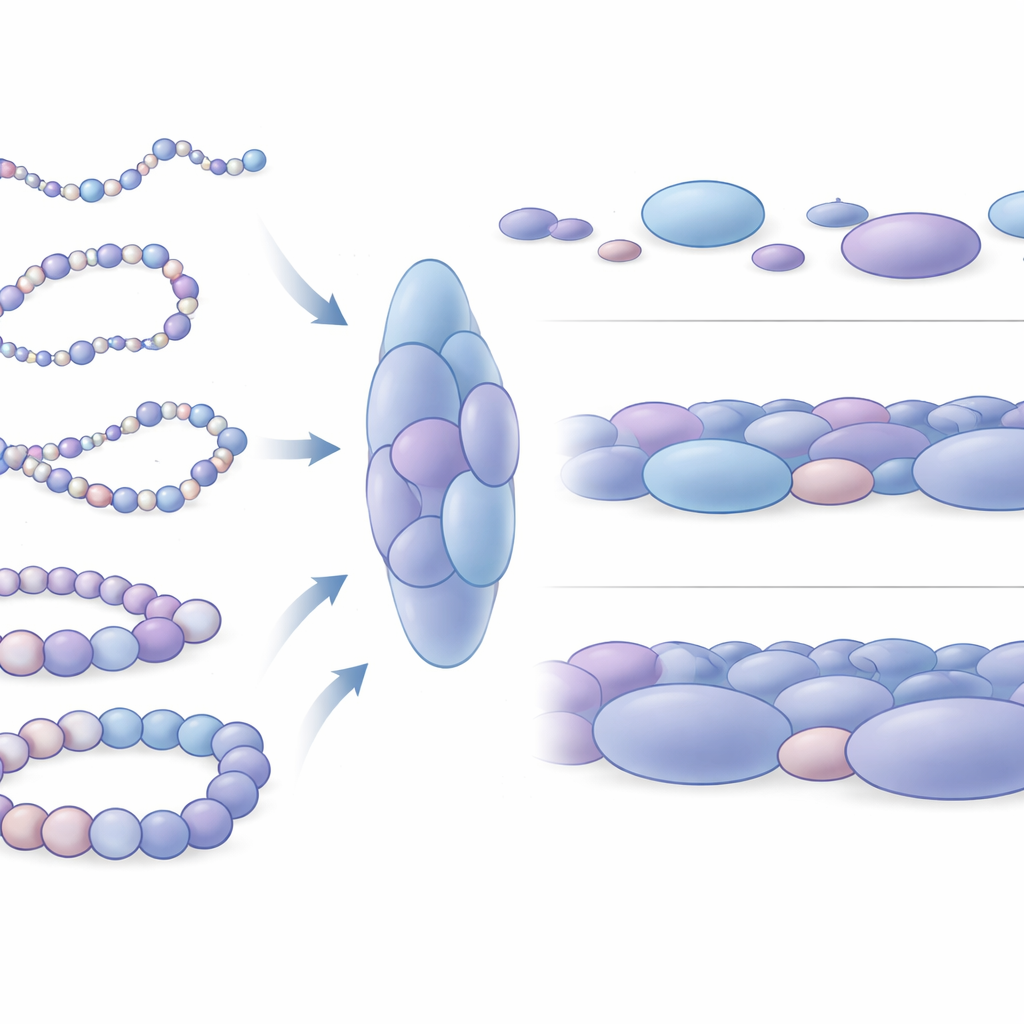
パッキングの違いが遺伝子活性をどう反映するか
研究者らは次に、これらのブロブが活性な遺伝子周辺と不活性な遺伝子周辺でどう異なるかを調べました。対象は幹細胞の柔軟で未分化な状態を保つのに関わる2つの遺伝子(NanogとLin28A)と、同じ細胞で不活性化されている発生制御遺伝子(HoxB4とHoxA13)を含む、よく研究された4領域です。不活性な遺伝子の周辺ではブロブは平均して大きくより密に詰まり、ヌクレオソームはより完全に閉じた局所配置を形成していました。これに対し、活性な遺伝子近傍のブロブは小さめでやや緩く、ばらつきが大きかった。より広いスケールでは、活性遺伝子周辺のDNAは多くの異なる形をサンプリングし、機械的にも曲げやすい一方で、不活性領域はより剛直なクロマチンセグメントのように振る舞いました。この機械的違いは、遠く離れた制御性DNA要素が出会って遺伝子スイッチと協調する難易度に影響を与えると考えられます。
遺伝子制御の理解における意義
総じて、本研究の発見は、ゲノムが動的なヌクレオソームのクラスターから構成され、それらの大きさ、形、間隔が近傍の遺伝子がアクセス可能か封鎖されているかを左右するという図を描きます。新しいモデルは、実験の接触データ、ヌクレオソームマップ、物理原理を一つの枠組みに結びつけ、幹細胞遺伝子が柔軟で相互作用的に保たれる一方で発生遺伝子がより堅くコンパクトな近隣に隔離される理由を説明します。専門外の読者にとっての核となる考え方は、遺伝子活性はDNA配列だけで決まるのではなく、そのDNAがどのように三次元構造として折りたたまれているかにも依存するという点です。ヌクレオソーム・ブロブを折りたたみの基本構成要素として明らかにすることで、本研究は微視的なゲノム構造と発生、細胞アイデンティティ、疾患のような大規模過程とを結びつける有力な道筋を提供します。
引用: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
キーワード: クロマチン折りたたみ, ヌクレオソームクラスター, 3Dゲノム構造, 遺伝子制御, ポリマーモデリング