Clear Sky Science · ja
レカネマブ関連ARIAにおける細胞傷害性CD8⁺ T細胞のクローン性拡大
なぜこれがアルツハイマー病の人々に重要なのか
レカネマブは脳からアミロイドを除去し、アルツハイマー病における記憶障害の進行をわずかに遅らせることができる最初期の薬剤の一つです。しかし、この治療を受ける患者のなかには脳浮腫や微小脳出血など、MRIで検出される変化を示すものがあり、これらは総称してアミロイド関連画像異常(ARIA)と呼ばれます。本研究は患者と家族にとって重要な問いを投げかけます:ARIAが現れるとき、免疫系では何が起きているのか、そして将来的に簡便な血液検査が誰がリスクが高いかを予測する助けとなる可能性はあるか?
新しいアルツハイマー治療の期待とリスク
レカネマブは点滴で投与される抗体で、アルツハイマー病の特徴であるアミロイドβの凝集体を標的とします。体がアミロイドを除去するのを助けることで、認知機能低下をわずかに遅らせることができます。しかしこの恩恵には安全性の懸念が伴います:一部の人は脳浮腫や微小出血を含むARIAを発症し得ます。これらの副作用は頻回のMRI監視を必要とし、投薬対象を制限することがあります。誰もが同じように脆弱なわけではなく、APOE4と呼ばれる遺伝子変異を持つ人はリスクが高いとされますが、遺伝子だけでは特に治療開始直後になぜARIAが起きるかを説明できません。レカネマブは血流を通じて投与されるため、著者らは血中の免疫細胞を詳しく調べれば、早期の警告サインや治療と脳血管損傷を結ぶメカニズムが明らかになるかもしれないと考えました。 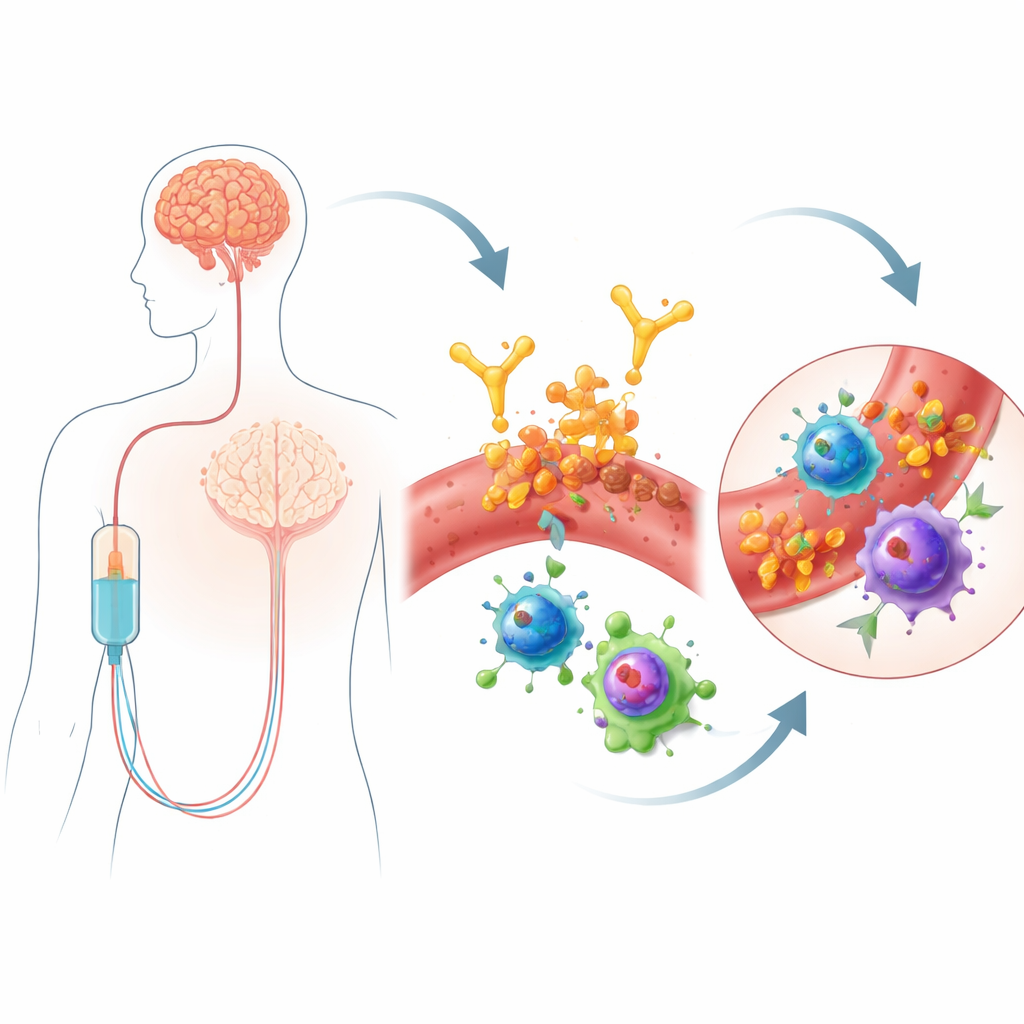
ARIAを発症した患者としなかった患者の免疫細胞の追跡
研究者らは地域の記憶外来でレカネマブを受けている6人のアルツハイマー病患者を調べました。うち3人が異なる形のARIAを発症し、残りの3人は年齢、性別、APOE遺伝子型、投与回数が類似した対照患者でした。採血は点滴直前に行われ、チームは集中的な「マルチオミクス」アプローチを用いました:数千の個々の免疫細胞でどの遺伝子が活性化されているかを読む単一細胞RNAシークエンシング、細胞型を定義する抗体タグ、クローンを追跡するT細胞受容体の配列解析、そして細胞代謝に関わる数百の低分子を測定するターゲット代謝オミクスです。これにより、どの細胞型が存在するかだけでなく、それらがどれだけ活性化しているか、どのような燃料を使っているか、そして特定のT細胞ファミリーが何らかの刺激に応じて増殖しているかを明らかにできました。
高度に武装したキラーT細胞の拡大
ARIAを発症した患者群では明確なパターンが浮かび上がりました。対照に比べてCD8「キラー」T細胞の比率が高く、CD4ヘルパーT細胞は少ない傾向がありました。CD8集団の中では、エフェクターメモリー細胞とTEMRAと呼ばれる末期分化型の二つの亜群が際立っていました。これらのTEMRA細胞はベテラン兵士のようで、標的細胞を殺すための強力な機構を備えた高度に攻撃特化した細胞です。ARIA陽性の患者ではTEMRA細胞がより多く、特定のT細胞ファミリーが増殖していることを示すクローン性拡大が見られ、細胞傷害能、血管を通った移動、慢性的刺激の痕跡に関連する遺伝子プログラムを持っていました。類似のT細胞状態は加齢や慢性感染、 多発性硬化症、そしてアルツハイマー病患者の脳脊髄液でも観察され、血管や脳表面近傍に蓄積することがあります。
代謝の再配線と他の免疫細胞との相互作用
研究チームはまた、これらのCD8エフェクター細胞が代謝を再配線していることを見出しました。ミトコンドリアでの効率的なエネルギー産生に主に依存するのではなく、より速いが効率は低い解糖系にシフトしており、短命で高強度の活動を支える代謝様式です。血中細胞の代謝産物測定はこれを裏付け、乳酸やピルビン酸のレベルが上昇し、クエン酸回路の重要な構成要素が減少していることが示され、これは炎症性免疫細胞に典型的なパターンです。別の白血球である単球も補完的な変化を示しました。ARIA陽性の患者では単球が抗原提示、細胞付着、ケモカイン産生の遺伝子をオンにしており、ケモカインはT細胞を引き寄せる化学信号です。リガンド—レセプター対の計算モデルは、単球がCD8エフェクター細胞に対してより強い活性化およびホーミング信号を送っており、これがキラー細胞を血管壁へ誘導する環境を作っていることを示唆しました。
T細胞を脳血管へ導く「宛先コード」
本研究は血液のみを解析しているため、著者らは独立したレカネマブ治療患者の脳から得られた単一細胞データセットを用いて、同じT細胞プログラムが脳の血管ニッチに関連しているかを検証しました。彼らは自身のCD8亜群をこの脳マップ上に投影したところ、ARIA陽性患者由来のTEMRAおよびエフェクターメモリー細胞は、疾患脳の内皮(血管)細胞と一致する接着分子やケモカイン受容体の組み合わせという転写上の「宛先コード」を示しました。これらの署名は、拡大したキラーT細胞が高度に武装され代謝的に活性化されているだけでなく、アミロイド除去の部位で損傷を受けた脳血管にホーミングし相互作用するように整備されていることを示唆します。 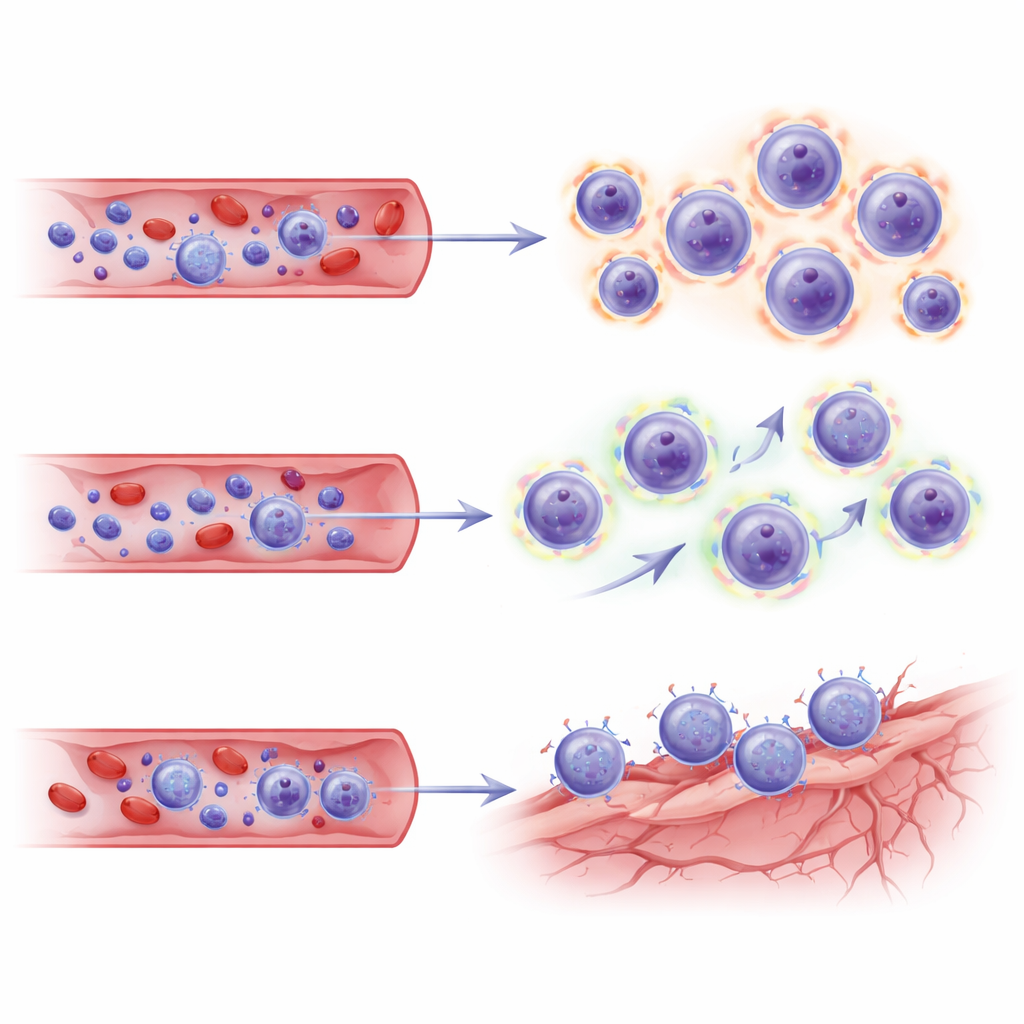
患者や今後のケアにとって何を意味するか
総じて、この小規模だが詳細な研究は、ARIAを単なるアミロイド除去の受動的な副作用以上のものとして描きます。むしろ血中で調整された免疫応答に関連しているようです:特定のキラーT細胞クローンの拡大と代謝活性化、単球からの強化されたシグナル伝達、そして脳血管と関わりやすい分子特徴の出現。これらの細胞がARIAを引き起こすことを証明するものではありません—免疫変化は血管損傷への反応かもしれませんが—しかし検証可能な仮説と血液ベースのバイオマーカーの設計図を提供します。将来的には、CD8 TEMRA細胞の量や代謝状態、重要なシグナル分子を測定することで、ARIAのリスクが高い患者を識別し、モニタリング計画を導く、あるいはアミロイド除去の利益を保ちながらこの免疫応答を一時的に抑える標的化戦略を考案する手がかりになるかもしれません。
引用: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
キーワード: アルツハイマー病, レカネマブ, 免疫細胞, 脳血管, 治療の副作用