Clear Sky Science · ja
TMEM63タンパク質は機械的に活性化されコレステロールで調節される脂質スクランブラーとして働き、膜の機械的回復力に寄与する
物理的ストレスでも細胞が壊れずにいられる仕組み
心臓の鼓動、働く筋肉、腫瘍が組織を押し広げる場面などで、私たちの細胞は常に押し潰されたり引き伸ばされたり衝撃を受けています。本研究は、OSCA/TMEM63と呼ばれる膜タンパク質群が、外側の「殻」を構成する脂質を再配列することでこうした強い力から細胞を守る仕組みを明らかにします。この組み込み型のショックアブソーバーを理解することで、聴覚障害や神経の絶縁、さらにはがんの浸潤といった病態への新たな視点が得られる可能性があります。
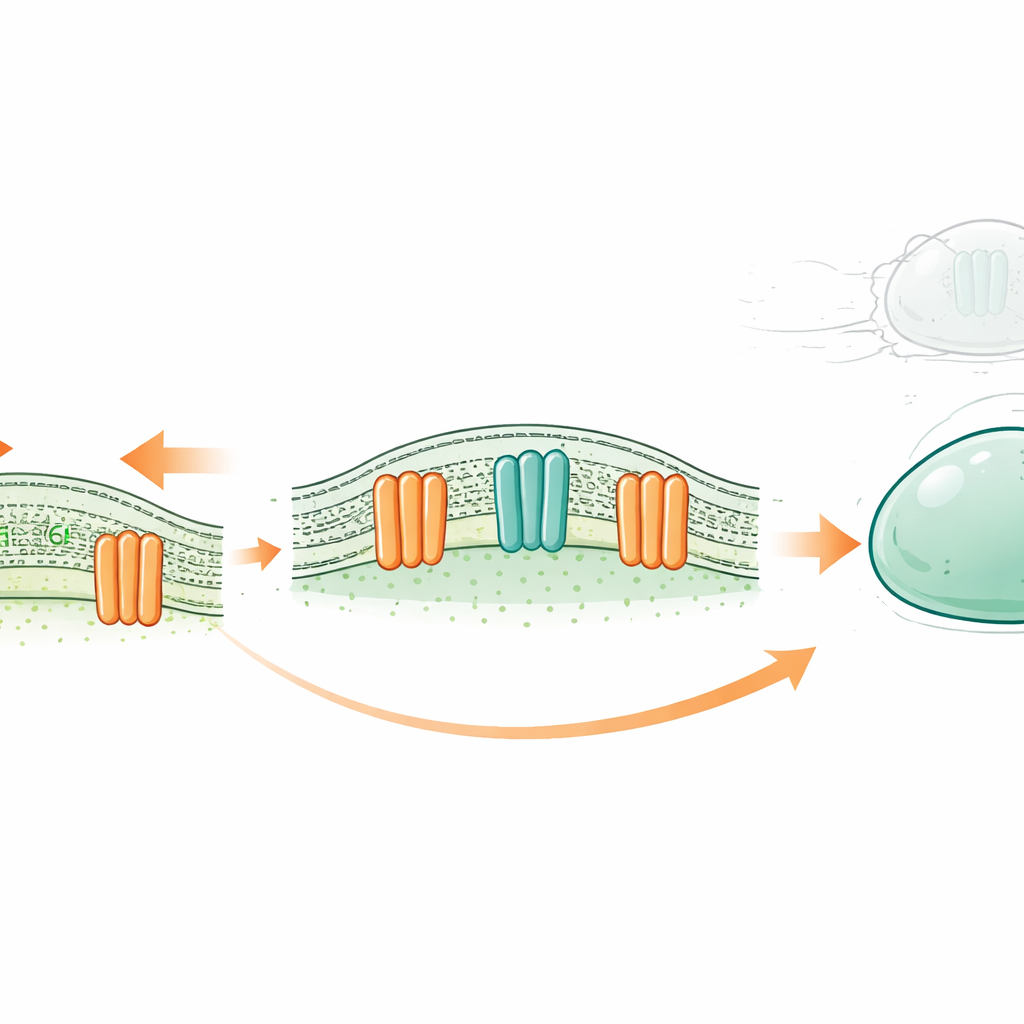
新しいタイプの細胞用ショックアブソーバー
すべての細胞は、脂質と呼ばれる脂肪様分子が二重層を成す薄い油状の膜に包まれています。従来、ある種の膜タンパク質はイオンチャネル―伸展などの刺激に応じて電荷を通す小さな弁としてのみ機能すると考えられてきました。植物からヒトに至るOSCA/TMEM63ファミリーは膜張力に応答して開くことが知られています。これまでの構造研究は、古典的なイオンチャネルとは異なり、その細孔が部分的に脂質で覆われていることを示唆していました。これにより挑発的な仮説が生まれます:これらは力を受けると膜の内外の脂質を入れ替える「スクランブラー」としても働くのではないか?
脂質が膜を越えて移動する様子を観察する
この仮説を検証するために、著者らはコンピュータシミュレーションと純化成分から作った還元主義的な実験系を併用しました。シミュレーションでは、開いた状態の複数のOSCAおよびTMEM63タンパク質をモデル膜に埋め込みました。脂質分子はこれらのタンパク質中の溝を自発的に移動して二重層の両側をつなぐベルトを形成し、その一方でイオンのための水に満たされた経路を残しました。同時に行った実験では、蛍光標識脂質と特定タンパク質を含む巨大な人工“バブル”(小胞)を作製しました。外側表面の蛍光を消光剤で消した後にさらに信号が低下するなら、それは内側から外側への脂質の反転(フリップ)が起きたことだけで説明できます。OSCA1.1、OSCA1.2、OSCA2.2、TMEM63A/Bを含む小胞はこの追加の蛍光低下を示し、能動的なスクランブリングを示しました。一方、脂質をスクランブルしない対照チャネルではそのような変化は見られませんでした。
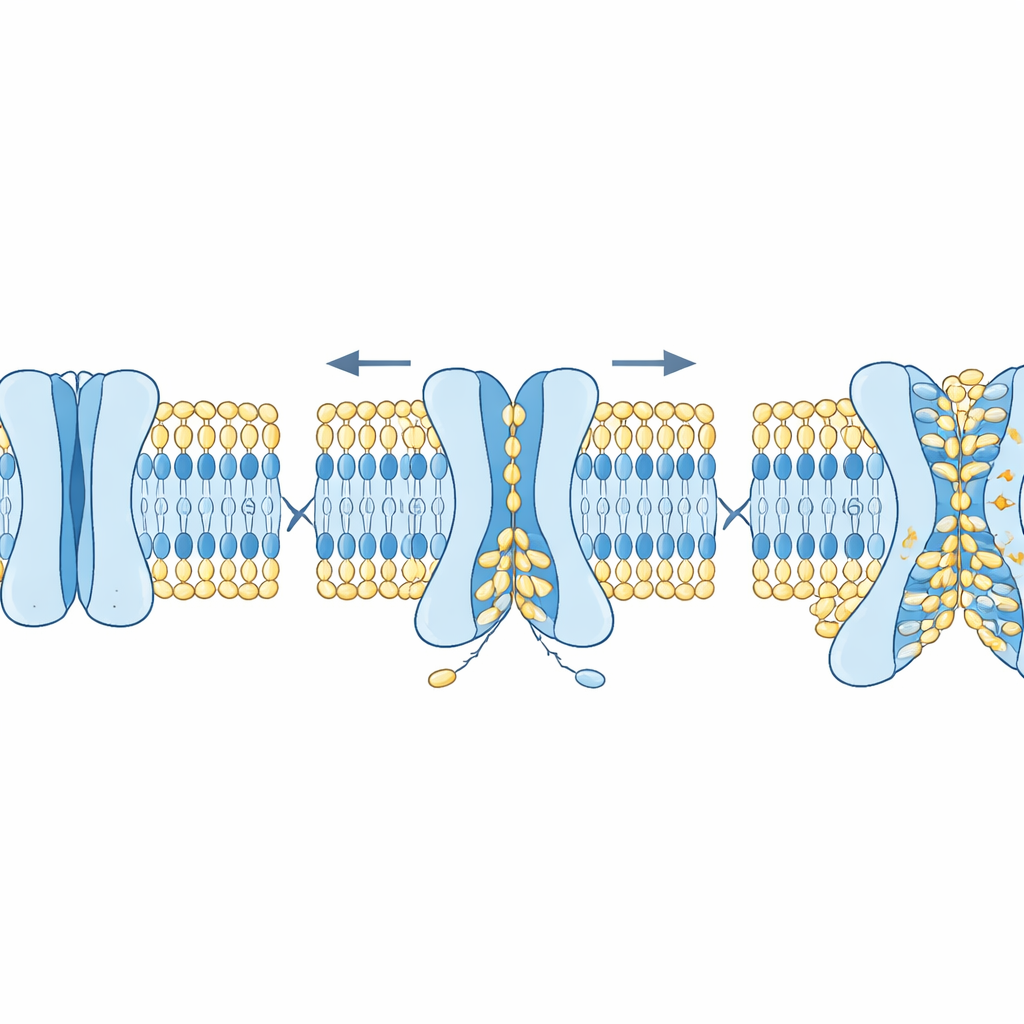
構造とコレステロールがプロセスをどのように調節するか
研究者らは次に、TMEM63タンパク質のどの特徴がこの二重機能を制御するかを検討しました。AlphaFold2を用いて、人のTMEM63タンパク質の閉じた状態から開いた状態までの多くの合理的な立体構造を生成しました。シミュレーションは、溝の中に存在するいくつかのかさばるアミノ酸残基が“ボトルネック”として機能することを明らかにしました。ある残基は主にイオンの流れを制限し、他の残基は脂質の移動を遮ります。イオンのボトルネックを変異させると電気伝導は増加したものの脂質スクランブリングにはほとんど影響がありませんでしたが、脂質ゲートを変異させると脂質のフリップがより起こりやすくなり、追加の刺激がないにもかかわらず細胞表面に“食べて”シグナルが露出することさえありました。もう一つの重要な調節因子はコレステロールで、これは細胞膜を硬くする成分です。モデル膜にコレステロールを加えると脂質スクランブリングは著しく遅くなり、TMEM63Aの閉鎖状態が安定化しました。これはシミュレーションだけでなく、コレステロールがタンパク質の特定部位に入り込んだ凍結電子顕微鏡構造でも確認されました。
機械的な力がオンスイッチになる
もしコレステロールが細胞内でスクランブリングを抑えているとすれば、適切な瞬間にそれを起動するのは何でしょうか。研究チームはリング状の糖分子であるシクロデキストリンを使い、コレステロールを除去することなく膜から選択的に脂質を引き抜いて張力を高めました。細胞サイズの小胞では、シクロデキストリンを加えるとタンパク質が存在する場合に限りTMEM63Aによる脂質スクランブリングが活性化され、機械的ストレスだけでフリップが誘導され得ることを証明しました。生きた細胞でも同様の手法により、軽度のコレステロール除去だけでは十分でなく、その後に機械的な刺激が必要であることが示されました。TMEM63Aを発現するよう改変した細胞を繰り返し伸張すると、外側表面に特定の脂質が急速に露出し(スクランブリングの指標)、これらのタンパク質を欠く細胞では変化がはるかに少なかったのです。
細胞の破裂からの保護
脂質の反転に加え、機械的に活性化されたスクランブリングは極端なストレス下で膜の振る舞いを変えました。強い力を受けた人工小胞では、スクランブラーを欠く小胞は破裂しがちでしたが、TMEM63Aや既知のスクランブラーを含む小胞は縮み、細いチューブを形成して大部分が無傷で残りました。天然にTMEM63AおよびTMEM63Bを発現するヒトの脳腫瘍由来細胞株では、いずれかのタンパク質の量を減らすと強い機械的ストレスに対して細胞が破裂しやすくなりました。これらの発見は、OSCA/TMEM63タンパク質が張力に応じて開く弁として働き、膜の内外の違いを一時的にぼかすことで、脂質を迅速に再配分させ、応力を均等化して致命的な断裂を防ぐというモデルを支持します。
健康と病気への意味
平たく言えば、この研究は一部の伸展感受性チャネルが電気信号を伝える以上のことを行っていることを示しています。これらは細胞の“外皮”を再構築して圧迫に耐える手助けをします。TMEM63タンパク質は膜組成、特にコレステロールによって精密に調節される機械的に活性化される脂質スクランブラーとして浮かび上がりました。この機械的回復力の仕組みは、神経線維の絶縁や耳の音を感知する細胞から、密な組織を移動するがん細胞まで、大きな力にさらされるさまざまな場面で重要かもしれません。この二重のイオンチャネル—スクランブラー機能を理解し最終的に操作できれば、脆弱な組織を保護する新たな手段や、逆に殺しにくいがん細胞を脆弱にする戦略につながる可能性があります。
引用: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
キーワード: 機械感受性イオンチャネル, 脂質スクランブリング, 細胞膜の力学, コレステロール調節, TMEM63 / OSCAタンパク質