Clear Sky Science · ja
TDP-43依存の暗号化スプライシングから生じる神経毒性の隠れたペプチド、PKN1由来
脳細胞内に潜む見えない脅威
筋萎縮性側索硬化症(ALS)やアルツハイマー病を含む多くの脳疾患では、TDP-43というタンパク質の凝集が見られます。このタンパク質が正常に機能しなくなると、神経細胞は重要なメッセージを失い、最終的に死に至ることが知られています。本研究はより驚くべき局面を明らかにします。TDP-43の機能不全は、これまで知られていなかった毒性を持つ小さなタンパク質断片を脳細胞に作らせ、それが記憶回路を損なう原因になり得るというのです。この隠れた因子を理解することは、壊滅的な認知症の診断や治療の新たな道を開く可能性があります。
細胞内の校正者がRNAを整える仕組み
ニューロンの内部で、TDP-43はRNAの校正者のように働きます。RNAはDNAとタンパク質の間にある中間的なメッセージで、TDP-43は特定の短い配列に結合してこうしたメッセージへの余分な「挿入」を阻止します。ALSや多くのアルツハイマー病の症例で見られるように、TDP-43が失われたり局在が乱れたりすると、暗号化エクソンと呼ばれる余分な断片がRNAに入り込むことがあります。これまでに知られている多くの暗号化エクソンは、メッセージを不安定にして速やかに破壊されることで正常なタンパク質の喪失を引き起こすにとどまっていました。しかし、このような出来事が新たに有害なタンパク質を生み出す可能性があるかどうかは明確ではありませんでした。
暗号化スプライスが毒性断片を生む
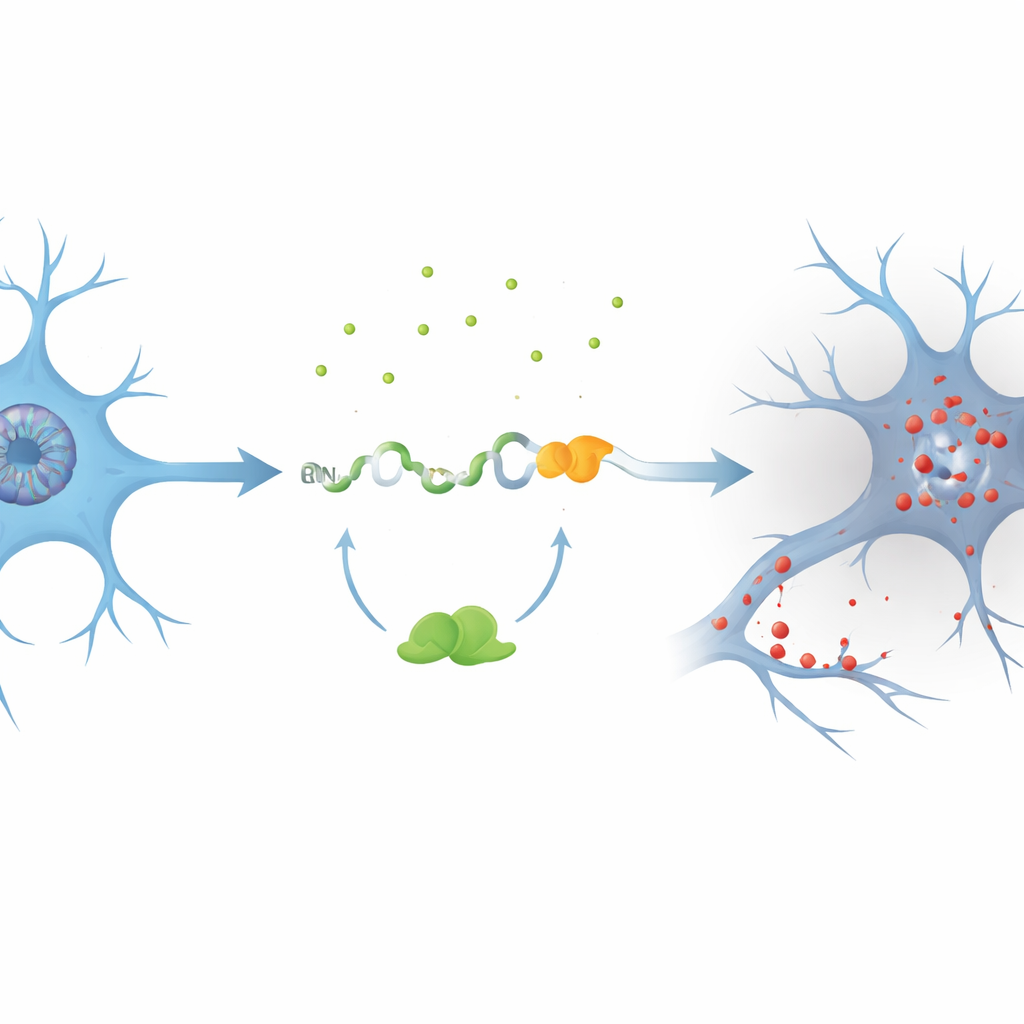
研究者たちはニューロンの内部骨格とシグナル伝達の維持に関わるPKN1という遺伝子に注目しました。TDP-43を減らした細胞モデルを使って、彼らはこれまで認識されていなかった暗号化エクソン、PKN1-5a1と名付けられた断片がPKN1のRNAの二つの通常のセグメントの間に挿入されることを発見しました。この挿入は早期終止信号を導入し、短縮されたRNAを作り出します。驚くべきことに、この欠陥のあるメッセージの一部は細胞の品質管理システムをすり抜けて翻訳され、PKN1タンパク質の最初の207アミノ酸だけを含む安定な断片が生成されます。研究チームはこの切り詰められた産物をPKN207と名付けました。彼らはTDP-43が通常、暗号化エクソンをはさむ複数のUGに富む領域に結合することでこの誤りを防いでいることを示し、その結合が失われるとエクソンがスプライスされPKN207が生成されることを明らかにしました。
患者脳と大規模データセットからの証拠
この現象が人の疾患で起きているかを調べるため、研究者たちは数百例のALS脳および脊髄サンプルのRNAシーケンスデータを解析しました。彼らは運動皮質や脊髄などTDP-43病理で影響を受けることが知られる領域でPKN1-5a1暗号化エクソンの広範な活性化を見つけた一方で、比較的保護されている小脳では見られませんでした。次に研究者たちはPKN207の固有の尾部だけを認識し、全長のPKN1タンパク質とは反応しない高特異的抗体を作製しました。リン酸化異常を示すTDP-43を伴うアルツハイマー患者の海馬組織では、これらの抗体によりPKN207に対応する明瞭なバンドが検出されたのに対し、対照脳ではそのようなバンドは見られませんでした。追加のアルツハイマーのデータセットは、暗号化エクソンが早期の病期でもオンになることを確認しており、この分子レベルの誤りが症状の顕在化よりずっと前に始まる可能性を示唆しています。
記憶に大きな影響を与えるミニタンパク質
病変を示す人の脳でPKN207が見つかったことは、核心的な疑問を投げかけます。それは有害なのか?この問いに答えるため、研究チームはウイルスを用いて若いマウスの海馬(記憶に重要な脳領域)で正常なPKN1かPKN207のどちらかを発現させました。数か月後、両群のマウスはモリス水迷路で学習障害を示し、隠された足場を見つけるのに長く泳ぐようになりました。脳脊髄液には軸索損傷のマーカーである神経原線維軽鎖の濃度が高くなっていました。培養ニューロンではPKN207を増やすと膜損傷を示す酵素の漏出により細胞損傷が引き起こされました。海馬の詳細なタンパク質プロファイリングは、シナプス強度(長期増強)やよく知られた神経変性疾患に関連する経路に広範な変化を示し、特に効率的なシグナル伝達と健全な神経繊維の足場を支える分子の強い破壊が見られました。
断片が脳の配線を乱す仕組み
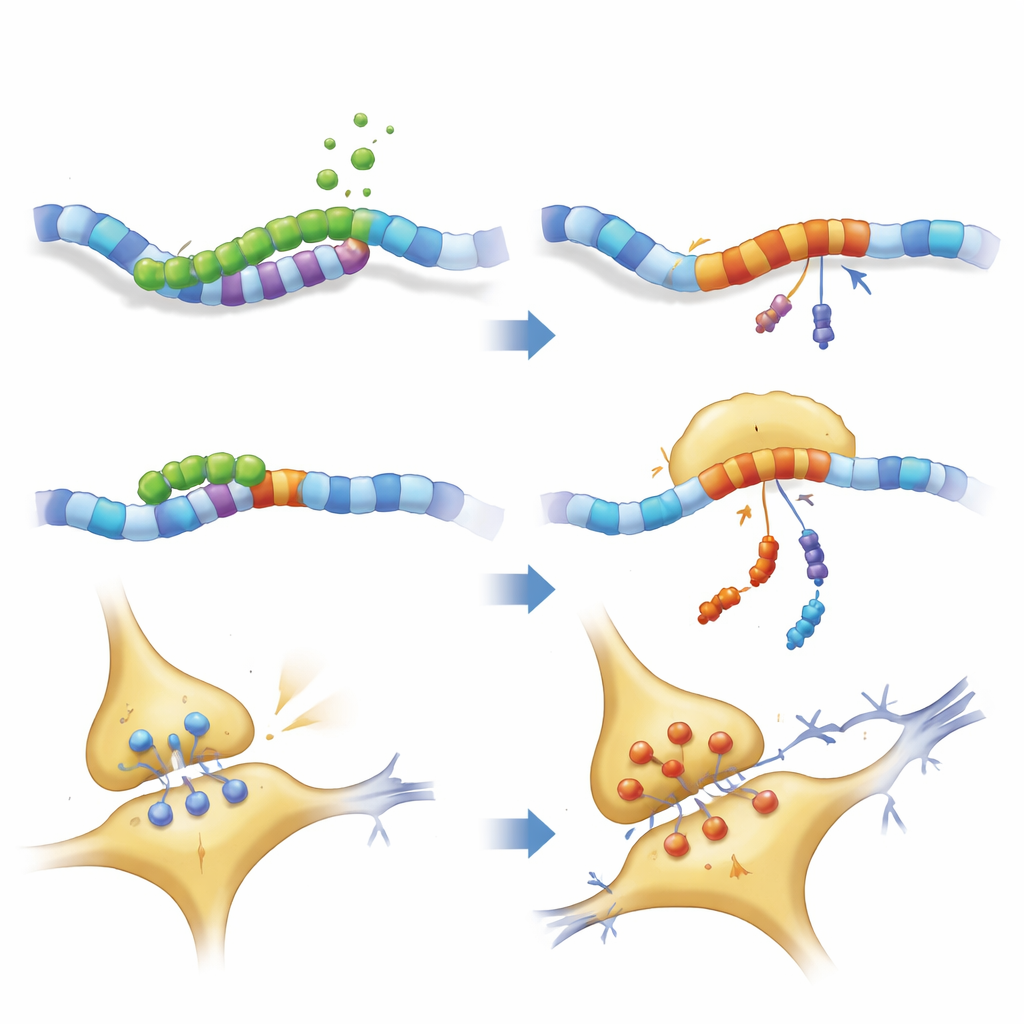
ニューロン構造の詳細観察により、全長のPKN1もPKN207も軸索の形を与え輸送を助ける神経原線維ネットワークを乱すことが示されました。主要なモーターおよび足場タンパク質が減少する一方で、いくつかの神経原線維成分が蓄積しており、輸送の渋滞や凝集の可能性を示唆します。海馬スライスからの電気生理学的記録は、PKN207を発現するマウスで長期増強が弱まっていることを裏付けました。長期増強は繰り返しの活動後にシナプスが強化される過程であり、学習と記憶の細胞基盤として広く受け入れられています。PKN207はPKN1の酵素ドメインを欠いているにもかかわらず、その存在はしばしば全長タンパク質の撹乱効果を模倣し、時に上回るほどであり、共有するN末端領域だけでニューロンの恒常性を妨げうることを示唆しています。
この発見が脳疾患にとって重要な理由
この研究はTDP-43関連疾患の理解に新たな層を加えます。重要なRNAの喪失を引き起こすだけでなく、TDP-43の機能不全はシナプスと認知を損なう安定で毒性のある微小タンパク質を生み出すことがあり得ます。暗号化されたPKN1-5a1エクソンとそのペプチド産物PKN207は、早期のTDP-43機能障害のバイオマーカーや、スプライシングを修正したり有害断片を阻害したりする治療標的の候補として注目されます。より広く見れば、本研究は他の隠れたエクソンも同様に病態を駆動するペプチドを生み出している可能性を示しており、神経変性における分子レベルの犯人たちという、これまで見落とされてきた豊かな領域を研究者に示しています。
引用: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
キーワード: TDP-43, 暗号化スプライシング, PKN1, 神経変性, アルツハイマー病とALS