Clear Sky Science · ja
代謝性チオラーゼ複合体の進化的再利用が抗生物質生合成を可能にする
日常の微生物が化学をどのように作り替えるか
私たちが頼りにする多くの抗生物質や医薬品は、細菌によって静かに合成されています。これらの小さな化学者は、分子機械としての酵素を使って複雑な防御化合物を組み立てます。本研究では、基本的な細胞の維持に使われていた中心的な代謝酵素複合体が、口腔内細菌で進化的に配線換えされ、強力な抗生物質を製造するようになった過程を明らかにします。この変化を理解することは、自然がどのように新しい化学を発明するかを示すだけでなく、次世代の薬やバイオ触媒を設計する手がかりを提供します。
基礎代謝から化学的武器へ
すべての生細胞は、脂肪の分解や必須分子の合成などの中心的代謝を担う保存された酵素群に依存しています。そのひとつ、チオラーゼ超族は通常、アセチル-CoAのような小さなエネルギー豊富分子の取り扱いや、脂質など細胞構成要素の合成経路を支えます。著者らは、いくつかの口腔連鎖球菌(Streptococcus)種で、HMGS、ACAT、および第三の補助タンパク質に関連するタンパク質から構成される三者のチオラーゼ系複合体が、本来の代謝役割を放棄していることを発見しました。代わりに、この複合体は抗生物質ルーテリサイクリンAの生合成を完了し、口腔という混み合った環境でこれらの細菌が競争するのを助けています。
抗生物質骨格上で起こる新しい種類の酵素反応
研究者たちは、Streptococcus由来の複合体を試験管内で再構成し、化学合成したルーテリサイクリンAの前駆体を供給することで、この複合体がフリーデル=クラフツ型のC–アシル化として知られる異例の炭素–炭素結合形成反応を行うことを示しました。多くの酵素が酸素にアセチル基を付加するのとは異なり、この複合体はアセチル基をピロリジン-2,4-ジオン環の炭素原子に直接導入します—これはルーテリサイクリン骨格の重要な部分です。複合体はアセチル-CoAのような天然のアセチル供与体だけでなく、いくつかの人工的供与体も受け入れ、さらには作成した結合を逆に切断する反応も行えます。この柔軟性は、生物学的アシルトランスフェラーゼの既知の機能範囲を拡大し、こうした酵素が多様な化合物を合成するように適応できる可能性を示唆します。
保存されたタンパク質足場の再利用
高分解能クライオ電顕(cryo-EM)を用いて、研究チームはSmaATaseと名付けたStreptococcus複合体の三次元構造を解明しました。新しい機能を獲得していても、SmaATaseはイソプレノイド脂質の合成に関わるメバロン酸経路の古細菌に存在する関連複合体と目立った構造的類似性を保っていました。両者は繰り返しモジュールから成る大きな多量体アセンブリーで、CoA補因子が結合して活性部位間を移動できる共有の空洞を特徴とします。しかし、元の代謝反応に必須だった主要な触媒残基は細菌版では欠けているか変化していました。生化学的試験により、SmaATaseはもはや祖先的産物であるHMG‑CoAを合成できず、アセチル‑CoAを新しい小分子基質への供与体としてのみ利用することが確認されました。
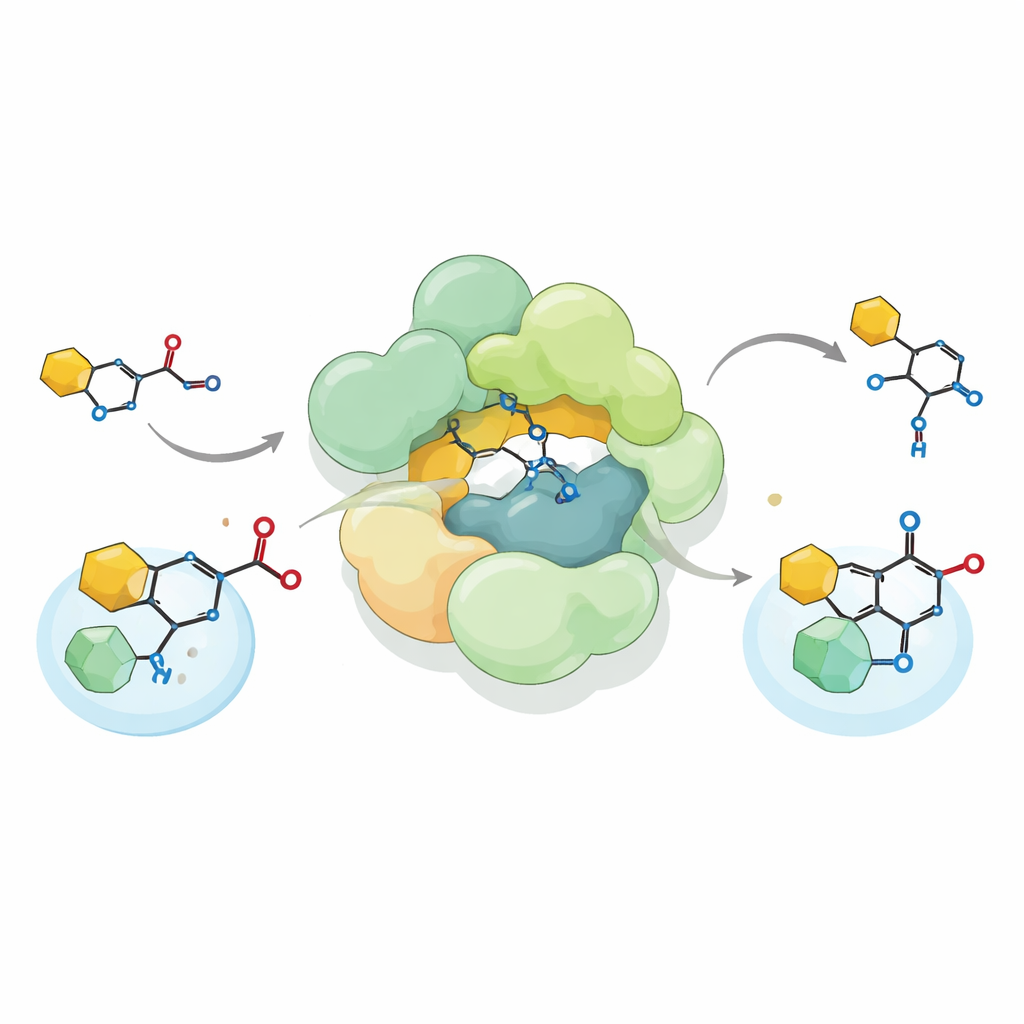
代謝から抗生物質へ至る進化の軌跡
こうした再利用がどのように進行したかを理解するために、著者らは多数の細菌や古細菌にわたる関連複合体の配列と活性を比較しました。彼らは同じ三種の酵素型を含む千を超える遺伝子クラスターを同定しました。その一部は古典的なチオラーゼ化学を維持していますが、Pseudomonasのように異なる小分子抗生物質を生産するものもあります。Pseudomonas fluorescens由来の代表的複合体はこの進化経路の中間に位置するようで、HMGS様ドメインは機能を失っているものの、ACAT様ユニットは依然としてCoA結合基質に対してより従来型の反応を行います。SmaATaseや作物保護化合物DAPGを作るPseudomonas対応体では、活性部位周辺にさらなる変化が生じ、芳香族環やテトラミン酸コアのような非標準のアクセプターを認識するように酵素が調整されていました。
なぜ小さなアセチル基が大きな違いを生むのか
最終的に、この分子改造の生物学的利益は明白です。チームがアセチル化された抗生物質ルーテリサイクリンAやDAPGをグラム陽性菌のパネルに対して試験したところ、これらの分子は強い殺菌活性を示したのに対し、非アセチル化の前駆体ははるかに弱いかほとんど不活性でした。再利用された酵素複合体が正確な位置に付けたその小さなアセチル基は、控えめな骨格を強力な兵器へと変え、口腔中のStreptococcusや植物根圏のPseudomonasが近隣を出し抜くことを可能にします。本研究は、進化がどのように既存の酵素フレームワークを最小限かつ戦略的な変異でリサイクルし、日常的な代謝機構を化学的防御のための専門的ツールに変えるかを示すとともに、薬剤探索や合成生物学のための炭素–炭素結合形成触媒を設計する際の設計図を提供します。
引用: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
キーワード: 酵素の進化, 天然物の生合成, 抗生物質化学, 代謝の再利用, フリーデル=クラフツ アシル化