Clear Sky Science · ja
ヒトiPSCベースの肺線維症モデルが示す p300/CBP 阻害による肺胞過渡的細胞状態の抑制
肺の瘢痕化が私たち全員に関係する理由
特発性肺線維症(IPF)は、肺が徐々に瘢痕組織に置き換わり、呼吸が次第に困難になる厳しい疾患です。現在の薬は進行を遅らせることはできますが、しばしば重大な副作用を伴います。本研究は最先端の幹細胞およびゲノミクス手法を用いて、ラボ内で瘢痕化した肺を再現し、重要で単純な問いに答えようとしています:損傷した肺細胞を有害な状態から回復へ向かわせるスイッチを見つけられるか?
培養で再現する瘢痕化した肺の窓
IPF を探るため、研究者らはヒト誘導多能性幹細胞(iPSC)からミニ肺を作製しました。これらのiPSCは酸素が血液に入る小さな気嚢を覆う肺胞細胞へと分化させられ、瘢痕を形成する結合組織細胞である肺線維芽細胞とともに培養されました。柔らかなゲル内に埋め込まれたこれらの「肺胞オルガノイド」は実際の肺組織に似た振る舞いを示しました。化学療法薬ブレオマイシン(肺障害を誘発することで知られる)に曝露すると、線維芽細胞がゲルを引き縮め、線維化で見られる組織の収縮を模倣しました。
この系を用いて、チームは264種の低分子化合物ライブラリをスクリーニングし、各薬剤がゲルの収縮をどれだけ防ぐかを自動で計測しました。ディープラーニングベースの画像解析ツールが客観的な読影を担いました。多くの化合物は効果を示しませんでしたが、明らかに目立った一群がありました:DNAの梱包や遺伝子の発現制御に関与するタンパク質 p300 と CBP の阻害剤です。ライブラリ中の8つの p300/CBP 標的化化合物はいずれも低用量で収縮を抑え、この経路が線維化に対する有望な手がかりであることを示しました。 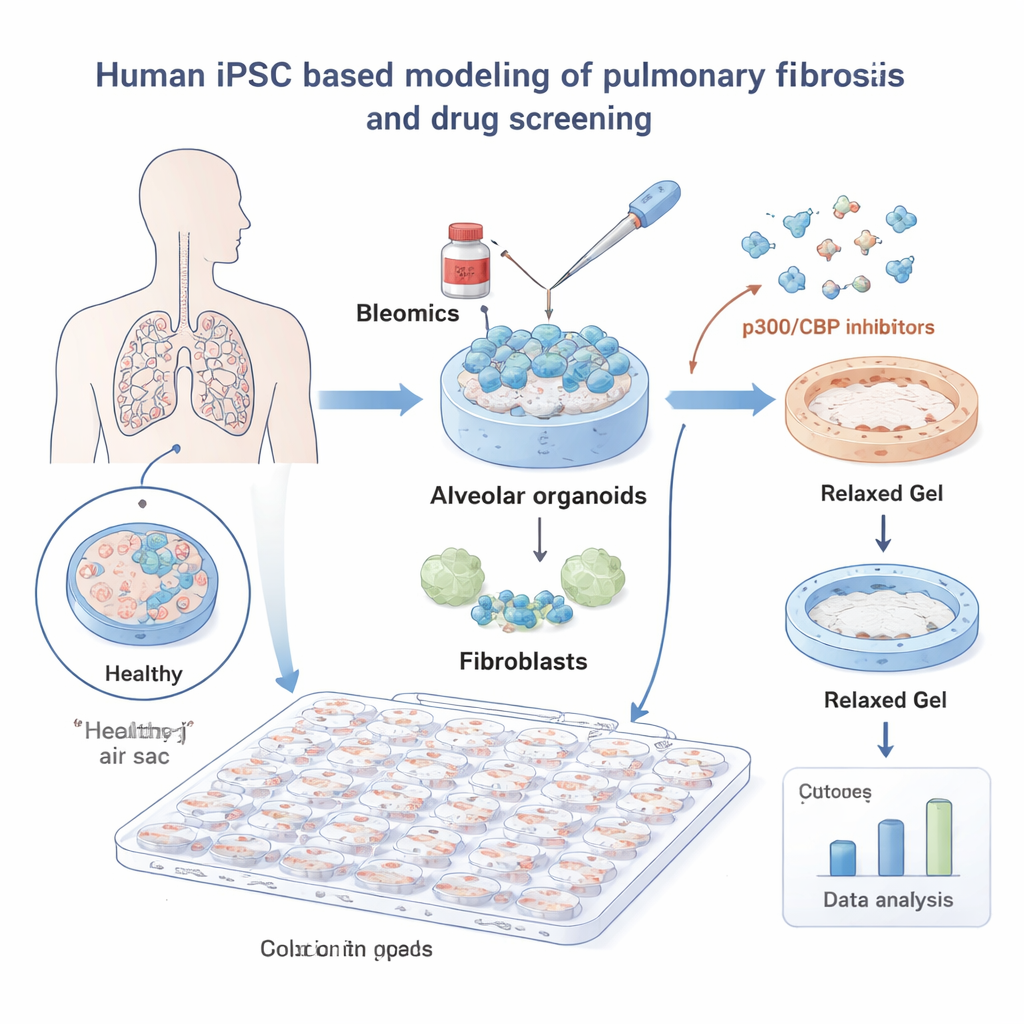
問題を引き起こすのは:過渡的な肺細胞
最近の研究は、疾患肺に問題を起こす「中間」的な細胞状態――肺胞過渡的細胞状態――を明らかにしました。通常、支持的な AT2 細胞は極めて薄い AT1 細胞へ成熟し、気嚢を覆ってガス交換を可能にします。しかし IPF では、AT2 細胞がしばしばこの過渡的な状態で立ち往生し、ストレス応答や修復に関わる遺伝子を発現しつつ、機能的な AT1 への分化を完了できません。これらの過渡的細胞は線維化領域に集積し、線維芽細胞と強くコミュニケーションしますが、単なる損傷の副産物か、あるいは瘢痕化を能動的に駆動する元凶かは不明でした。
オルガノイドでのRNAシーケンシングとオープンクロマチンプロファイリングにより、モデルで出現する過渡的細胞はIPF患者の肺で見られるものと密接に一致することが示されました。誘導された過渡的細胞はストレス、炎症、マトリックス再構築の遺伝子サインを示し、共同培養された成体肺線維芽細胞を強く活性化しました。重要なのは、p300/CBP を阻害すると過渡的状態のマーカーが低下し、AT2 の同一性がよりよく保持され、線維芽細胞の活性化が弱まったことです。換言すれば、薬剤は細胞を広く毒殺するのではなく、AT2 細胞がこの有害な中間状態に陥るのを選択的に防いでいました。
分子スイッチの解明
p300/CBP がどのように細胞運命の決定に影響するかを探るため、チームはDNAを梱包するヒストン上の化学的修飾を調べました。特に H3K27 アセチル化は、活性化されたエンハンサーやプロモーターで p300/CBP によって付与されることが多い修飾です。過渡的細胞では、ストレス応答や線維化促進遺伝子の近傍領域に強い H3K27 アセチル化が存在し、AP‑1 や HNF1B といった転写因子の結合部位が濃縮していました。p300/CBP 阻害剤で処理すると、これらの部位でのアセチル化マークは減少し、多くの線維化促進遺伝子の発現が低下しました。AP‑1 を直接阻害するか、AP‑1 と HNF1B を小分子干渉RNAで低下させると、同様に過渡的プログラムとオルガノイドの収縮が抑えられ、p300/CBP、AP‑1、HNF1B の三者が線維化再構築を駆動する機構に結びつきました。
培養系の外でも、研究はブレオマイシン誘発肺障害マウスに対して阻害剤 CBP30 を試験しました。CBP30 を投与された動物では過渡的上皮細胞が減少し、瘢痕形成性の筋線維芽細胞の活性化が弱まり、線維化マーカーの発現も低下しました。ヒトの幹細胞モデルと動物モデルの相互検証は、p300/CBP が単なるラボ上のアーティファクトではなく肺の瘢痕化を制御する実在の因子であることを裏付けます。 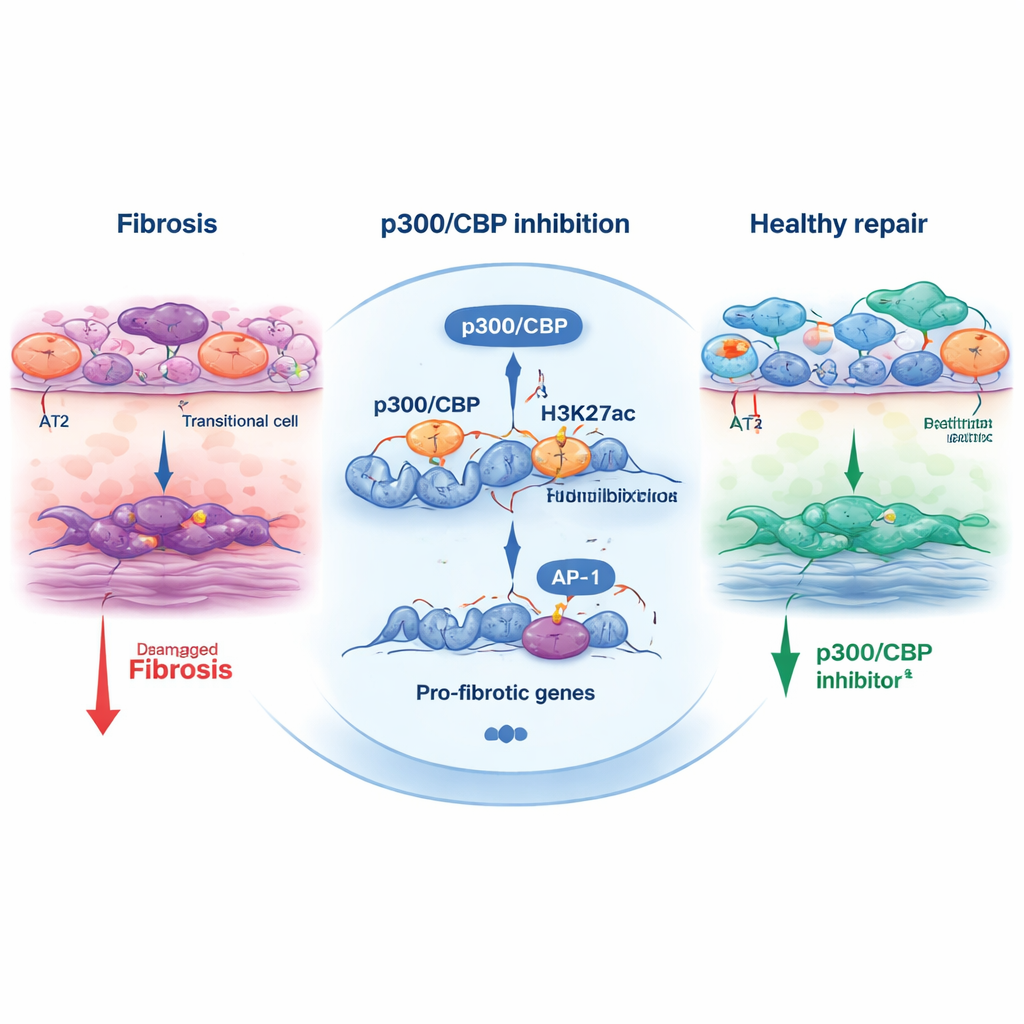
将来の治療への含意
専門外の読者にとっての要点は、著者らが現実味のあるヒト線維化肺モデルを構築し、それを用いて新たな薬剤標的を浮き彫りにしたことです。彼らの仕事は、肺の瘢痕化が一部は可逆的なストレス誘導型の過渡的細胞状態によって駆動され、周囲組織を誤った方向へ導いていることを示唆します。p300/CBP を抑えることで、この状態を鎮め、肺胞細胞を健全な発達経路に留め、線維芽細胞を過剰活性化させるシグナルを減らせる可能性があります。p300/CBP 阻害剤は安全性の最適化と臨床試験を要しますが、本研究はIPFの結果をただ遅らせるのではなく、根本的な細胞間の誤った情報伝達に対処する治療法の方向性を示しています。
引用: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
キーワード: 特発性肺線維症, 肺胞オルガノイド, p300/CBP 阻害剤, 過渡的上皮細胞, 肺幹細胞