Clear Sky Science · ja
人工的な複製起点を備えたプラスミドの設計
微生物のDNAを書き換える意義
インスリン生産から最先端の遺伝子回路に至るまで、現代のバイオテクノロジーの多くの道具はプラスミドと呼ばれる小さな環状DNAに依存しています。これらの遺伝的ワークホースは改変遺伝子を細菌に運びますが、その基本設計は何十年もほとんど変わっていません。本研究は、プラスミドの核心—細胞にいつどれだけコピーするかを指示する配列—を完全に再設計できることを示します。コピーの「エンジン」を基礎から作り直すことで、調整や組み合わせ、プログラムが容易なプラスミドを作り出し、診断、バイオ製造、合成生物学の柔軟性を大きく広げます。
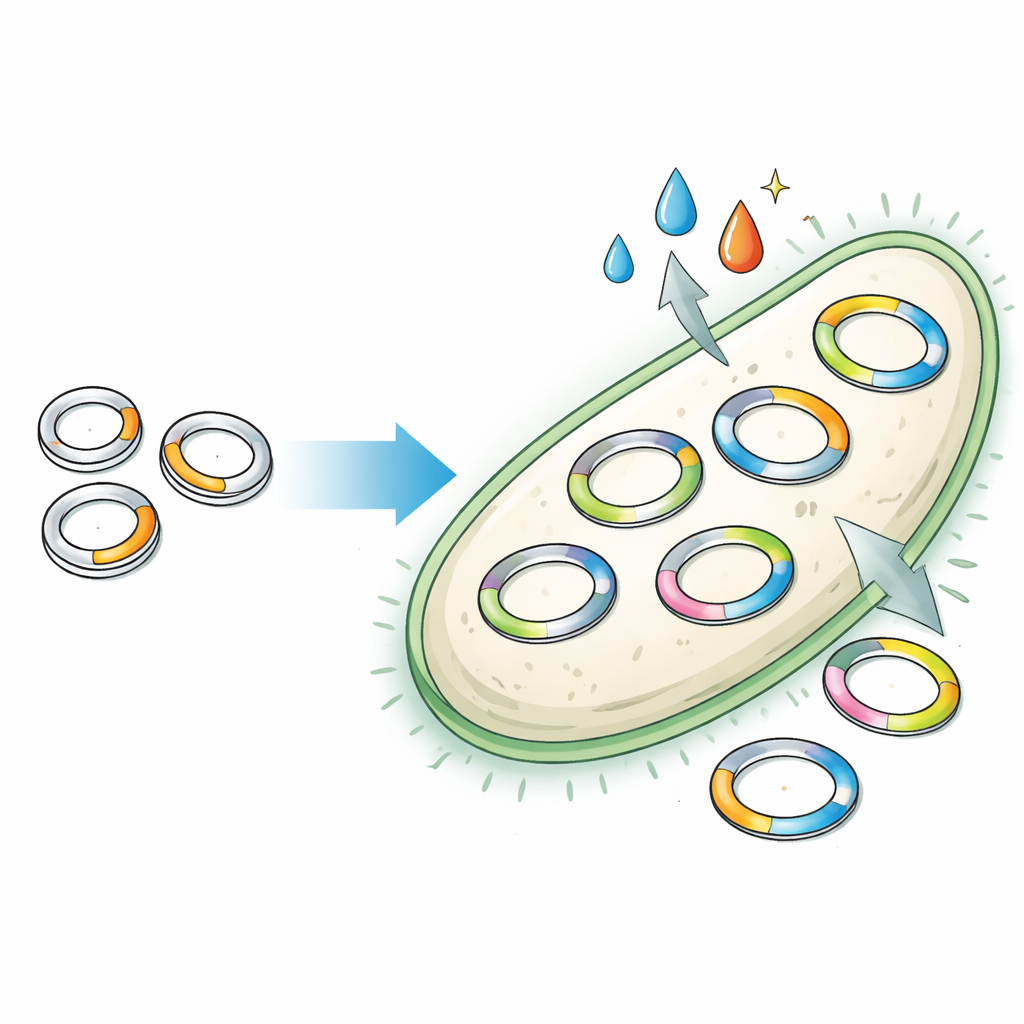
古い道具に潜む制約
プラスミドは本来、抗生物質耐性や新たな栄養源の利用法などの性質を細菌間で共有するために進化した可動性のあるDNAです。研究室ではエンジニアがこれらを借用して有用な遺伝子を運ばせますが、ほとんどは1980年代に発見されたいくつかの古典的設計に依存しています。これらの古い設計には、プラスミドが細胞内に何コピー存在するかや異なるプラスミド同士が共存できるかを制御する、重なり合った遺伝的要素の入り組んだ絡みが隠れています。これらの部位が結合しているため、ある機能を変えると別の機能が予測不能に壊れることがあります。その結果、研究者は固定されたコピー数や限られた互換性を持つ限定的なプラスミドの選択肢に縛られ、設計の複雑さが制限されてきました。
コピーエンジンを一から作り直す
研究者たちはpMB1プラスミドファミリーに由来する広く使われている複製起点に着目しました。自然型では、この起点は複製を始めるRNAとそれを抑えるRNAという二者の精密なやり取りによってコピー数を維持しています。チームはまずこのシステムを「リファクタリング」しました。重複する遺伝子を分離し、埋もれていたプロモーターを無効化し、重要な構成要素を別々のクリーンなカセットに配置しました。これによって、複製起点の核心的な機能は保たれつつ構成が単純化され、進化によって形作られた複雑な部位がモジュール式で扱いやすい機械に近づきました。
合成の制御ノブを差し込む
もともとの制御ロジックが露出したことで、著者らはそれを完全に合成の調節器と置き換えました。複製プライマーを設計されたRNAスイッチに接続し、それらを調光器のように機能させました:小さな制御RNAがスイッチを切り替えてプライマーの産生を許可または遮断し、結果としてプラスミドの複製を制御します。異なるスイッチ変異体と強弱の異なるプロモーターを組み合わせることで、プラスミドのコピー数を2桁を超える範囲で調節しました。さらに制御カセットのDNA上での物理的配置も検討し、安定性を向上させつつ複製領域をコンパクトな機能コアに縮小し、問題となるプラスミド間の干渉を防ぐ自然由来の補助システムを追加できる配置を見出しました。
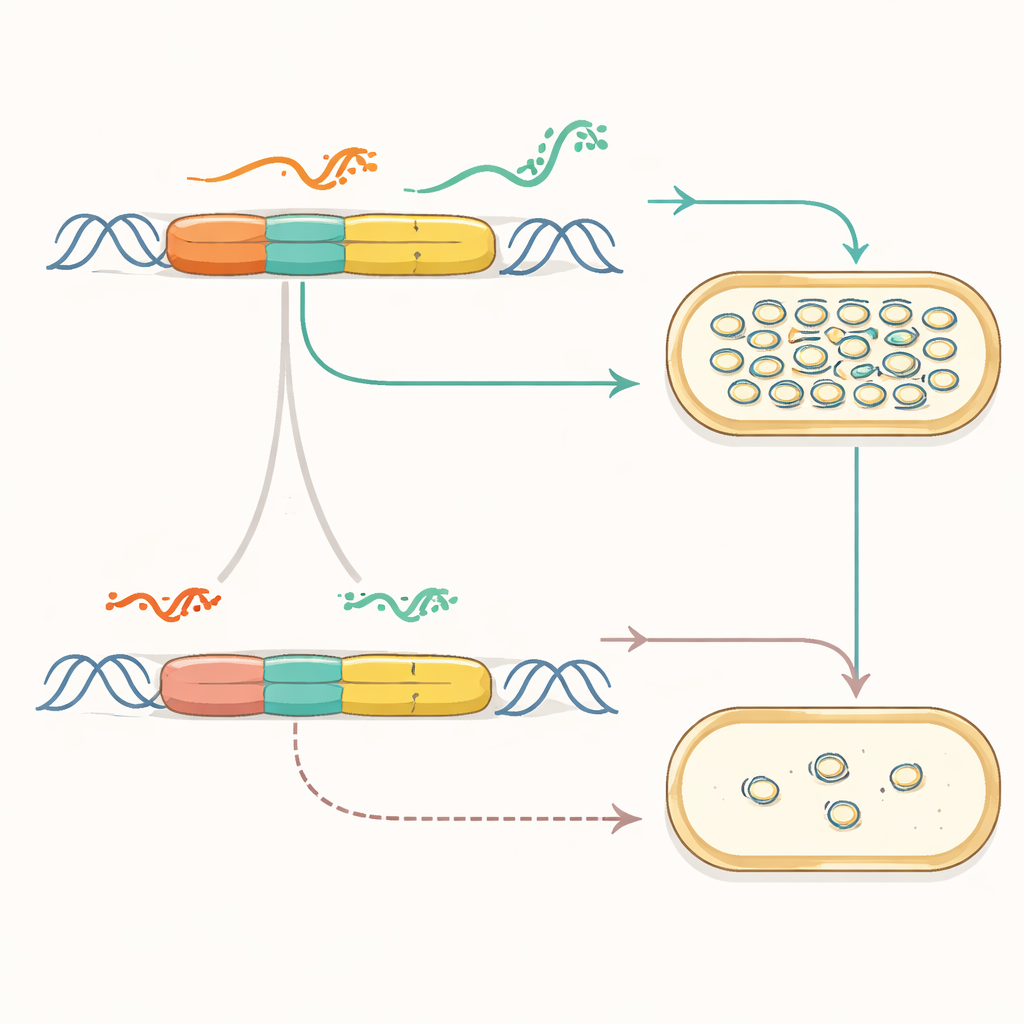
化学信号をDNAコピー数に変換する
コピーエンジンがモジュール化されると、それを外界に感知させる配線が可能になりました。研究者らは合成起点を誘導型プロモーターや、小分子に応答して形を変えるリボスイッチと接続しました。これらの新しいプラスミドでは、IPTGやクメートのような化学物質を加えるとプラスミドのコピー数—ひいてはレポーター信号—が上がったり下がったりしました。複数の信号を組み合わせ、ある化学物質が複製を駆動し、別の化学物質がそれを抑えるといった制御も可能にしました。研究者らはさらに異なる化学に応答するプラスミド対を作り、同一細胞内でDNAシーケンシングを用いてそれらのコピー数の変化を追跡し、事実上プラスミドのカウントを環境履歴のバーコードに変換しました。
1細胞内の多数のカスタムプラスミド
このアプローチの重要な試験は、複数の独立制御されたプラスミドが共存できるかどうかでした。直交するRNA調節器のライブラリを利用して、チームはそれぞれ独自の合成起点と抗生物質マーカーを持つ6種類のプラスミドを構築し、これらを同時に大腸菌に導入しました。数日間にわたる全プラスミドシーケンシングは、相対的な存在比が変動する一方で6種類すべてが残存していることを確認しました。同じことを従来の6つのプラスミドで試みたところ失敗し、リファクタリング設計と安定化システムの追加が、新しいプラスミドを単一細胞内で混雑した状態でもより互換性があり頑健にしていることを強調しました。
将来のバイオテクノロジーへの示唆
専門外の人にとっての要点は明快です:著者らはプラスミドを硬直したワンサイズの道具からカスタマイズ可能なプラットフォームに変えました。彼らの合成複製起点は、速度、感度、入力を必要に応じて選べるプラグアンドプレイのエンジンのように機能します。これにより、化学暴露をDNAコピー数の変化として記録する細菌の構築、複数のプラスミドに遺伝経路を分配して並列で多数の経路を試験すること、あるいは工業株で増殖と生産のバランスを精密に調整することが可能になります。安定性に関するトレードオフはいくつか残るものの、本研究はプラスミド複製の基本的な仕組みがもはや工学の手の届かない領域ではないことを示し、合成生物学における新たな革新の余地を開きます。
引用: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
キーワード: 合成プラスミド, 複製起点, RNA 調節因子, コピー数制御, 合成生物学