Clear Sky Science · ja
抗TLR2免疫療法はマウスおよびヒトモデルにおけるニューロンからオリゴデンドロサイトへのαシヌクレイン伝播を調節する
この研究が重要な理由
多系統萎縮症(MSA)は稀ではあるが進行の速い脳疾患で、パーキンソン様の運動障害に加え、血圧低下などの姿勢や自律神経の障害を伴います。医師は症状を和らげることはできますが、現時点で病気の進行を遅らせる手立てはありません。本研究は、誤った折りたたみをしたタンパク質が脳細胞間でどのように広がり「配線の絶縁」であるミエリンを損なうかを明らかにし、標的化した抗体治療が動物および細胞モデルでこの過程を遮断できることを示しています。この成果は、症状を治療するだけでなく、MSAの経過を変える可能性のある具体的な薬物的戦略を示唆します。
脳の配線がどのように誤るか
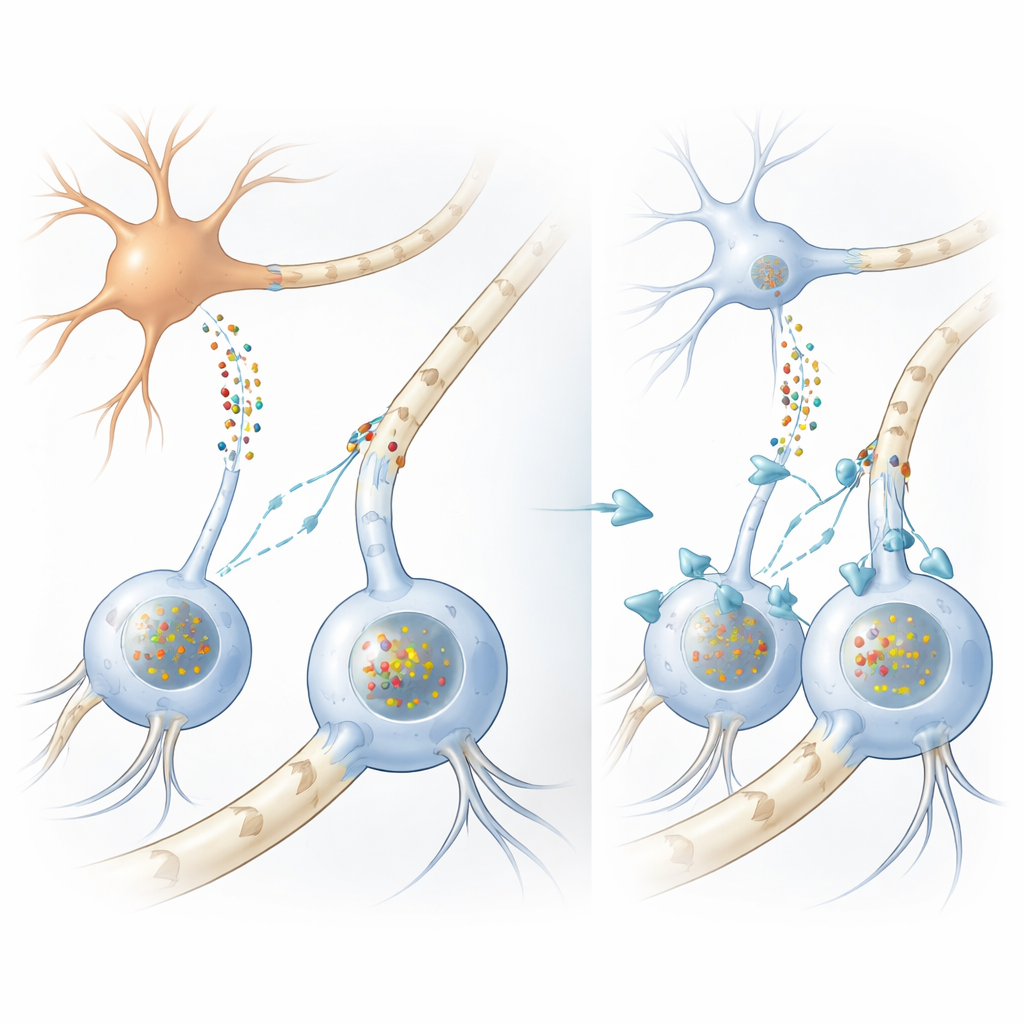
パーキンソン病を含む多くの運動障害では、αシヌクレインと呼ばれるタンパク質の凝集が神経細胞内に蓄積します。しかしMSAでは、最も顕著な凝集は支持細胞であるオリゴデンドロサイト内に形成されます。オリゴデンドロサイトは通常、神経繊維を脂質性のミエリン鞘で包んで電気信号を高速化しますが、奇妙なことにこれらの細胞自身はほとんどαシヌクレインを作りません。では、これらの細胞内の大量のタンパク質沈着はどこから来るのかという長年の謎がありました。著者らはまず、人間の脳サンプルと大規模なRNA解析を用いて、オリゴデンドロサイトが実際にニューロンよりはるかに少ないαシヌクレインを産生していることを確認し、有害なタンパク質は外部から到来するに違いないという考えを裏付けました。
タンパク質はニューロンから支持細胞へと渡る
これを検証するために、研究チームはいくつかの補完的なモデルを構築しました。培養皿内で、神経幹細胞から分化させたヒトのオリゴデンドロサイト様細胞に、αシヌクレインを大量に放出するよう遺伝子操作したニューロン様細胞から採取したコンディショニング培地を与えました。支持細胞はこのタンパク質を取り込み、MSA脳で見られるグリア内包と非常によく似た凝集を形成し、同じ化学的修飾や補助タンパク質を伴っていました。さらに、ニューロンだけでヒト変異型αシヌクレインを産生するマウス系統を調べると、オリゴデンドロサイトがヒト遺伝子を発現していないにもかかわらず、白質内にヒト由来のタンパク質凝集が見られました。これらの実験は総じて、αシヌクレインがニューロンからオリゴデンドロサイトへ移行し、そこで病的な内包を形成しうることを示しています。
細胞表面の門
次に、研究者たちはタンパク質がどのようにオリゴデンドロサイトに侵入するかを問いかけました。先行研究は、免疫センサーであるトール様受容体2(TLR2)がニューロンやミクログリアの細胞表面でαシヌクレインのドッキングサイトとなることを示していました。MSA脳の遺伝子発現データを解析したところ、患者のオリゴデンドロサイトは対照に比べて異常に高いレベルのTLR2を持ち、TLR2が高いほどミエリン関連遺伝子(例えばミエリン塩基性タンパク質〈MBP〉)の発現が低いことが関連していました。この関係は複数の独立したパーキンソン病データセットでは観察されず、TLR2を介したオリゴデンドロサイトのαシヌクレイン感受性は、すべてのシヌクレイン疾患に共通する特性ではなくMSAに特有の特徴であることを示唆しています。
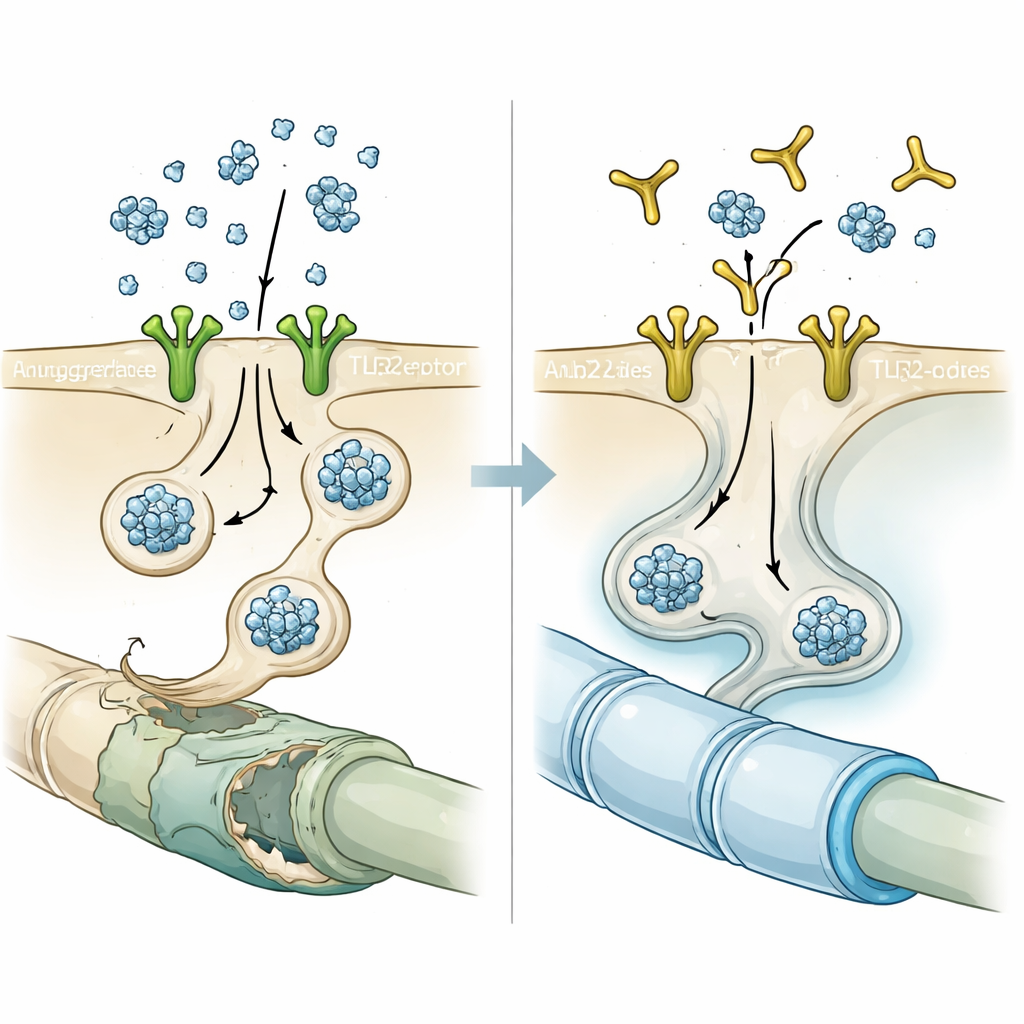
抗体で門を遮断する
この手がかりをもとに、研究者らはTLR2に結合してその活性化を阻害するよう設計された抗体NM-101を試験しました。細胞培養では、ニューロン由来のαシヌクレインを添加する前に短時間オリゴデンドロサイトをNM-101で前処理すると、内包様凝集の数と強度が大幅に減少しました。ニューロン性のαシヌクレインを過剰産生するマウスや事前に形成したαシヌクレイン繊維を注射されたマウスでは、週1回のNM-101投与により白質での凝集タンパク質が減少し、ミクログリアやアストロサイトからの炎症反応が鎮められ、オリゴデンドロサイト内の炎症性酵素カスパーゼ-1の活性化が低下しました。治療を受けた動物は寿命が延び、運動試験の成績も改善し、抗体の保護効果が単なる顕微鏡的な観察にとどまらない機能的意義を持つことを示しました。
損なわれた絶縁を回復する
オリゴデンドロサイトは脳のミエリンを作る細胞であるため、研究チームはαシヌクレインの移行がミエリンを損なうか、TLR2遮断がこれを改善するかを検討しました。ニューロン由来のコンディショニング培地中のαシヌクレインにさらされたヒト由来オリゴデンドロサイトの単一細胞RNAシーケンシングは、成熟してミエリンを生産する状態から離れ、未熟で前駆的なプロファイルへと広範にシフトし、多くの主要なミエリン遺伝子の発現が低下していることを明らかにしました。レーザーで切り出したMSA患者とマウスモデルのオリゴデンドロサイトの遺伝子発現解析でも共通の署名が示され、ミエリンの形成および維持に関与する遺伝子の発現が低下していました。電子顕微鏡観察では、αシヌクレインマウスの白質は薄く混乱したミエリン鞘を示しました。NM-101治療はこれらの変化の多くを逆転させ、ミエリンを肥厚させ、ミエリンタンパク質のレベルを回復し、オリゴデンドロサイトの成熟に必要な遺伝子の発現を正常化しました。
将来の治療への意味
本研究は明確な筋書きを支持します。MSAではニューロンが産生したαシヌクレインがオリゴデンドロサイトの表面にあるTLR2を介して浸入し、そこで蓄積して炎症を引き起こし、細胞の発生プログラムを狂わせ、脳の配線のミエリン被覆を侵食します。TLR2を標的とした抗体でこれを遮断することで、研究者らはマウスおよびヒト細胞モデルでこの一連の事象を中断し、有害な内包を減らし、炎症を鎮め、ミエリンを修復し、生存と運動機能を改善しました。NM-101自体はヒトでの厳格な試験がまだ必要ですが、本研究はTLR2依存のタンパク質移行をMSA様病理の主要な駆動因子として位置づけ、抗TLR2免疫療法がこの破壊的な病気を遅らせるか防ぐための有望な戦略であることを示しています。
引用: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
キーワード: 多系統萎縮症, αシヌクレイン, オリゴデンドロサイト, ミエリン障害, 免疫療法