Clear Sky Science · ja
逆方向に並ぶCsuピリがAcinetobacter baumanniiの3次元バイオフィルム組立を駆動する
病院菌が守られた「都市」を築くしくみ
最も手強い病院由来の病原体の一部は、バイオフィルムと呼ばれる粘性のある三次元コミュニティに身を潜めることで抗生物質を生き延びます。本研究は一見単純だが極めて重要な問いを扱います:個々の細菌はどうやって頑強で層状の構造を織りなすのか?最先端の電子顕微鏡で拡大して観察したところ、危険な病原体Acinetobacter baumanniiが自身を保護的な三次元の塊に織り込むための、生物学的な“ベルクロ”のような毛状フィラメントが見つかりました。この隠れた足場構造を理解することで、バイオフィルムを分解して既存の薬剤の効果を高める新たな手段が開ける可能性があります。
細菌同士をつなぐ微小な毛
A. baumanniiは治療が難しい病院感染の主要因であり、表面にCsuピリと呼ばれる細い毛状突起が密生しています。以前の研究でこれらのピリが頑丈なドーム状バイオフィルムの形成に不可欠であることは示されていましたが、個々の細胞をどのようにして三次元構造に編み上げているかは不明でした。複数の電子顕微鏡手法を用い、著者らはまず浮遊培養ではピリが各細胞から単独で突き出している様子が棘のようであることを確認しました。しかし、密な表面上に形成されたコロニーでは様相が大きく変わります:多くのピリが密に詰まり、隣接する細胞間に広く平らな帯を作り、三次元にわたる繊細に見えるが広がりのあるメッシュワークを形成していました。 
対向するフィラメントで作られる平らな梯子状構造
これらの帯がどのように形成されるかを解明するため、チームはCsuピリを精製して単独での挙動を観察しました。数日から数週間にわたり、単一のフィラメントが対を成し、次第に多本の“スーパー積層”へと融合し、最終的に実際のバイオフィルムで観察された構造をよく模倣するゼリー状ネットワークを形成しました。高分解能のクライオ電子顕微鏡により、その基礎となる設計が明らかになりました。各ピリは滑らかな管状ではなく、ジグザグ走行する棒状です。二本の棒が逆向きに並ぶと、繰り返し現れる角点で接触して安定した側方接合を形成します。多くのこうしたアンチパラレルな対が並ぶことで非常に薄いシート状の積層、すなわち幅は多数フィラメント分あるが厚さは一フィラメント分しかない微細な梯子やリボンのような構造ができあがります。
三次元成長のための組み込みブループリント
詳細な構造解析は、この積層能がピリ自身の幾何学に組み込まれていることを示します。ジグザグのパターンは非常に短い間隔で繰り返し、多数の潜在的接触点を各フィラメントに提供します。その結果、二本のピリが正しい向きで出会うと、ファスナーのように接合が連鎖的に形成されてシートが急速に伸長します。重要なのは、棒の向きが通常同一細胞内のピリ同士ではなく異なる細胞由来のピリ同士で接触が生じるようになっている点で、これが自然に細胞間の結びつきを促進します。積層は柔軟で伸縮性があるため、成長するバイオフィルムは物理的な応力を吸収して破断しにくくなります。さらに、細胞分裂時に新しい娘細胞のピリがしばしば相対向きに配置されることが観察され、まさに細胞を三次元クラスターに結びつける必要な場所で積層形成が促されることがわかりました。 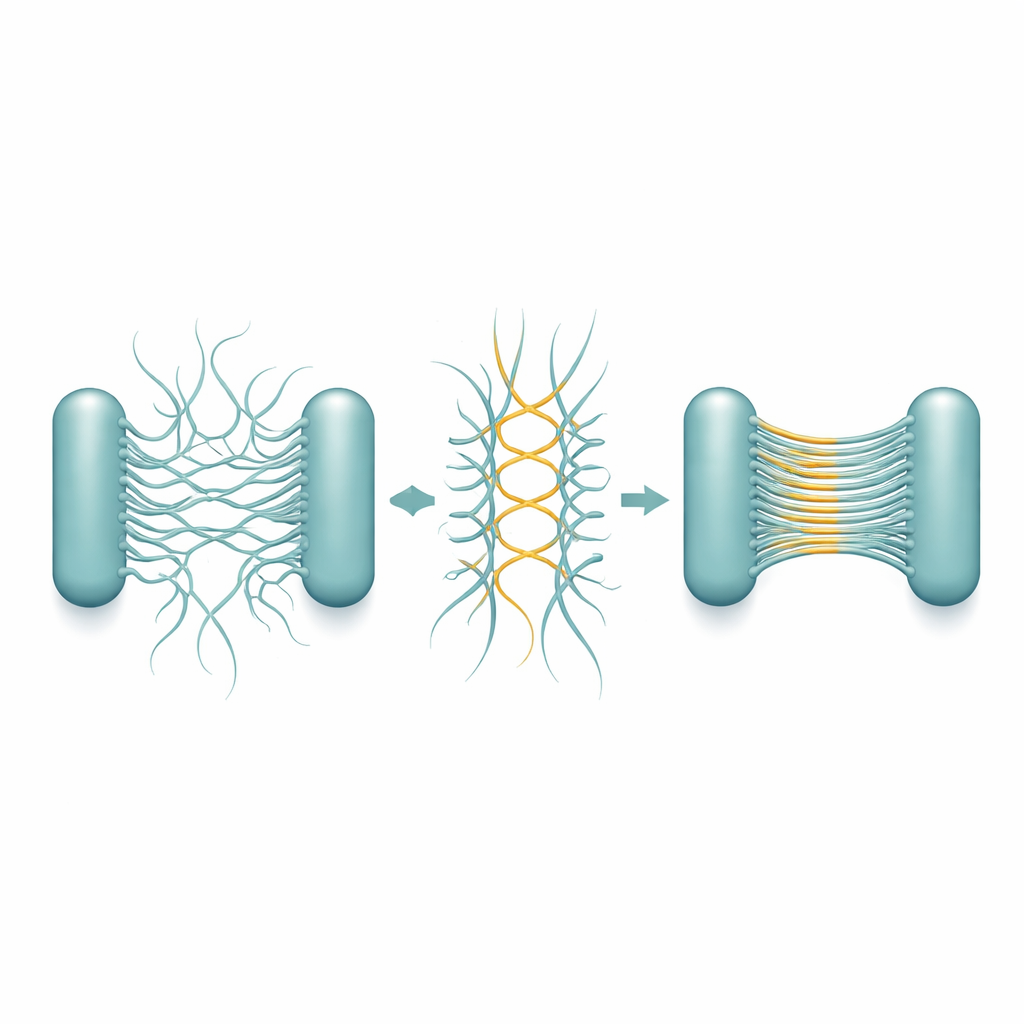
接着材、充填物、初期の足場
研究はまたバイオフィルムの他の成分がどのように寄与するかも調べました。PNAGと呼ばれる糖性ポリマーや壊れた細胞由来の遊離DNAは成熟したバイオフィルムに蓄積することが知られています。顕微鏡観察により、これらの物質が細菌間の狭い隙間を埋め、ピリの積層を包み込む様子が示され、まるで鉄筋の周りに注がれたコンクリートのようでした。しかし、チームがPNAGとDNAを除去しても、細菌はCsuピリ積層だけで整理された筏(ラフト)を形成しました。これはピリが一次的な足場を構築し、周囲の物質が後からそれを固め安定化させることを示しています。
細菌の要塞に対する新たな弱点
簡潔に言えば、本研究はA. baumanniiがどのように表面の毛で自らを丈夫な多層クラスタに編み込み、薬剤や免疫細胞が浸透しにくい状態を作り出すかを説明します。ピリはまずフックとして表面に取り付き、その後フレキシブルなストラップとして平らなシートに積み重なり、隣接する細胞をあらゆる方向で結び付けます。糖性ポリマーやDNAが隙間を埋めることで、このストラップネットワークは堅固な要塞へと変わります。ピリ同士の接触がどのように成立するかを正確に突き止めたことで、新たな標的が浮かび上がります:ピリ–ピリ接触を阻害する薬剤や分子はバイオフィルムの足場を内部から弱め、長引く細菌感染の除去を容易にする可能性があります。
引用: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
キーワード: バイオフィルム, Acinetobacter baumannii, ピリ(毛状突起), 抗生物質耐性, クライオ電子顕微鏡