Clear Sky Science · ja
ウイルス模倣は大腸炎で腫瘍抑制因子として働く
がんと闘う隠れたDNA
私たちのDNAの奥深くには、かつて「ジャンク」と片付けられていた広大な領域が存在します。本研究は、そのような隠れた配列のいくつかが、慢性的な腸の炎症を抱える人々を大腸癌の発生から守ることがあると示しています。これらのDNA要素は細胞内で偽のウイルス感染のように振る舞い、内部の警報システムを作動させて、がんを引き起こす危険な幹細胞を抑制します。
目覚めうる眠ったDNA
ヒトゲノムのほぼ半分は、トランスポゾンと呼ばれる反復配列で構成されています。これらは増殖して移動できるDNAの断片です。健康な細胞では、こうした要素はDNAメチル化などの化学的な目印で強く抑え込まれ、静止しています。しかし特定の疾患や一部の抗がん薬による治療後には、これらが再び活性化されることがあります。活性化されると、異常な二本鎖RNAを産生し、細胞にとってはウイルス由来の遺伝物質に非常によく似たものとして認識されます。
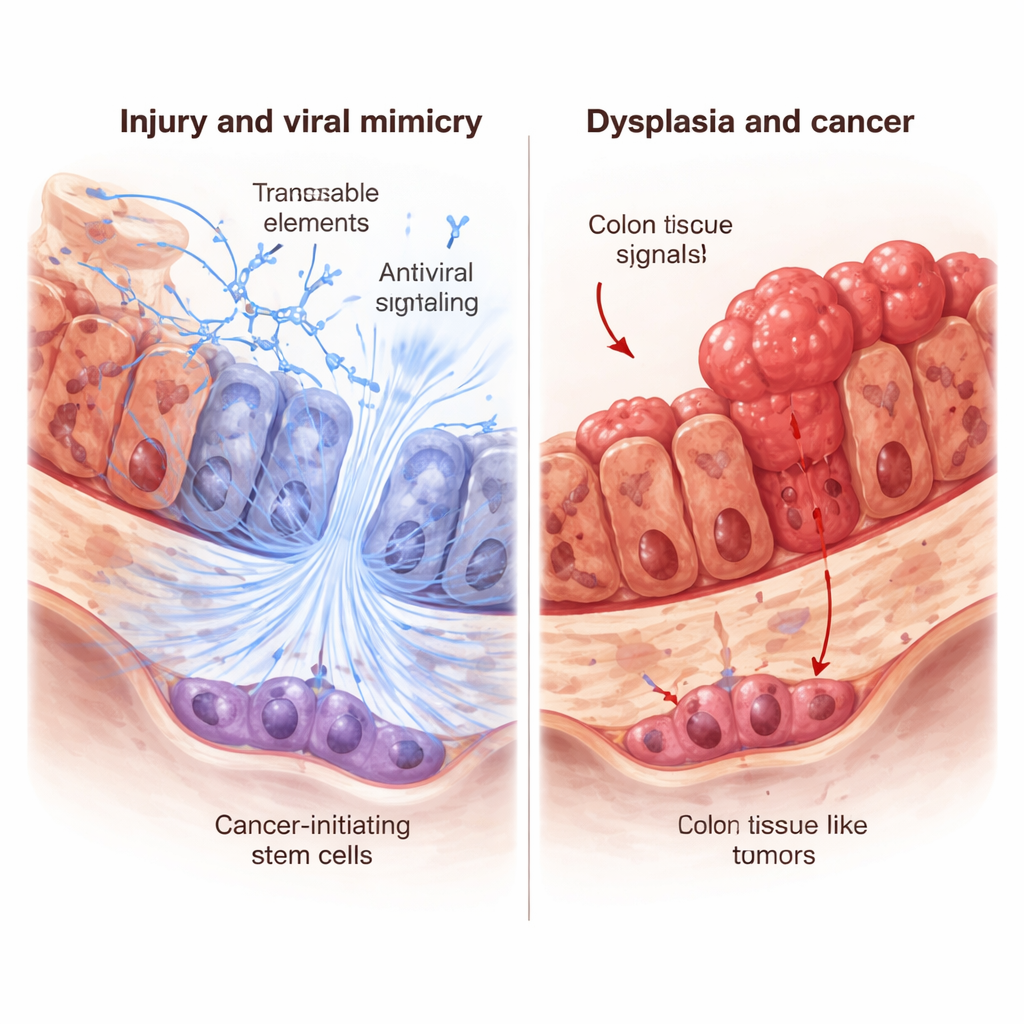
炎症を起こした腸での偽ウイルス警報
研究者たちは炎症性腸疾患(IBD)の患者の大腸組織と、実験的に大腸炎を誘導したマウスの組織を調べました。ヒトとマウスの両方で、活発な炎症はトランスポゾンの活動増加とインターフェロン遺伝子の強い活性化に結びついていました。インターフェロンは体の抗ウイルス警報系の一部であり、この現象は「ウイルス模倣」として知られます。しかし、長期間のIBDが前がん状態(異形成)や大腸癌に進行した患者を調べると、逆のパターンが見られました。トランスポゾンとインターフェロン関連遺伝子の双方が抑えられていたのです。これはウイルス模倣反応の消失が慢性炎症から癌へ至る過程の一段階である可能性を示唆します。
DNAメチル化を下げて腫瘍を阻止する
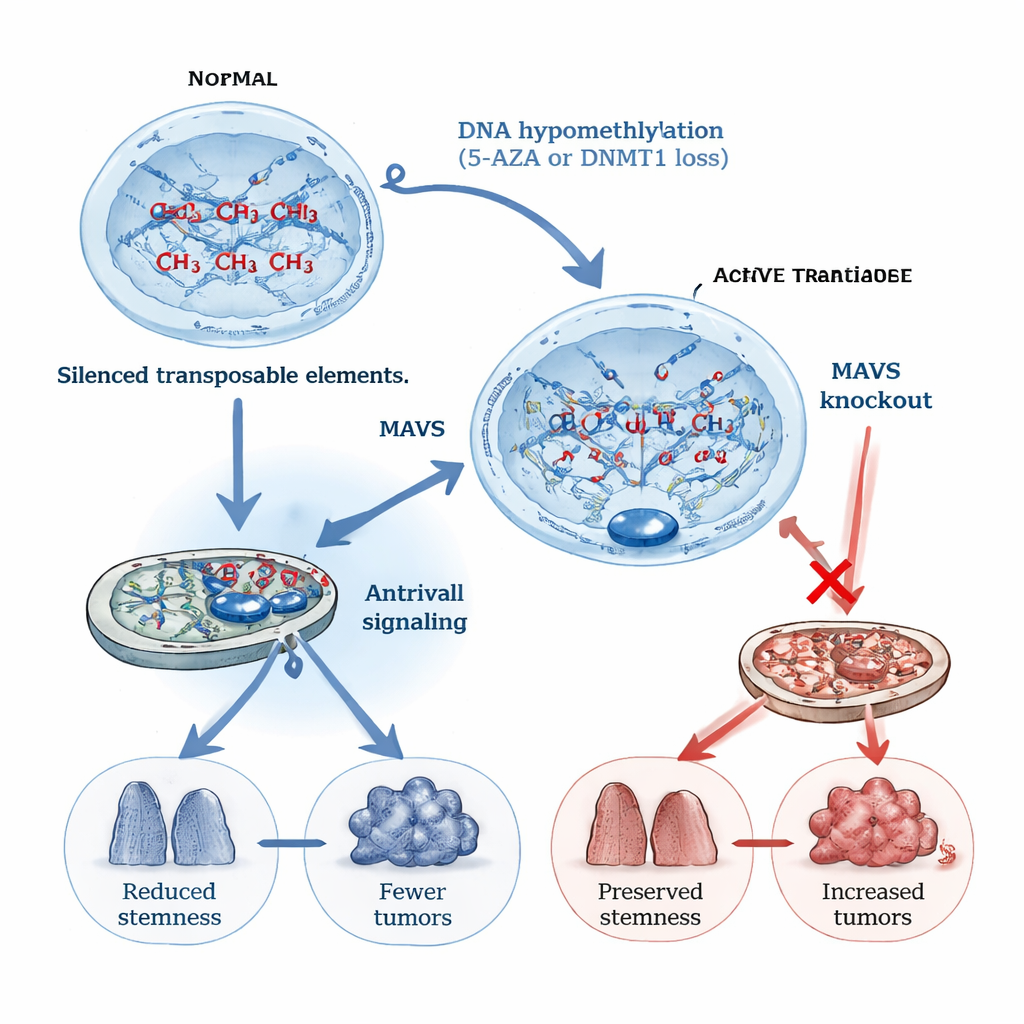
この偽ウイルス警報を高めることが実際に癌の形成を止めうるかを検証するために、研究チームは大腸のDNAメチル化を低下させる2つの方法を用いました。1つは一部の血液がんで用いられる薬剤5‑AZA、もう1つはDNAメチル化を維持する主要酵素DNMT1を、がんを起こしうる稀なDCLK1陽性細胞に特異的に遺伝子欠失させる方法です。化学的損傷と炎症の組み合わせで駆動されるマウスモデルでは、5‑AZA処置とDNMT1欠失のいずれでも腫瘍数が減り、場合によっては腫瘍が小さくなりました。これらの変化は広範なDNA脱メチル化、多くのクラスのトランスポゾンの強い再活性化、インターフェロンおよびJAK/STATシグナルの高まりを伴い、ウイルス模倣が誘導されたことを裏付けました。
警報を無効にすると発がん性細胞が解き放たれる
抗ウイルスタンパク質MAVSはミトコンドリア上に局在し、細胞内のウイルスRNAセンサーからのシグナル伝達に不可欠です。著者らはマウスでMAVSを欠損させると、5‑AZAやDNMT1欠失がもたらす腫瘍抑制効果が消失することを示しました:腫瘍は増加し、生存率は悪化しました。培養皿内で育てたミニ大腸組織(オルガノイド)では、DNA脱メチル化によるウイルス模倣の活性化が、APC変異を持つDCLK1細胞の幹細胞性や新たなオルガノイド形成能を鋭く低下させました。MAVSを取り除くとこの阻害は逆転し、DNAが脱メチル化された状態でも幹様の振る舞いと増殖が回復しました。これらの実験は、ウイルス模倣が免疫細胞の助けを必要とせず、細胞自律的に発がん性幹細胞性を抑えることを明らかにしました。
患者にとっての意味
慢性大腸炎を抱える人々にとって、大腸癌の発症への不安は現実的な問題です。本研究は、再覚醒したトランスポゾンが作り出す内部の「ウイルス警報」が体の自然防御の一部である可能性を示唆します。その警報が作動していると、損傷した細胞が完全ながん幹細胞になる能力が制限され、警報が消えると腫瘍はより容易に発生し得ます。DNAメチル化やその制御因子を標的にしてウイルス模倣を慎重に増強する治療法は、将来的に長期の炎症性疾患を抱える高リスク患者の大腸癌の予防や治療に役立つ可能性があります。
引用: Larsen, F., Jeong, W., Schep, D. et al. Viral mimicry acts as a tumor suppressor in colitis. Nat Commun 17, 1313 (2026). https://doi.org/10.1038/s41467-026-68850-1
キーワード: ウイルス模倣, 大腸炎, 大腸癌, トランスポゾン(転移因子), DNAメチル化