Clear Sky Science · ja
イソギンチャクにおける神経運命決定の細胞・転写経路は成体神経新生の二つの様式を明らかにする
単純な海洋生物がどのように新しい脳細胞を作り続けるか
ヒトを含む多くの動物は、神経細胞の大部分を幼少期に作り、その後はほとんど生成を止めます。しかし、イソギンチャクのように一見単純な生物の中には、成体になっても新しい神経細胞を追加し続けるものがあります。本研究は、ヒトデの仲間ではないものの星形の小型イソギンチャク(Nematostella vectensis)が、どのように拡散型の神経系を恒常的に更新・再編成しているかを調べ、脳を成長・修復するための古代的な解決策を反映する可能性のある戦略を明らかにします。
成長する個体には成長する神経網が必要だ
イソギンチャクには脳はなく、体壁に張り巡らされた網状の神経網を持ちます。これらの動物は餌の有無で成長したり縮んだりするため、神経網もそれに応じて拡大・縮小する必要があります。著者らは光感受性蛍光タンパク質をタイムスタンプとして用い、幼若な成体の既存ニューロンをマーキングし、その後1週間にわたって新たに出現する細胞を追跡しました。すると、体軸に沿って散在する豊富な新生ニューロンが見つかり、特定の成長領域に限られないことが示されました。新生細胞は口側と反対側の両端に現れ、成体神経新生が空間的に広くかつ継続的であることを示しています。
新しい神経細胞の起源を追う
これらの新生細胞がどこから来るのかを明らかにするため、研究者らはライブイメージングと単一細胞RNAシーケンシングを組み合わせました。後者は数千の個々の細胞でどの遺伝子が活性化しているかを読み取る技術です。彼らは3つの主要遺伝子によって制御される蛍光“レポーター”を持つ細胞に注目しました:FoxL2、SoxC、Elav。FoxL2は分裂する多能性を持つ前駆細胞の広いプールを示し、SoxCは細胞が分化を始める際に短時間オンになり、Elavは主に小さなシグナルペプチドで情報を伝達するペプチド作動性ニューロンで強く活性化します。チームは、FoxL2陽性かつPiwi1陽性の前駆細胞集団が幹細胞のように振る舞い、自己複製を続けながらニューロン、刺胞細胞(cnidocytes)、分泌細胞など多様な子孫を常時生み出していることを示しました。一方でSoxCとElavは、これらの前駆細胞プールを離れて特定の神経運命にコミットする際にのみ点灯します。
成体ニューロンへの二つの異なる経路
レポーターの時系列を各細胞の遺伝子発現パターンと照合することで、研究は成熟した神経細胞への二つの明確な経路を明らかにしました。ペプチド作動性ニューロンは直接的な経路をたどります。すなわち、すでに“ペプチド作動性にコミットした”分子プロファイルを持つ前駆細胞から生じ、速やかにさまざまなニューロン亜型へと分化します。各亜型の新規個体は、その亜型が既にどれだけ一般的であるかに応じた割合で出現し、システムが特定の型を偏重するのではなくバランスのとれた混合を維持していることを示唆します。この系統では明確な中間段階の連続は見られず、むしろ類縁性の高いニューロン亜型が同様に準備された前駆細胞から並行して出現します。 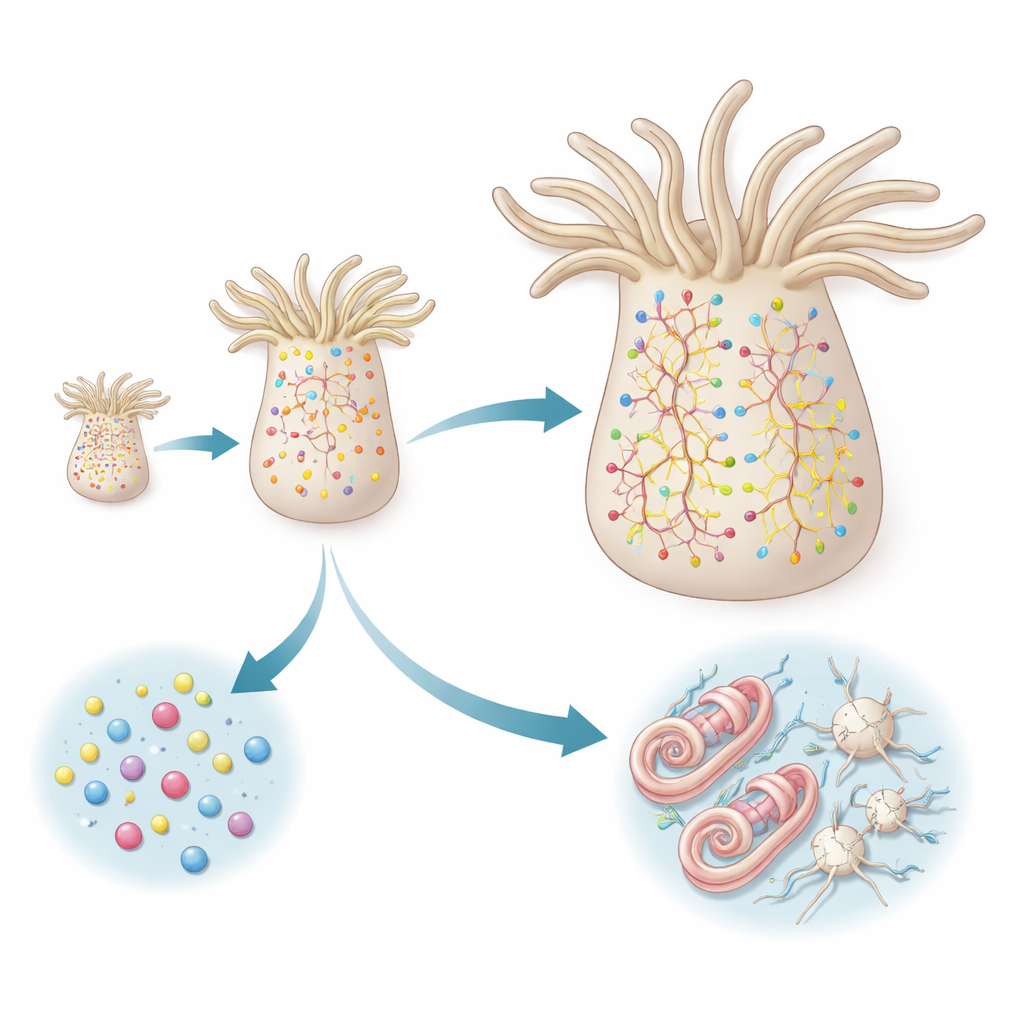
刺胞細胞という特殊なケース
刺胞細胞(cnidocytes)は、より段階的な経路をとります。まず「カプセル構築」段階を経て、微視的なハープーンを発射できる加圧された特徴的な小器官を形成します。この段階は他の細胞型にはほとんど見られない一連の調節遺伝子と構造タンパク質に依存します。中間プログラムが完了した後に初めて刺胞細胞は二段目の、より従来型の神経プログラムをオンにし、電気的シグナル伝達に必要なイオンチャネルなどの構成要素を付け加えます。初期段階で停止する変異体から得られた遺伝データはこの二段階モデルを補強しており、その移行を阻害すると後期の神経的特徴が出現しなくなることを示しています。 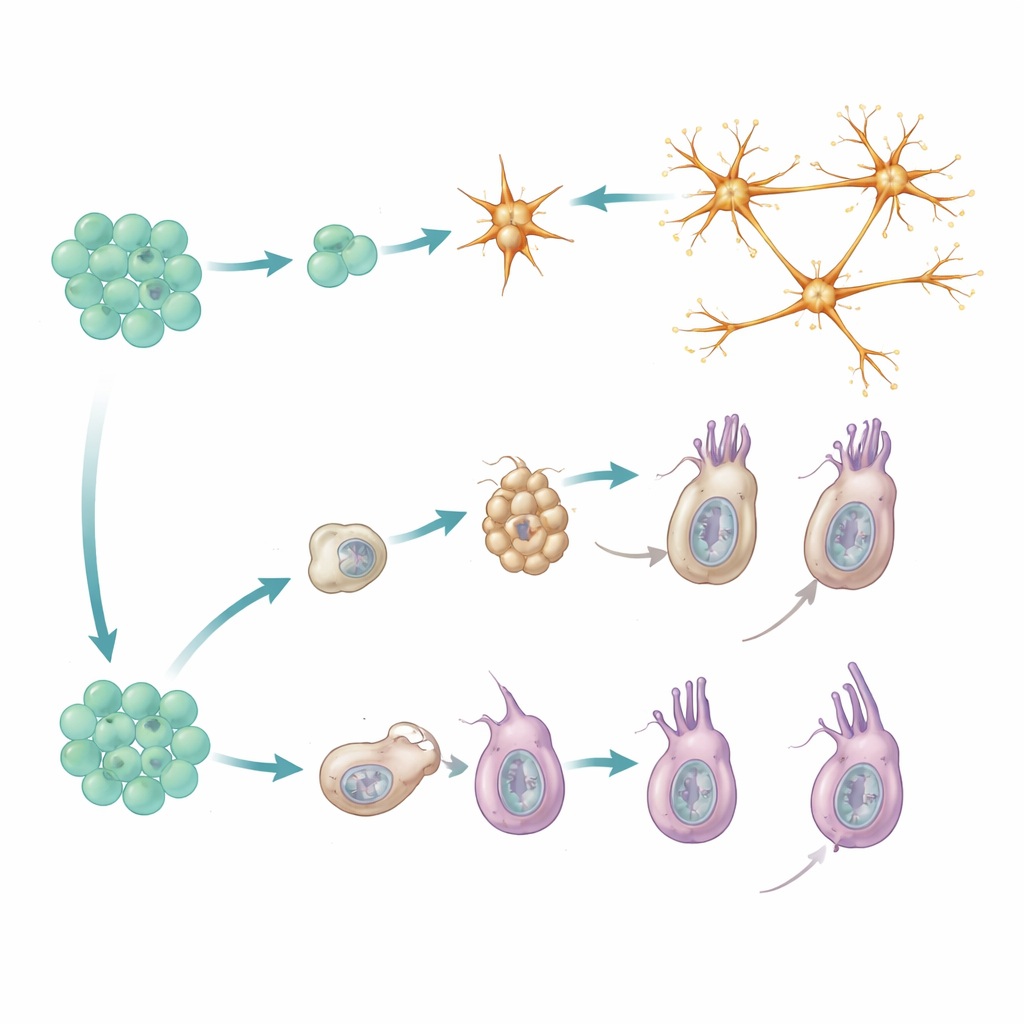
共有される規則と古代の起源
異なる経路をたどるにもかかわらず、ペプチド作動性ニューロンと刺胞細胞はいずれも同族の調節遺伝子群に依存してその同一性を確立します。広範な神経的特徴はbHLHおよびbZIP転写因子に関連し、各ニューロン亜型の細かい同一性はホメオドメイン遺伝子と亜鉛フィンガー遺伝子の独特の組み合わせによって指定されます。これは、線虫や脊椎動物を含むより複雑な動物でニューロン型が定義される仕組みを想起させる“コード”です。著者らは、幹細胞様の前駆細胞、コミット時の一過性SoxC活性、亜型を決定するホメオドメインコードといったモジュール化された戦略が、神経新生の深く保存された原理を表している可能性があると主張します。イソギンチャクではこれらが神経網の生涯にわたる更新とスケーリングを支え、他の動物では関連する機構が限定的な成体神経新生や一部系統に見られる顕著な再生能力の基盤となっているかもしれません。
引用: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
キーワード: 成体神経新生, イソギンチャク, 神経前駆細胞, 刺胞細胞(ニドサイト), 単一細胞トランスクリプトミクス