Clear Sky Science · ja
細胞内で安定した相互作用ハブを形成するペプチドコアセルベートの導入
細胞内に新しい「作業場」を構築する
細胞の中には、エネルギー産生やストレス応答のような重要な作業が行われる小さな作業場が多数存在します。加齢や病気に伴い、これらの自然の作業場は機能不全に陥ることがあります。本研究では、短い合成ペプチドから作った簡単な液滴を用いて、生きた細胞内に新たな「相互作用ハブ」を導入する方法を探りました。これらの合成ハブは特定のタンパク質を捕捉して濃縮し、さらにはそれらを分解するのに役立つことが示されており、将来の治療や細胞工学の新たな戦略を示唆します。
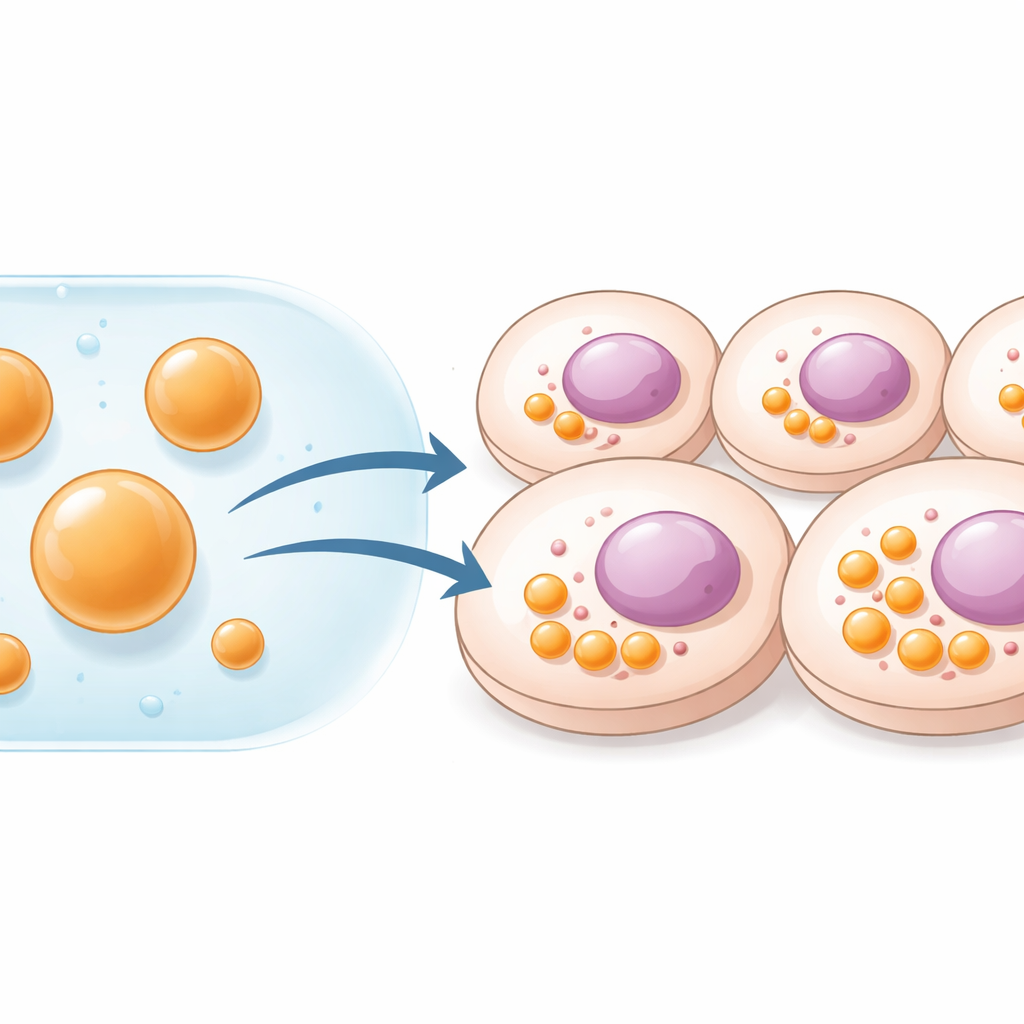
なぜ細胞にカスタム作業場が必要か
細胞はさまざまな作業を異なる区画に分けて秩序を保っています。ミトコンドリアのように膜で囲まれたものもあれば、特定のタンパク質やRNAが集まって生じる柔らかい液滴状の構造もあります。これらの流動性のある凝縮体は反応センターとして働き、特定の生化学経路を促進または抑制します。これまで、研究者たちは遺伝子を導入して細胞に特別な足場タンパク質を作らせることでこうした区画を設計してきましたが、この方法は遺伝子導入を必要とし、細胞が生産できる量に制約があります。本研究の著者らはDNAを介さず、外部で既製の区画を作り、それを安定したミクロンサイズの液滴として直接導入するというアプローチを採りました。
安定したハブを形成するペプチド液滴
研究チームは短く無秩序なペプチドであるHBpepと、酸化還元応答性の変異体HBpep‑SAを用いました。弱酸性条件ではこれらのペプチドは溶解したままですが、pHを生理的近傍に戻すか温度を下げると、直径約1〜5マイクロメートルの柔らかくゲル状の液滴へ相分離します。ペプチド濃度を調整することで、液滴のサイズと数を制御できました。蛍光法を用いると、液滴内のペプチド分子はゆっくりと移動しており、希釈や取り扱いに耐える十分に頑丈なゲル状態であることが示されました。これらをヒトのがん細胞、マウスのメラノーマ細胞、一次ヒト免疫細胞の培養に加えると、液滴は効率よく取り込まれ細胞質に蓄積しました。特に大きな液滴は少なくとも5日間形を保ち、細胞内で長寿命の合成オルガネラのように振る舞いました。
ハブへの搭載と標的化
これらのハブを実用的にするには、貨物タンパク質を保持して整理できる必要があります。研究者らはまず、標的タンパク質であるGFPに短いHBpep由来のタグを付けることで搭載性を向上させました。このタグはGFPが液滴へ強く分配することを促し、興味深いことに表面近くに濃縮されてコア–シェルの構造を生みました。次に、特定の標的に強く結合する小型の抗体様タンパク質であるナノボディを液滴内部に組み込みました。GFP結合ナノボディを入れたハブは、試験管内でも細胞内でも選択的にGFPを捕捉しました。ペプチドゲルは比較的密であるため、最初は捕捉されたGFPの大部分が液滴表面に蓄積しましたが、内部構造を部分的に緩める(酸化還元条件を変える、あるいは液滴が周囲のエンドソーム膜から逃れるのを助ける)と、GFPは内部へも浸透し始めました。細胞内では、エンドソーム脱出を促進する化学的補助剤が、標的を呼び込むことに成功するハブの割合を大きく増やしました。
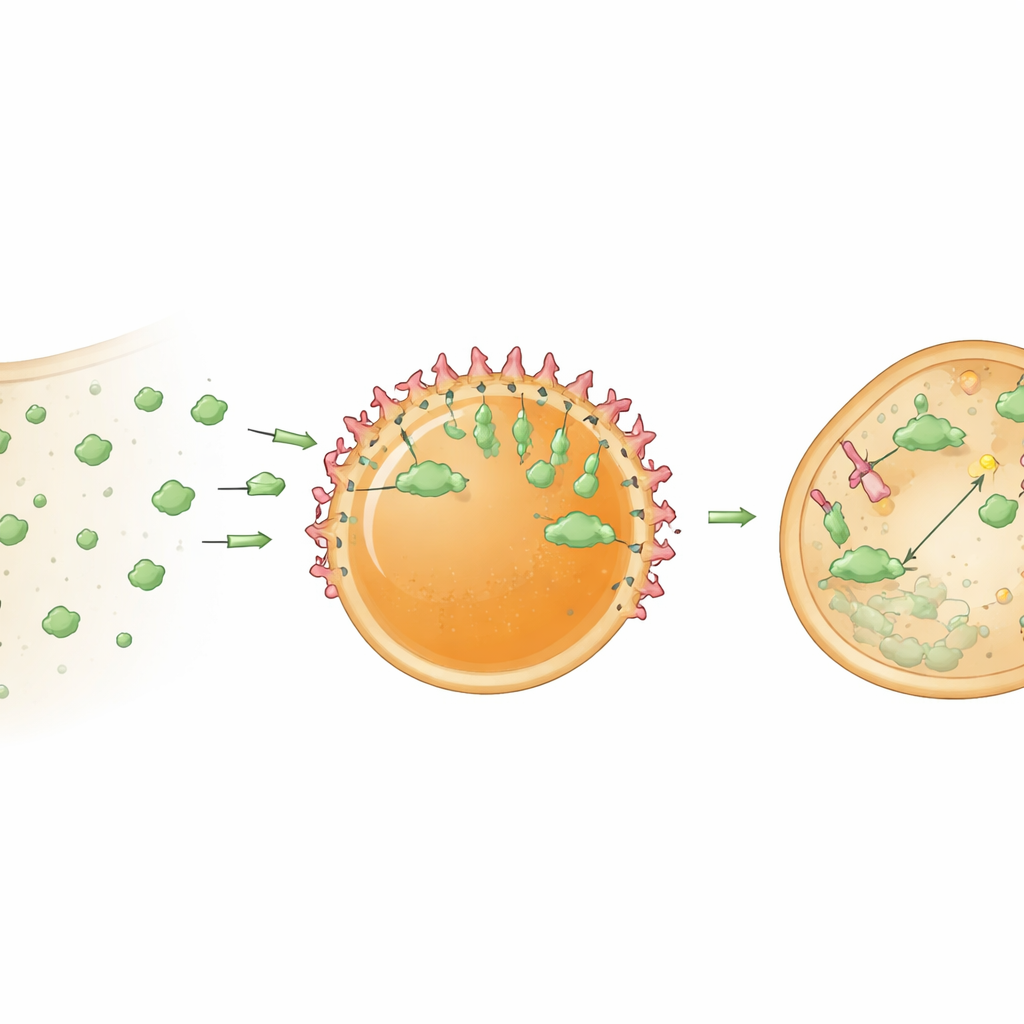
ハブをタンパク質分解マシンに変える
著者らは次に、これらのハブを受動的なトラップから能動的な処理センターへとアップグレードしました。彼らは液滴にbioPROTACを搭載しました。これは、標的に結合するナノボディと、細胞の廃棄機構がタンパク質を標的化するためのアダプターの一部を融合したタンパク質です。「デグラドソーム」液滴が細胞内に導入され、GFPを安定的に発現する細胞では、細胞質中のGFP量が1日以内に約78パーセント減少しました。ナノボディのみを含む対照ハブはGFPを隔離したものの、全体量を有意に低下させなかったため、観察された大きな減少は単なる捕捉ではなく標的特異的な分解によるものであることが確認されました。この結果は、bioPROTACを濃縮された微小環境内にクラスタリングすることが、細胞質中に自由に拡散しているときよりもはるかに強力に働くことを示唆します。
将来の治療法にとっての意義
平たく言えば、本研究は研究室でペプチドベースの液滴を作製し、カスタムのタンパク質ツールを詰め、それらを生きた細胞に導入して新しく長寿命のオルガネラのように振る舞わせることができることを示しています。これらの合成ハブは自然のタンパク質を選択的に引き寄せ、分解機構を搭載すれば特定の標的を能動的に除去することができます。細胞の遺伝子を改変せず、搭載可能な要素がモジュール化されているため、有害なタンパク質の除去や故障したシグナル伝達の書き換えといった細胞の挙動を回復・再構築する治療へとつながる道を開く可能性があります。
引用: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
キーワード: 合成オルガネラ, ペプチドコアセルベート, 細胞内送達, タンパク質分解, 細胞工学