Clear Sky Science · ja
NatAはリボソームのポリペプチドトンネル出口で多因子複合体を形成する
誕生するタンパク質を細胞がどう微調整するか
細胞は毎秒何千もの新しいタンパク質をリボソームという小さな機械で合成しています。新しいポリペプチド鎖が現れると、それは切断され、タグ付けされ、正しく折りたたまれなければならず、そうでないと機能不全を起こし疾患に寄与することがあります。本研究は主要なタグ付けシステムの一つであるN末端アセチル化に注目し、中心的な酵素複合体NatAが新生タンパク質がリボソームを出るその場で複数のパートナーとどのように協働するかを示します。この協調の理解は、細胞がタンパク質生産ラインを円滑に保つ仕組みを説明する助けになります。
重要な小さな化学的タグ
ほとんどのタンパク質は最初に同じアミノ酸、メチオニンで始まります。しばしばこの初発メチオニンは除去され、アセチル基という小さな化学タグに置き換えられます。タンパク質の先端(N末端)に付加されるこのタグは、タンパク質の寿命、細胞内局在、機能に影響を与えることがあります。リボソームの出口では、この最初の仕上げを担う酵素が主に二種類配置しています。出発メチオニンを切断するメチオニンアミノペプチダーゼ(MAP)と、アセチル基を付加するN末端アセチルトランスフェラーゼ(NAT)です。NATの中でもNatAはヒト細胞で働き手であり、全タンパク質の約40%を修飾する可能性があります。多数のタンパク質が同時に作られるため、切断とタグ付けが迅速かつ適切な順序で起こるよう、細胞はこれら酵素を組織化する必要があります。
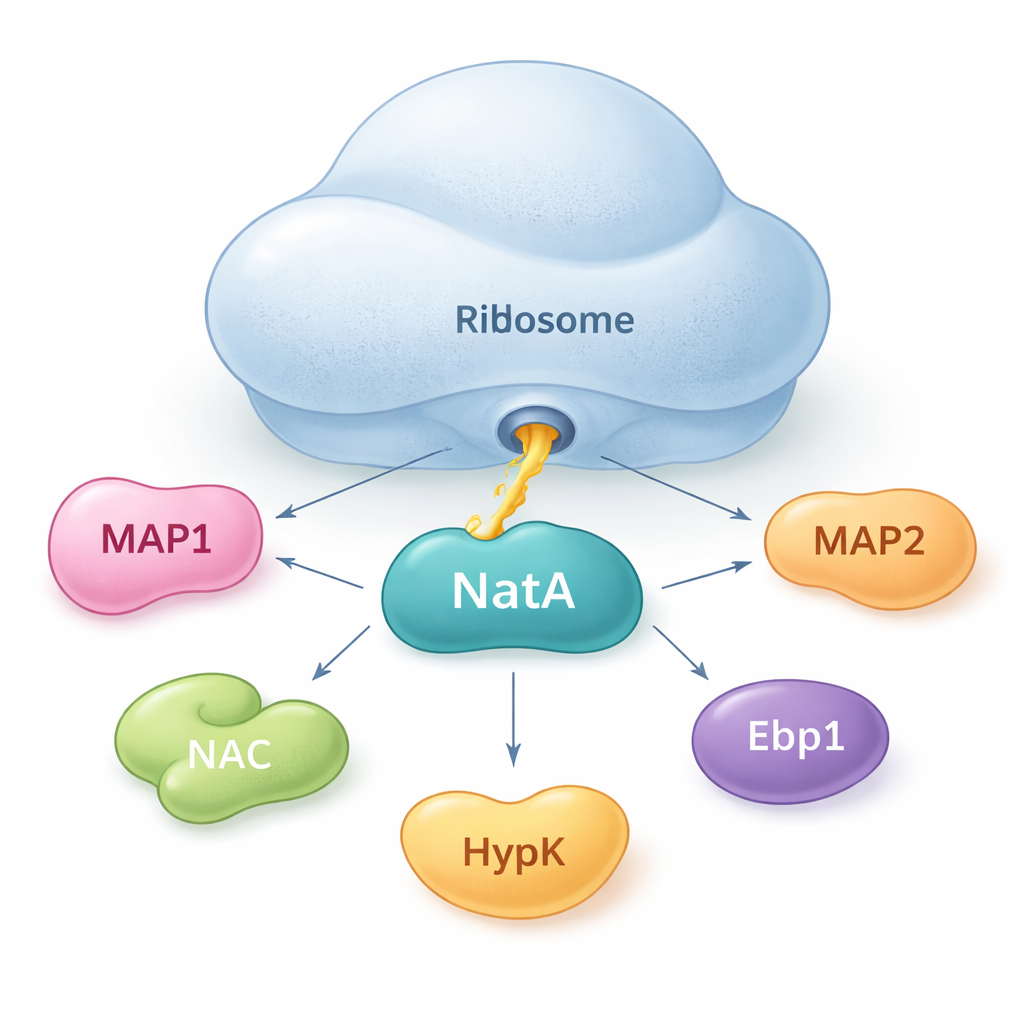
タンパク質補助因子の集まるハブとしてのNatA
著者らはNatAが単独で作用しないことを示しています。むしろNatAはハブのように振る舞い、リボソーム上でもオフでも複数の補助タンパク質を引き寄せます。溶液中での高感度な結合測定により、NatAはリボソームがなくてもMAP1、新生ポリペプチド結合複合体(NAC)、制御タンパク質HypK、もう一つの酵素Naa50と強固な複合体を形成できることが見出されました。NACはNatAとMAP1を橋渡しして、切断とタグ付けの両工程を単一のアセンブリで連結させることができます。一方で、通常NatAの活性を抑えるHypKはNACの結合を妨げることがあり、これは細胞が必要に応じてNatAをより活性化されたNAC連結状態と抑制されたHypK結合状態の間で切り替え得ることを示唆します。
トンネル出口のすぐそばにもう一つのドッキング位置
クライオ電子顕微鏡法という大型分子をほぼ原子レベルで可視化する手法を用いて、研究者らはNatAがリボソームに二つの異なる位置で結合できることを発見しました。一つは既に知られていたややトンネル出口から離れた位置です。新たに見つかった「近接(proximal)」サイトはNatAの触媒コアを成長するポリペプチド鎖の出現点に非常に近づけ、修飾されるまで鎖が移動しなければならない距離を短縮します。興味深いことに、両方の位置が同時に占有されうるため、同一リボソーム上に二つのNatA複合体が存在することができます。より遠位のコピーは足場やアンカーとして機能し、近接のコピーは新しいタンパク質にタグを付けるのに最適な位置にあります。二つのNatA分子は互いに接触しており、NatAが自身の複製体を多酵素チームとして協調させ得ることも示唆されます。
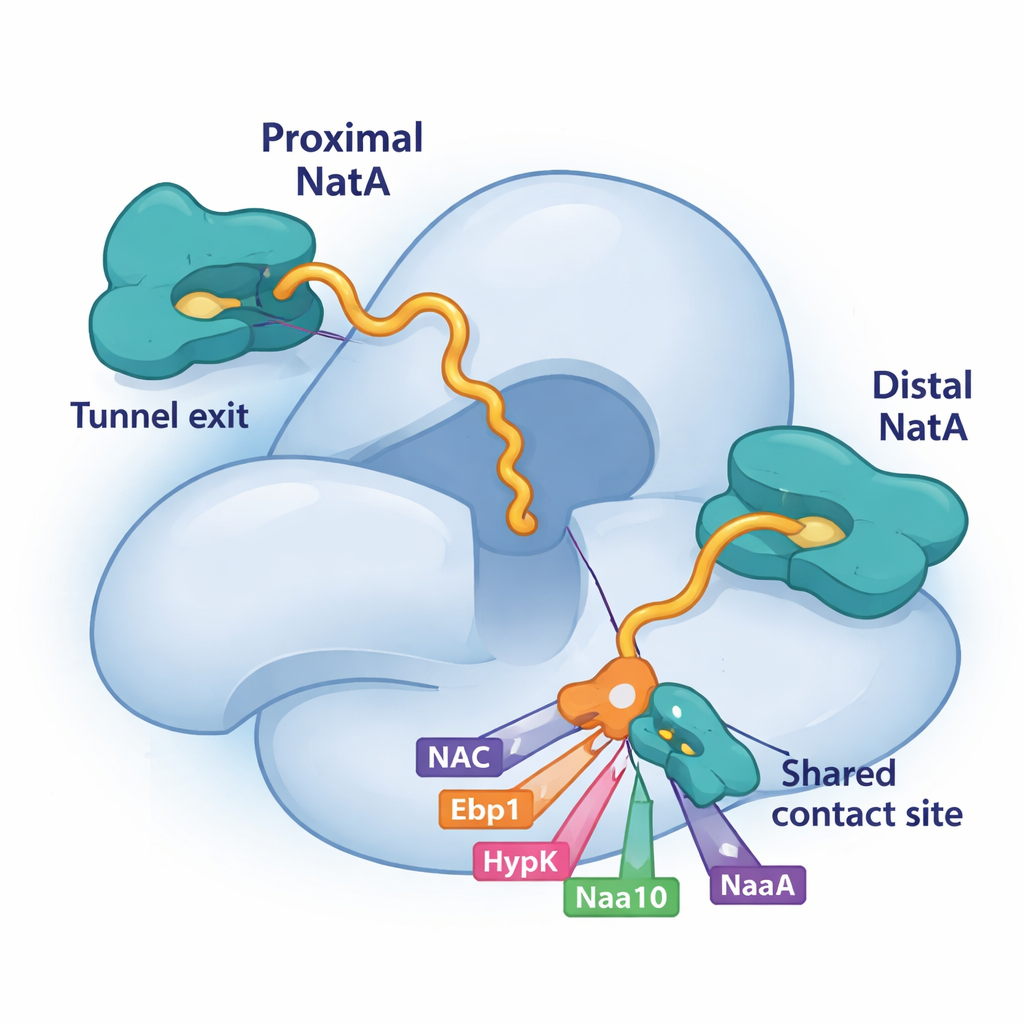
NatA上の共有ランディングパッドを巡る競合
このパズルの重要な部分は、大きなNatAサブユニットであるNaa15上の小さな溝です。本研究は、四つの異なるリボソーム関連因子—NAC、HypK、Ebp1、さらにはNatA自身の触媒サブユニットNaa10の末端断片—が短いヘリックスを使ってまさに同じNaa15のパッチに取り付くことを示します。これらは共通のランディングパッドに依存するため、互いにアクセスを競わなければなりません。HypKがその部位を占めると、NatAの活性を抑えるだけでなく、NatAがNACと結合したりNatA–NatA二量体を形成したりするのも妨げます。他方でNAC、擬似酵素であるEbp1、あるいは近接するNaa10がそこに結合すると、NatAの位置やリボソーム上での連結を再構築できます。この競合的結合は、細胞がある瞬間にどのパートナーがNatAの周りに組み立てられるかを柔軟に選ぶ手段を提供します。
交通整理者としての擬似酵素
タンパク質Ebp1は特に興味深い存在です。それはメチオニンを除去する酵素に似ているものの触媒活性を欠く「擬似酵素」です。これまでの研究でEbp1はトンネル出口付近のリボソーム上に位置し長いRNA断片を押さえ込むことが示されていました。本研究では、NatAがリボソームに加わるとEbp1は位置を変え、RNAの押さえを解放して代わりに自身のヘリックスを用いてNACやHypKが使うのと同じNaa15上の結合部位を占めることが分かりました。この配置換えは、Ebp1が実際の化学反応を行う代わりに、プレースホルダーやオーガナイザーとして振る舞い、局所的なRNA環境を形づくり、その後MAPやNatAのような活性酵素に制御を引き渡すことができることを示唆します。
なぜこの分子の群衆制御が重要なのか
ヘリックスや結合部位の詳細は非専門家には抽象的に聞こえるかもしれませんが、伝えたい要点は明快です。細胞はタンパク質が生まれるその場で高度に振付けられた多段階の品質管理システムを運用しています。NatAはこのシステムの中心に位置し、どの因子が重要なドッキングパッチへのアクセス権を獲得するか、そしてNatAがどのリボソーム部位を占めるかに応じて、異なるパートナーを招き入れたり放したりできます。この柔軟なネットワークは、何千もの異なるタンパク質に対して切断とアセチル化が適切なタイミングと順序で行われることを助けます。N末端処理の誤りは発達障害、神経変性、がんと関連するため、NatAとそのパートナーの組み立て方を明らかにすることは、初期タンパク質処理の制御がどのようになされているか、そしてそれが乱れたときにどう標的化できるかという研究者にとっての青写真を提供します。
引用: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
キーワード: タンパク質品質管理, N末端アセチル化, リボソームトンネル出口, NatA複合体, 翻訳共役修飾