Clear Sky Science · ja
植物フコシルトランスフェラーゼFUT11は受容体糖を歪め、一過性のオキソカルベニウム様中間体を介する機構で触媒する
植物がタンパク質上の糖鎖を微調整する仕組み
我々の細胞や植物のタンパク質はしばしば複雑な糖鎖で飾られ、折りたたみ、安定性、結合相手の選択などを導くバーコードのように機能します。本研究は、これらの鎖に微小な糖であるフコースを付加する植物酵素FUT11に焦点を当てています。FUT11が原子レベルでどのように働くかを解き明かすことで、著者らは驚くべきトリックを明らかにします:酵素は反応相手の糖を一時的に変形させ、困難な化学段階を進めるのです。この過程を理解することは基礎生物学にとどまらず、人体で望ましくない免疫反応を引き起こさない植物由来医薬品の設計にも重要です。
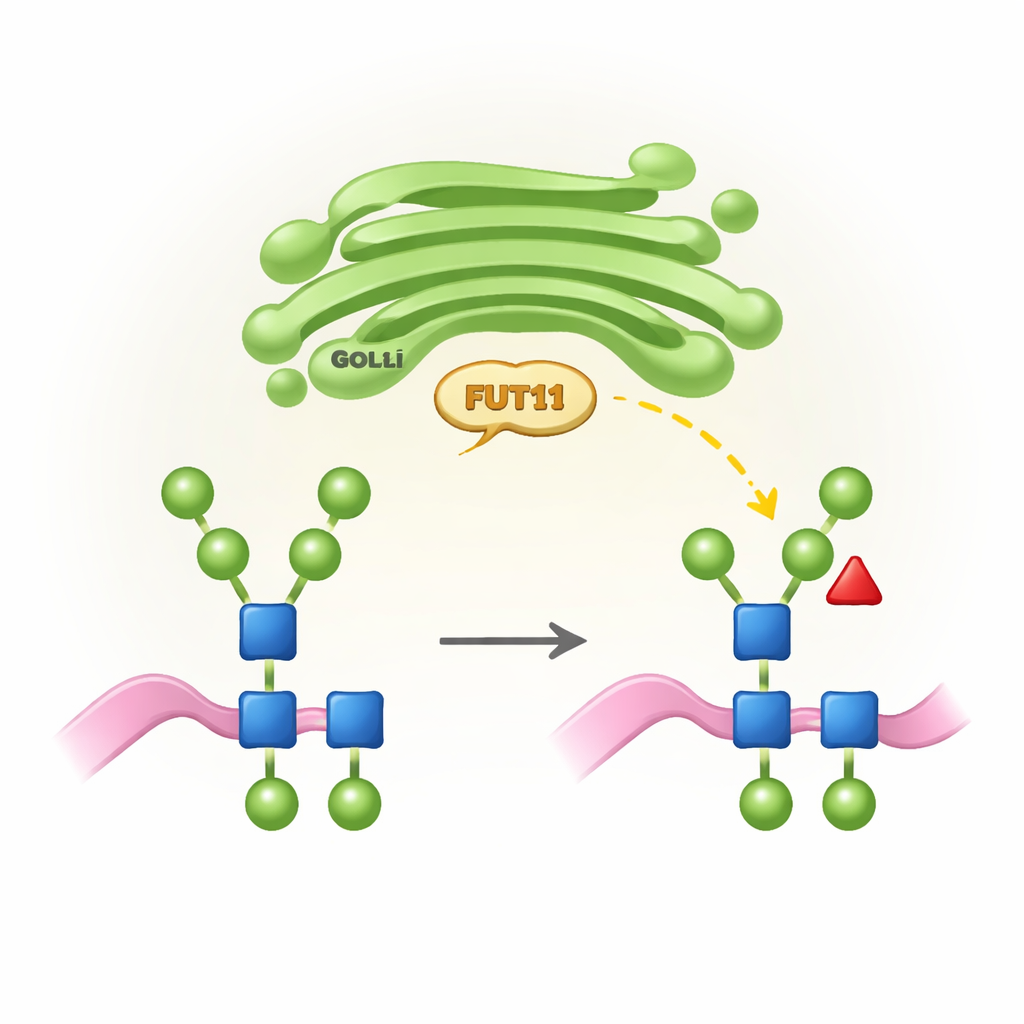
植物特有の糖のタグとその重要性
すべての高等生物はN-グリコシレーションと呼ばれる過程で特定の部位に糖鎖(N-グリカン)を付加します。動物では、これらの鎖はゴルジ体でリモデルされ、しばしばシアル酸で終わり、核となる位置に特定のコアフコースを持つ精巧な構造になります。一方、植物は異なる「設計規則」に従い、通常はシアル酸を欠き、別の位置(いわゆるβ1,3)にコアフコースを持ち、さらに余分なキシロースを付加します。これらの植物特有の特徴は正常な成長や生殖に不可欠ですが、人の免疫系には非自己として認識されることがあります。FUT11はこのコアフコースを導入する主要な植物酵素の一つであり、その活性は植物の発生と、植物由来治療タンパク質が人体でどのように扱われるかの両方を形作ります。
複雑な糖分岐のどこでFUT11が働けるかをマッピングする
FUT11が何を認識するかを理解するため、研究者らは144種類の異なるN-グリカン構造を並べたマイクロアレイ上で酵素を試験しました。FUT11は糖の木のある枝――いわゆるβ1,3腕――に対してかなり選択的であり、反応が進行するためにはその枝が特定の構成要素(末端のN-アセチルグルコサミン、GlcNAc)を持っている必要があることが分かりました。同時に、FUT11は他の修飾には寛容で、中央のマンノースが植物特有のキシロースを持っていても、またコアの哺乳類位置に既に別のフコースが付加されていても作用します。反対側の枝(β1,6)は主に溶媒に露出しており酵素との接触が弱いため、FUT11がそちらの多様な修飾に対処できる理由が説明されます。これらの結合特性は、なぜ植物が特徴的なN-グリカンセットを作るのかを説明し、FUT11がバイオテクノロジーでの利用や回避の対象となりうることを示します。
糖を掴み位置決めする独特の構造設計
X線結晶構造解析により、研究チームはGDP-フコースを供与体とするFUT11とN-グリカン受容体との三次元構造を解決しました。酵素は二葉式の「GT-B」アーキテクチャを持ち、一方の葉がGDP-フコースを支え、もう一方の受容体葉は異常に精巧で植物特有のN末端サブドメインを含み、N-グリカンを包み込みます。この余分なサブドメインはジスルフィド結合で酵素本体に繋がり、グリカンの中央部を固定して反応性のGlcNAc単位を供与体に向けて提示するのに寄与します。重要なアミノ酸を変異させた実験はそれらの役割を裏付け、単一のグルタミン酸(Glu158)を変えると活性が消失し、近傍の二つの残基を変えるとヒト細胞系でのフコシル化が大幅に弱まることが示されました。これらの結果は構造のスナップショットを細胞内での機能に結びつけ、どの部分が結合と触媒に不可欠かを正確に示します。
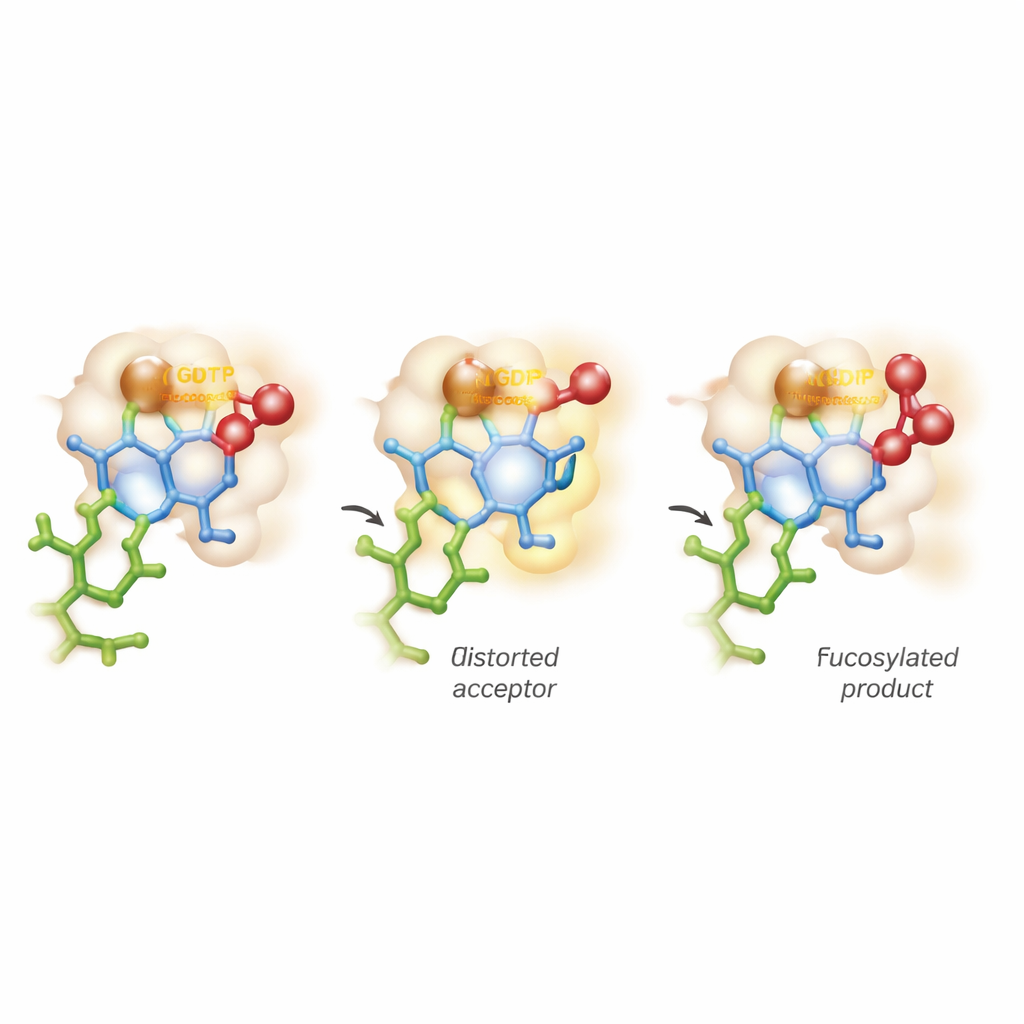
糖を曲げ、二つの反応経路の狭間を歩む
最も注目すべき知見は、量子化学と分子動力学を組み合わせた高度なコンピュータシミュレーションから得られました。従来の考え方では受容体糖は安定な椅子型のままで酵素は単に供与体を活性化すると想定されてきましたが、ここではFUT11はより能動的に振る舞います:Glu158による相互作用が内側のGlcNAc環を一時的に不快なひずんだ撓み形に変形させます。このゆがんだ姿勢では、重要なヒドロキシル基がフコース供与体を攻撃するのに理想的な位置に整列します。計算は、GDPとの化学結合が切れるにつれて糖上に短命で正に帯電した「オキソカルベニウム様」状態が現れ、その後に受容体への新しい結合が完全に形成されることを明らかにしました。これは反応が教科書的なSN1またはSN2のいずれかにきれいに当てはまるのではなく、非同期的でほぼ段階的な連続体に沿って進行することを意味します。
隠れた柔軟性と進化の残響
FUT11を関連するヒト酵素FUT9と比較すると、植物酵素は弱いながらも別種の糖モチーフ(LacNAc)を修飾してLewis Xとして知られる構造を作ることができることが分かりました。この副次的活性は植物で通常見られないLewis Xに関して生物学的には重要でない可能性が高いですが、類似したタンパク質骨格が進化の過程で異なる糖環境に合わせて再利用されうることを示しています。本研究はFUT11とその同族体がN-グリカンを認識するためのモジュラーな枠組みを共有し、微妙な調整が植物のコアと動物のアンテナ部分との特異性を変えることを示唆します。
この糖の曲げトリックが科学と医療で重要な理由
総じて、本研究はFUT11が単に二つの糖パートナーを近づけるだけでなく、受容体糖を反応性の姿勢に積極的に曲げ、一時的で電荷を帯びた中間体を経由して化学を導くことを示しています。一般向けに言えば、タンパク質上の糖は剛直なドッキングサイトではなく、酵素が必要に応じて形作る柔軟な参加者であるということです。この「立体配座触媒」の新しい見方は、酵素がどのように速度と選択性を両立するかを説明する助けとなり、糖鎖化経路の再設計の設計図を提供します。実用的には、FUT11が植物のN-グリカンをどのように認識・修飾するかを正確に知ることで、作物や植物由来生産系を設計してヒトの治療における免疫を引き起こす糖パターンを最小化したり、特性を持つデザイナー糖タンパク質を作成したりする手がかりになります。
引用: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
キーワード: 植物の糖鎖化, フコシルトランスフェラーゼFUT11, N-グリカン, 酵素機構, グリコエンジニアリング