Clear Sky Science · ja
単一細胞のエクソン欠失プロファイリングが遺伝子発現と細胞状態ダイナミクスを形作るスプライシング事象を明らかにする
RNAの小さな修飾が細胞の振る舞いを変える仕組み
細胞は常にRNAの指示を読み取りスプライスして、どのタンパク質を作るか、ストレスにどう応答するか、増殖や分裂をどう行うかを決めています。本研究は、RNAメッセージのごく小さな断片――エクソンと呼ばれる単一の区画――を変えるだけで、遺伝子活性が大きく再編され、細胞が細胞周期を進む様子まで変化することを示しています。本研究は多数のこうした微細なRNAの選択を細胞ごとに一度にスキャンできる強力な手法を導入しており、疾患理解や創薬標的の探索に新たな道を開きます。
遺伝情報から特定の「語」を切り取る
遺伝子は長いDNAの配列として書かれていますが、細胞はそれを一気に読み通すわけではありません。代わりにエクソンと呼ばれる小さなブロックを切り出して貼り合わせ、RNAメッセージを作ります。どのエクソンを残すかによって、同じ遺伝子から複数のタンパク質バリエーションが作られるため、まるで同じ生フィルムから異なる編集版を作るようなものです。がんや自閉症を含む多くの疾患がこの過程の異常に関連しますが、ほとんどのエクソン選択が実際に何をするかはまだ分かっていません。著者らはこれを解明するために、多数の遺伝子から特定のエクソンを除去し、何千もの個々の細胞を同時に観察してその編集が細胞の内部配線にどう影響するかを見る大規模なシステムを構築しました。
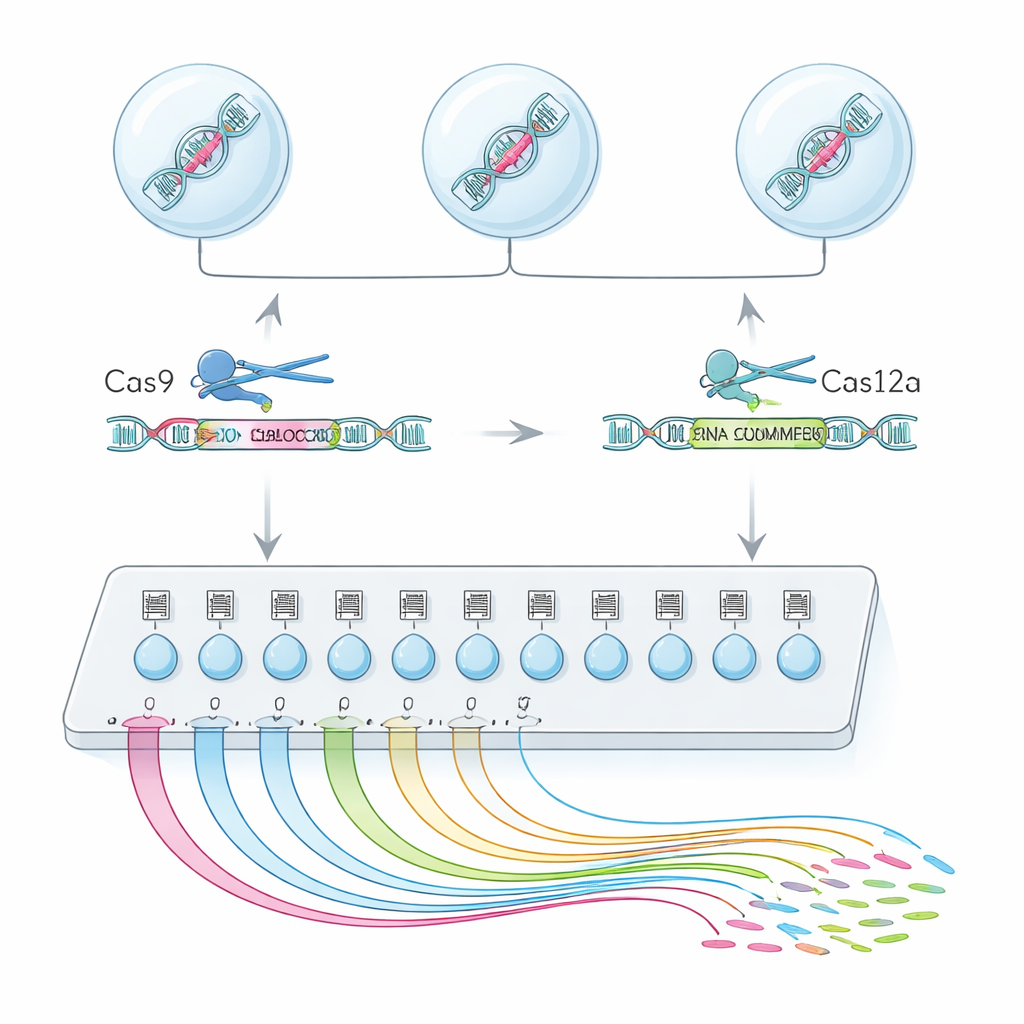
エクソン機能を探す単一細胞「検索エンジン」
これを実現するために、チームは2種類のゲノム編集酵素、Cas9とCas12aを組み合わせたハイブリッドプラットフォームCHyMErAを作りました。各酵素は短いRNAの「住所」によってDNAへ誘導されます。2つの酵素を選んだエクソンの直前と直後に切断させることで、その区間だけをきれいに削除し、残りの遺伝子は保ったままにできます。新しい手法scCHyMErA-Seqはこの精密な切断を単一細胞RNAシーケンシング技術に結びつけます。各細胞のRNAはバーコードおよびどのエクソンが除去されたかを指定するガイドRNAとともにドロップレット内で捕捉されます。シーケンシングにより、数万の細胞について各細胞が受けた編集と、その細胞がオンまたはオフにした遺伝子の詳細なパターンの両方が明らかになります。
両方の“刃”を可視化するための技術改良
主要な課題は、同一の単一細胞実験内でCas9ガイドとともにCas12aガイドを確実に検出することでした。初期の設計ではCas12aガイドRNAが捕捉されなかったり、編集効率が損なわれたりしました。研究者らはこれを、転写を早期に止めてしまう配列を除去するためのCas12aハンドル配列の慎重な再設計と、小さな安定化RNAエレメントの追加、さらにターゲット増幅ステップの導入で解決しました。これらの調整により、約90%の細胞で両方のガイドを検出できるようになり、強いエクソン欠失も維持されました。最適化されたこのセットアップで、著者らはヒト細胞の161遺伝子にわたる224の選択的エクソンをスクリーニングし、20万を超える高品質の単一細胞をプロファイリングしました。
遺伝子プログラムと細胞周期を制御するエクソンの発見
編集細胞と対照を比較したところ、試験したエクソンのほぼ半数が数百の他の遺伝子に実質的な変化を引き起こしていました。RNA処理や転写に関与する遺伝子由来のエクソンは類似した発現フィンガープリントを示して群を成し、リボソーム形成やRNA分解など共通の生物学的経路が明らかになりました。いくつかの例では、単一のエクソンを除去することで明確で解釈可能な影響が現れました。TAF5やLSM11のエクソンを欠失させるとヒストンRNAの正しい処理が乱れ、ポリアデニル化されたヒストンメッセージが異常に蓄積しました。データセットはまた、多数のエクソンを同定しており、その喪失が細胞周期の異なる段階に存在する細胞の割合に変化をもたらし、特定のスプライシング事象が細胞が停止するかDNAを複製するか、あるいは分裂の準備をするかといった決定に直接結びつくことを示しました。
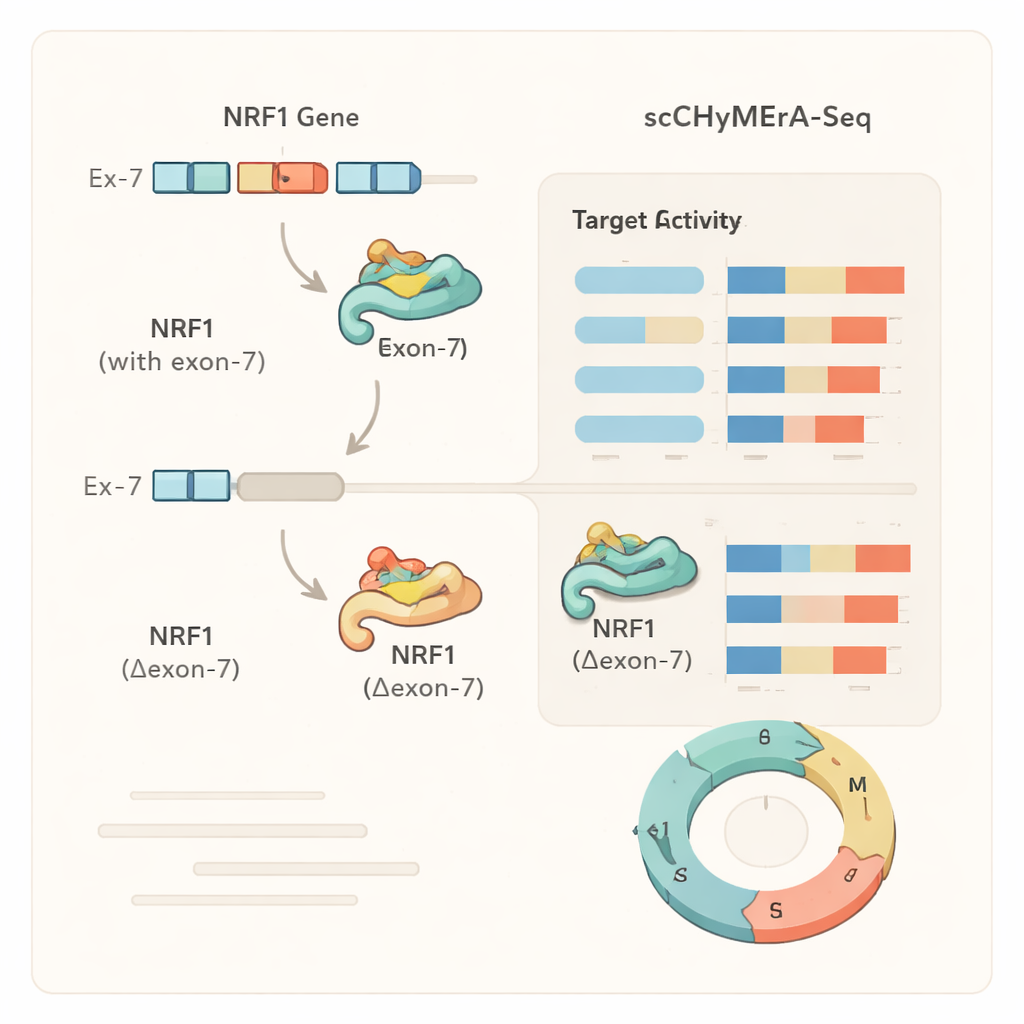
ケーススタディ:主要な調節因子を調整する一つのエクソン
顕著な例の一つが転写因子NRF1のエクソン7でした。NRF1は細胞のエネルギー産生に関与する多くの遺伝子を制御します。このエクソンはNRF1のDNA結合領域と部分的に重なっています。エクソン7を欠失させると、NRF1に制御される数百の遺伝子の活性が変化し、短くなったNRF1タンパク質はゲノム上の標的プロモーターへの結合能が大幅に低下することが詳細な実験で示されました。著者らはさらに、SRSF3という特定のスプライシング調節因子がこのエクソンの包含を促進することを同定し、スプライシング因子からNRF1のエクソン選択を経て細胞の遺伝子プログラムや代謝に広範な変化をもたらす一連の流れを明らかにしました。同様の解析は、ある遺伝子ではエクソン欠失が完全な遺伝子ノックアウトと類似した効果を示す一方、別の遺伝子ではより微調整された状態依存的な変化を生じさせることを示し、選択的エクソンが単にオン/オフを切り替えるのではなくタンパク質の振る舞いを繊細に調節しうることを示唆しました。
健康と将来の治療への意義
専門外の読者にとって重要なメッセージは、細胞がごく短いRNAの区間の包含やスキップに依存して遺伝子の働きを微調整しており、こうした細かな調整が細胞の分裂様式やストレス応答など大きな性質を変えうる、という点です。scCHyMErA-Seqプラットフォームはこれらのスプライス選択をハイスループットに検査する実験系として機能し、どのエクソンが実際に機能的影響を持つか、そしてそれらが細胞状態をどう再構築するかを特定します。多くのがんや神経疾患が誤ったスプライシングや変化した転写因子に関わることを考えると、このアプローチは将来の医薬品やRNA療法で標的化すべきスプライスバリアントの優先順位付けに寄与し、遺伝情報の小さな編集が細胞の振る舞いにどのように波及するかを理解するためのロードマップを提供する可能性があります。
引用: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
キーワード: 選択的スプライシング, 単一細胞RNAシーケンシング, CRISPRスクリーニング, 遺伝子調節, 細胞周期