Clear Sky Science · ja
ナノ小胞標的抗がん用途のためのグランザイムB模倣ナノザイム
体内のがん殺傷者を再考する
私たちの免疫系にはがん細胞を捜索・殺傷する専門の細胞が存在しますが、多くの固形腫瘍では浸潤が困難だったり、すぐに疲弊したり、誤った標的を攻撃したりします。本研究は、免疫系の最も強力な武器の一つを模倣し、それを直接腫瘍細胞に届ける完全人工のナノスケールシステムを記述しています。この成果が重要なのは、生きた免疫細胞のように振る舞うが、壊れやすいヒト細胞ではなく、安定で制御可能な材料から作られるがん治療の道を示している点です。
自然の暗殺者を設計図にする
サイトトキシックT細胞は白血球の一種で、グランザイムBという酵素を用いて危険な細胞を殺します。標的を認識すると細胞膜に小さな穴を開けてグランザイムBを注入し、細胞内の自殺プログラムを起動します。この戦略はCAR-T細胞などの現代療法の基盤であり、一部の血液がんを治癒することがあります。しかし、固形腫瘍ではCAR-T細胞が腫瘍領域すべてに到達できなかったり、疲弊したり、正常組織を誤って攻撃したりして失敗することがしばしばあります。著者らは、生きたT細胞に依存せず、グランザイムBの主要な機能――細胞の自滅機構を作動させること――を再現する非生物のナノスケール装置を構築できるかを問いかけました。
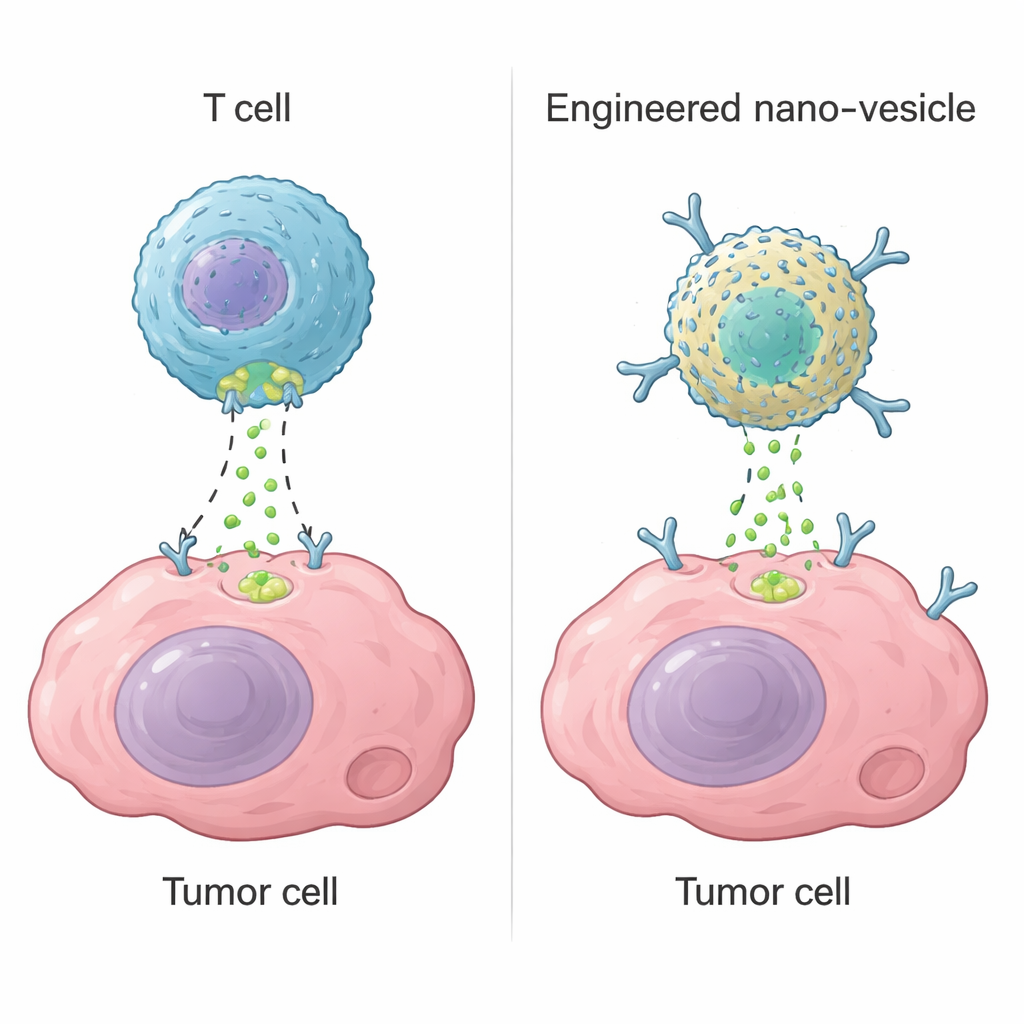
小さな人工酵素の設計
研究チームは空洞のナノケージを形成し大量生産が容易な天然タンパク質フェリチンを出発点としました。ヒトフェリチンにパラジウムイオンを結合させることで、酵素様の挙動を示す「ナノザイム」を作製しました。詳細な構造解析により、二つのパラジウム原子がタンパク質表面の特定ポケットに収まり、硫黄・窒素含有アミノ酸と水分子によって固定されていることが明らかになりました。この二核金属中心は、重要な標的であるカスパーゼ-3に対してグランザイムBが認識するのと同じ短い配列を認識する人工的な切断部位として働きます。in vitroの試験で、このナノザイムはカスパーゼ-3を正しい位置で効率的に切断して活性化し、類縁タンパク質は無視しました。人工酵素は天然のグランザイムBよりやや効率は劣りましたが、温度や酸性度の広い範囲で著しく安定でした。
ナノザイムを腫瘍細胞内に密輸する
グランザイムBのような酵素は、腫瘍細胞の内部に到達して初めて機能します。これを達成するために、研究者らはパラジウム–フェリチン・ナノザイムを脂質ナノ小胞――脂質分子でできた小さく柔らかい泡――の内側に封入しました。さらにこれらの小胞の表面を、乳がんや膀胱がん細胞で過剰発現することの多いタンパク質HER2を認識する抗体の断片でコーティングしました。こうしたカモフラージュされた小胞がHER2に富む細胞に遭遇すると、強く結合して細胞膜と融合し、小胞が細胞のリサイクリングコンパートメントに捕獲・分解されるのを避けて、ナノザイム荷物を細胞質内へ直接滑り込ませます。顕微鏡観察では、小胞が細胞表面にとどまりつつナノザイムが内部へ拡散していく様子が示され、内部からの制御された自己破壊が可能な状況が整いました。
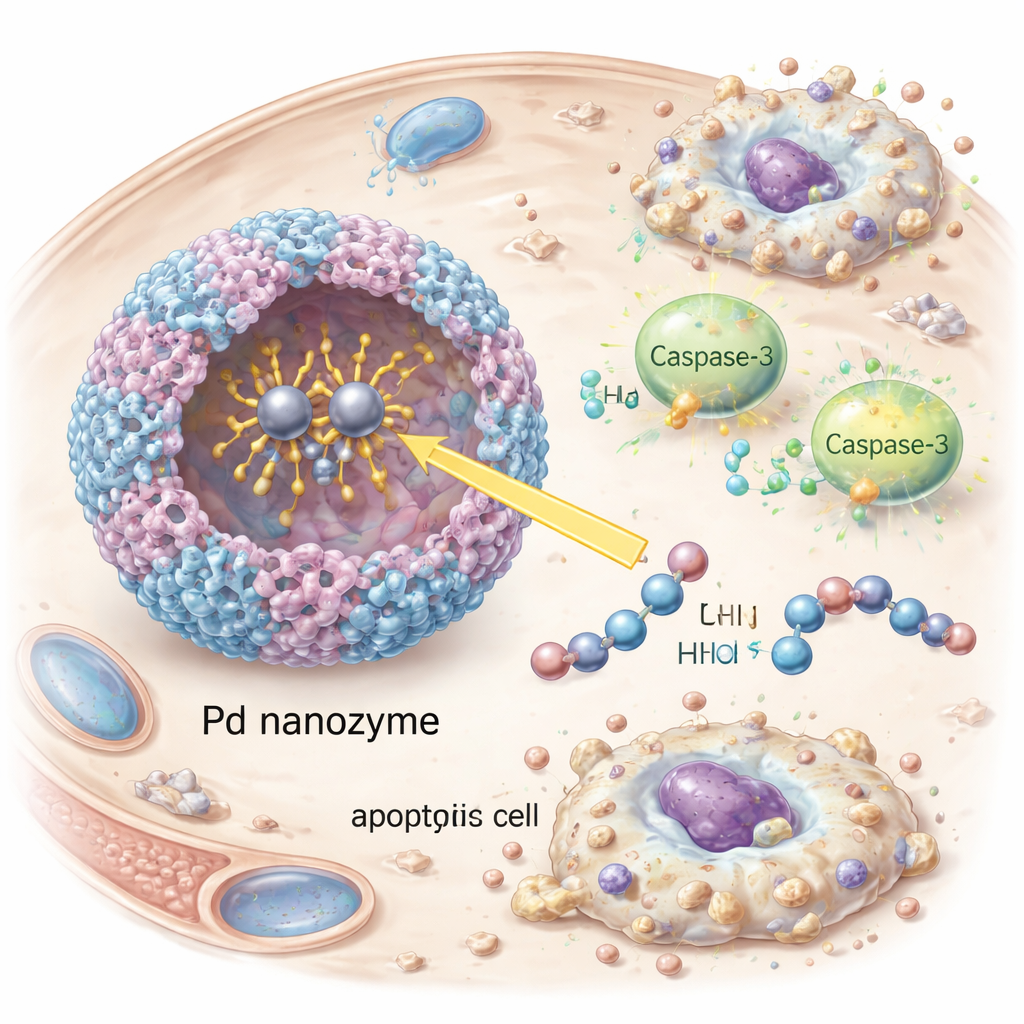
精密にがん細胞の自殺を誘導する
がん細胞内に入ると、ナノザイムはプログラム化細胞死の中心的実行因子であるカスパーゼ-3を作動させました。研究者らは活性化されたカスパーゼ-3とその下流標的であるPARPの出現、ならびにHE R2陽性腫瘍細胞の培養における縮小や断片化といった明確なアポトーシスの徴候を観察しました。RNA干渉によってカスパーゼ-3をサイレンシングすると細胞死が劇的に減少し、効果が非特異的な損傷ではなくこの経路に依存していることが確認されました。HER2陽性腫瘍を移植したマウスでは、抗体で飾られた小胞が血中での滞留が長く、腫瘍への蓄積が強く、標的抗体またはナノザイムのどちらかを欠く小胞よりも腫瘍成長をより効果的に遅延させました。重要なことに、治療を受けた動物では体重減少や血液異常、主要臓器の組織損傷は明らかに見られず、初期試験では良好な安全性プロファイルが示唆されました。
将来のがん医療にとっての意味
専門外の読者にとっての中心メッセージは、研究者らが免疫系のがん殺傷機構の主要素のように振る舞う小さな非生物デバイスを構築したということです。生きたT細胞を改変する代わりに、同じ自殺スイッチを腫瘍細胞内で作動させる安定した人工ナノ酵素を設計し、特定のがんに集まるスマートな輸送殻で包みました。ヒトでの使用に至るまでには多くの課題が残りますが、このアプローチは柔軟なプラットフォームを提供します。理論的には抗体コーティングを交換して別の腫瘍マーカーを狙ったり、人工酵素をさらに最適化したりすることが可能です。本研究は、生きた免疫細胞の代わりに精密に設計されたナノ材料を用いて固形腫瘍を追跡・破壊する細胞非依存型免疫療法への有望な道筋を示しています。
引用: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
キーワード: がんナノメディシン, 免疫療法, グランザイムB, ナノザイム, HER2陽性腫瘍