Clear Sky Science · ja
ボロネートで保護されたジヒドロテトラジンによって可能になった、生体内での活性酸素種(ROS)活性化バイオオーソゴナル化学
細胞ストレスを正確なスイッチに変える
がんから心疾患に至る多くの病気では、細胞が酸化ストレスを受け、水素過酸化物などの活性酸素種を大量に産生します。本研究は、化学者がそのストレス自体を内蔵のスイッチとして利用し、強力な治療を必要な場所だけでオンにする方法を示しています。ストレスのかかった環境でのみ反応する薬剤断片を設計することで、研究者らは正常組織を守りながら腫瘍細胞を死滅させたり、有害なタンパク質を除去したりすることを目指しています。
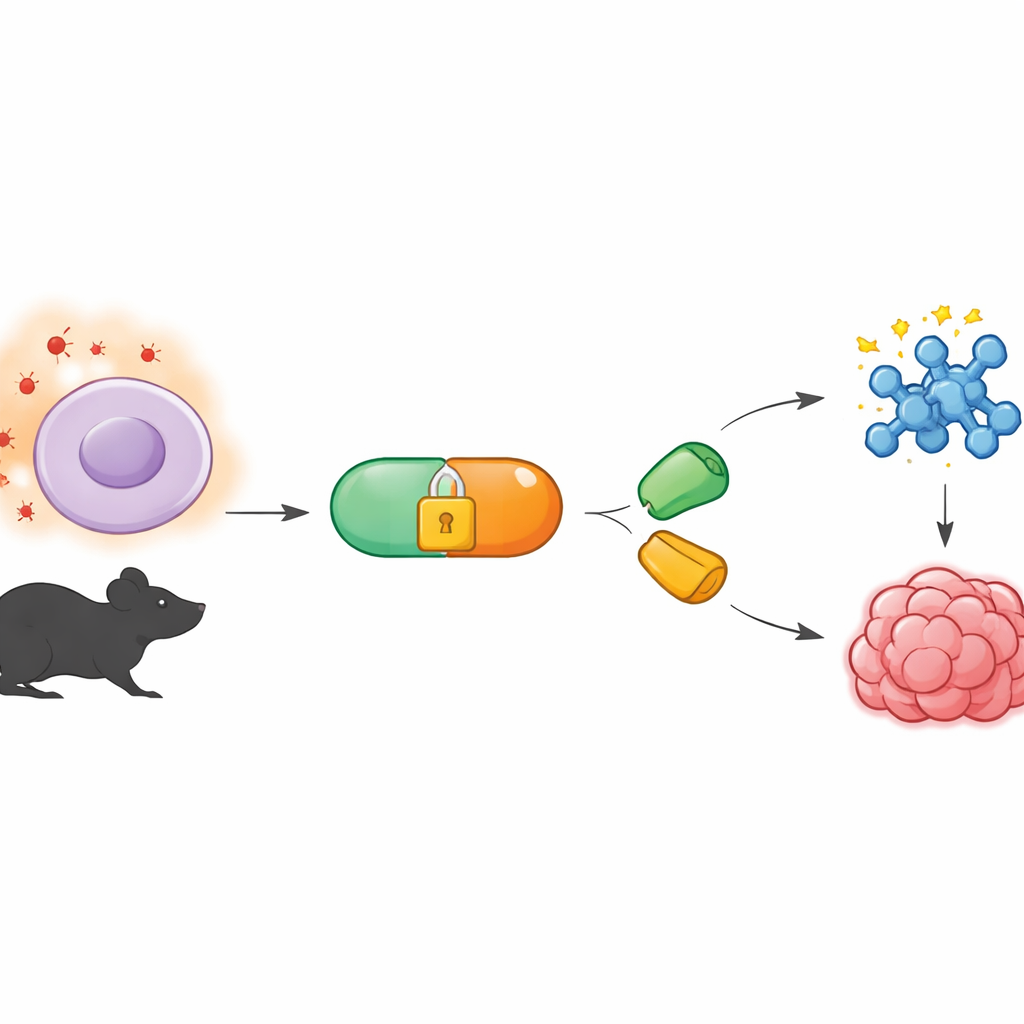
目立たずに働く化学ツール
この研究は、生体内で通常の生理を乱すことなく進行できる反応を開発する分野、バイオオーソゴナル化学に基づいています。一般に使われる手法の一つは、細胞内という混雑した環境でもパズルのピースのように互いに結合する特別な分子対を利用するものです。一方はテトラジンと呼ばれ、対応する“環”を持つジエノフィルと非常に速く反応します。これまで多くの反応は光照射や酵素添加で制御されてきましたが、著者らは体内の化学信号、具体的には腫瘍やその他の病変組織で見られる異常に高い活性酸素種のレベルに応答するシステムを目指しました。
ROSに感受性を持たせた化学トリガーの構築
そのためにチームはBTzと呼ぶテトラジン前駆体を作成しました。これは化学的に“ケージ”された形で、正常組織では不活性のまま維持されます。ケージは還元型テトラジンに結合したボロネート基から成り、水素過酸化物が乏しい条件ではBTzは水中や細胞培養でも長時間安定です。しかし、腫瘍で測定されるような濃度の水素過酸化物が豊富に存在すると、ボロネート基が酸化され自己分解の連鎖を経て崩壊し、活性なテトラジンが露出します。試験管内実験では水素過酸化物濃度を段階的に上げると生成される活性テトラジン量も一致して増加し、この反応が選択的でかつ用量依存的であることが確かめられました。
細胞ストレスを利用してがん駆動性タンパク質を破壊する
研究者らはまずこのスイッチを近年の薬学戦略である標的タンパク質分解の制御に用いました。BTzをサリドマイド誘導体であるサリドマイド(著者はそれをチアロリドームに相当する小分子)に結合させ、タンパク質を除去するための目印を付ける酵素複合体を呼び寄せられるようにしました。がん細胞内では、このBTz–サリドマイドは水素過酸化物レベルが上がるまで休止状態にあり、酸化が起きるとケージが外れて活性テトラジンが生成されます。生成されたテトラジンはBRD4結合薬に結合した対応するパートナーと迅速に結合し、BRD4を細胞の分解機構へと導く大型の“キメラ”を組み立てます。肺がんおよび子宮頸がんの細胞株では、すべての構成要素が揃い水素過酸化物が存在した場合にのみBRD4量が急減し、活性酸素種を阻害すると分解が阻まれたことから、このプロセスが真にストレス依存であることが示されました。
毒性薬を必要な場所だけに届ける
次にチームは同じ化学を用いて、強力だが心毒性のある化学療法薬ドキソルビシンの精密送達システムを構築しました。ドキソルビシンを歪められた環状パートナーに結合させ、不活性なプロドラッグ状態にロックしました。このプロドラッグがBTzと出会い、水素過酸化物に富む環境で新たに生成されたテトラジンと“クリック・トゥ・リリース”反応を起こすと、結合が成立して自由なドキソルビシンが放出されます。培養皿で育てた結腸がん細胞では、この二段階システムは遊離薬とほぼ同等の細胞殺傷効果を示しましたが、水素過酸化物が存在する場合に限られ、存在しない場合は細胞は大部分守られました。単純な水素過酸化物感受性のドキソルビシンプロドラッグはこれらの試験で効果も選択性も低く、感知と放出を二つの協調した段階に分ける利点が際立ちました。
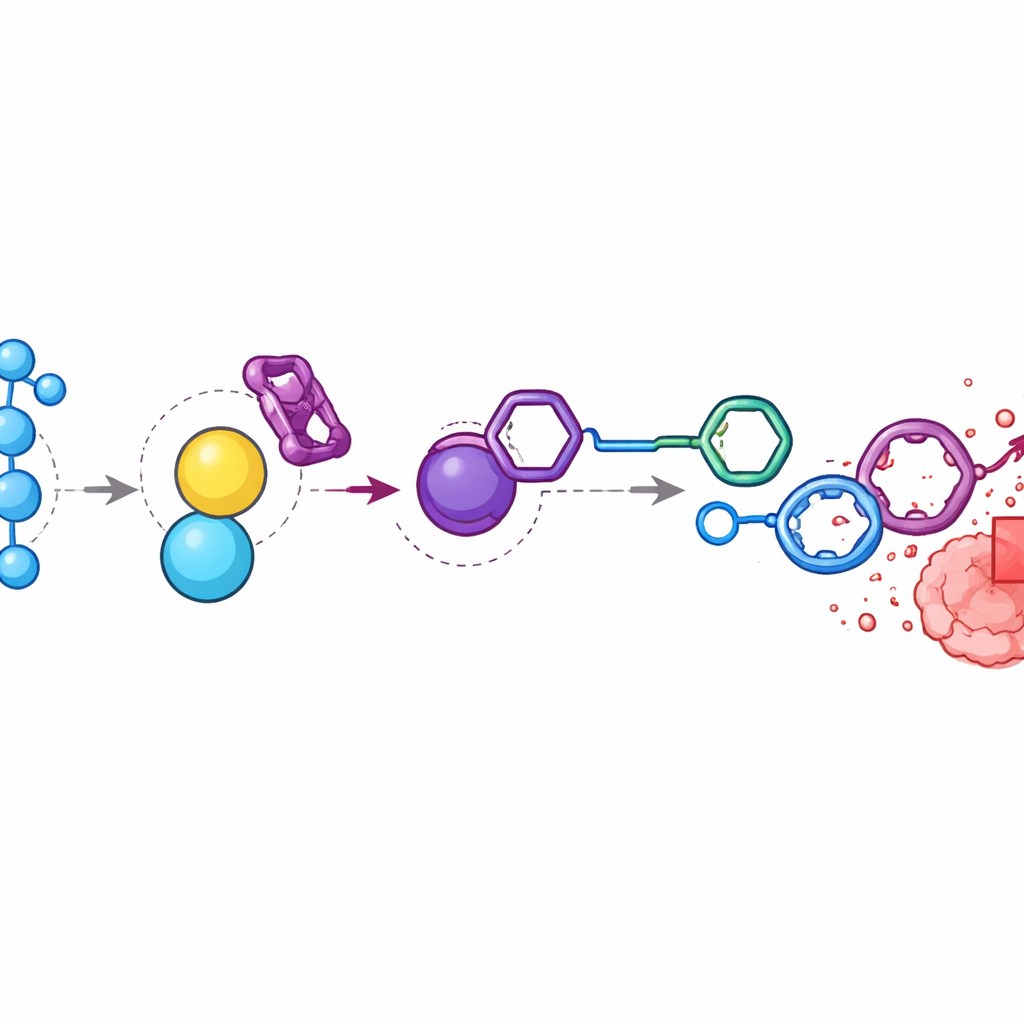
腫瘍内部に化学療法を集中させる
結腸腫瘍を有するマウスでは、腫瘍中の水素過酸化物レベルが周囲の筋肉に比べほぼ9倍高いことが分かりました。研究者らはドキソルビシンプロドラッグとBTzを時間差で注入し、両者が腫瘍付近に集積するようにしました。化学分析により、これらの成分は血流や臓器からはほとんど消失する一方で、腫瘍内部では高濃度の遊離ドキソルビシンが生成されていることが示されました。標準的なドキソルビシンを与えた動物と比べ、活性化システムで治療した群は同等かそれ以上の腫瘍縮小を示しつつ体重は安定し、高用量で見られる重篤な毒性を回避しました。カタラーゼを注入して水素過酸化物シグナルを断つと薬物放出と腫瘍選択的蓄積が大幅に低下したため、腫瘍部位の酸化ストレスが主要な駆動因子であることが確認されました。
ストレスシグナルから精密医療へ
総じて、本研究は疾患の特徴である過剰な活性酸素を生体内で強力な反応を制御する精密なスイッチに変える汎用性のある化学プラットフォームを示しています。テトラジンの反応性ハンドルを水素過酸化物に出会うまでロックしておくことで、必要な部位でのみ複雑な治療を体内で組み立てられるため、がん促進タンパク質を解体する場合でも、腫瘍内で毒性薬を解放する場合でも応用が可能です。酸化ストレスは老化、炎症、糖尿病、神経変性疾患にも関与しているため、同様のストレス応答型反応は、精度と安全性が重要な多くの疾患に応用され得るでしょう。
引用: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
キーワード: バイオオーソゴナル化学, 活性酸素種, テトラジン連結反応, 標的薬物送達, PROTAC