Clear Sky Science · ja
ゴルジイメージングと破壊のための巡回分子アセンブリ
細胞の出荷センターを戦略的標的に変える
動物細胞の内部にはゴルジ装置があり、何千ものタンパク質や脂質を仕上げ、梱包し、発送する忙しい仕分け拠点になっています。多くのがん細胞はこのハブに強く依存しており、成長シグナルを修飾したり、周囲環境を形作る因子を分泌したりします。本論文は、ゴルジに選択的に到達して迅速に可視化できる小さな設計分子を紹介し、再設計することでゴルジの機能を妨げ、特定の健康な細胞をある程度温存しながらがん細胞を機能不全に陥れる可能性を示します。
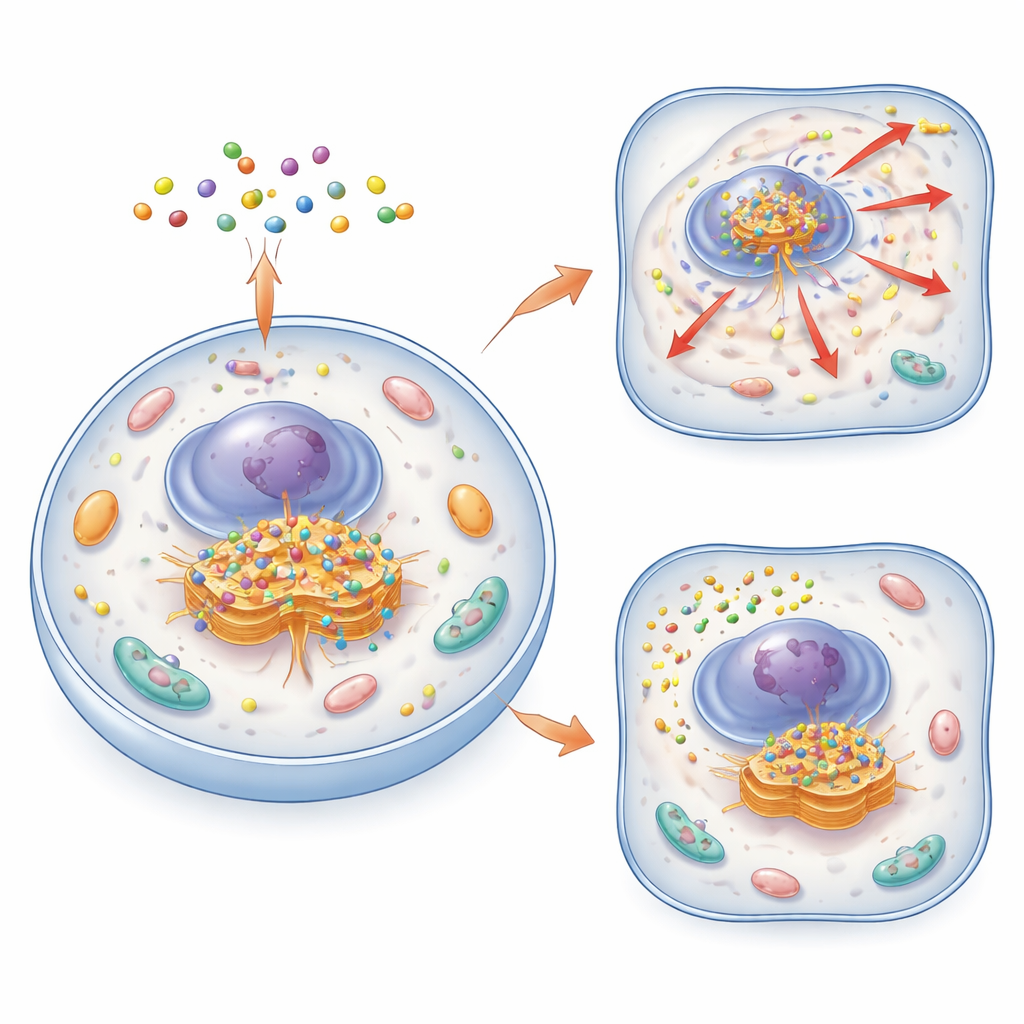
ゴルジを見つけて観察する新しい方法
著者らは巡回分子アセンブリ(cycling molecular assemblies、略してCyMA)と名付けた一群の小さく賢い分子を作り出しました。これらは細胞膜を通過でき、かつ互いに集まって小さなクラスターを作る短いペプチドから構成されています。「イメージング」版(CyMA‑i)では、ペプチドに蛍光色素が結合しており、分子が集合すると強く発光します。細胞内に入ると、酵素がCyMA前駆体から保護キャップを切り取り、反応性の手がかりを露出させます。ゴルジに常在する酵素がその手がかりに脂肪鎖を付加すると、分子はより粘着性を帯びて自己集合しやすくなり、まさにゴルジ上で集合します。このプロセスは迅速で細胞の自然な機構を利用するため、研究者は生細胞内でごく低濃度のプローブを用い、数分でゴルジの形状を描き出すことができます。
分子をゴルジに固定する無益なサイクル
CyMAは単なるラベルではなく、ゴルジで「無益なサイクル」に関与するよう設計されています。ある酵素群がペプチドに脂肪鎖を付け、別の酵素群がそれを取り除きます。脂肪鎖が付加されたり除去されたりを繰り返す間に、修飾されたペプチドはその場で組み立てたり分解したりを続けます。この絶え間ない往復により、ゴルジ膜上に固体状のコアが捕捉されつつ、個々の分子は循環を続けます。細胞はこのループを維持するために自前の脂肪酸系の材料を常に消費する必要があり、実質的にアセンブリに「餌」を与えてそれらを持続させます。同時に、追加の酵素がCyMA内の別のエステル結合をゆっくり切断してより親水性の断片に変え、これらは拡散して離れていきます。肝細胞や一部の免疫細胞のようにエステラーゼ活性の高い健康な細胞はこの分解を得意とするため、CyMAを解体しやすく、影響を受けにくいという性質があります。
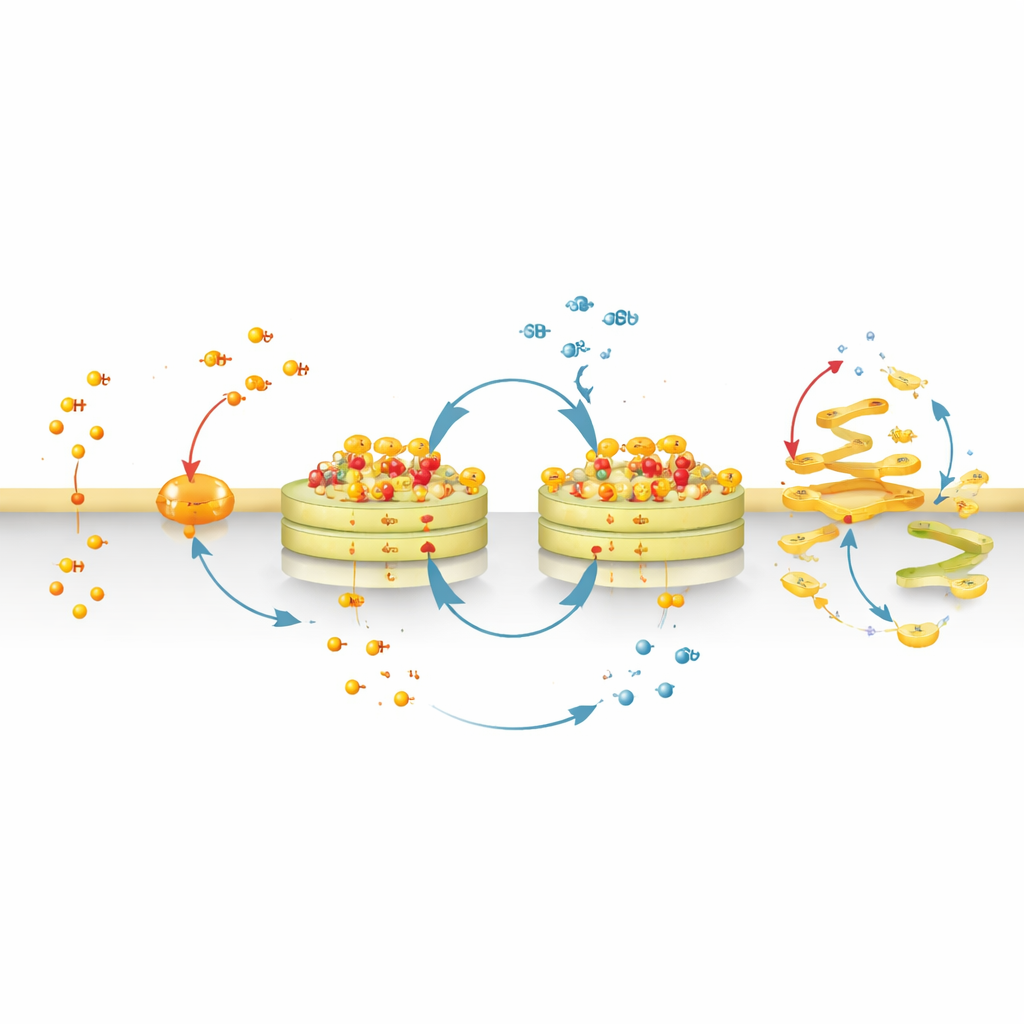
優しいイメージングツールからゴルジ破壊剤へ
蛍光色素をより強く膜親和性を持つ化学基に置き換えることで、研究チームはCyMA‑iを発光しないが依然としてゴルジで巡回・集合する破壊型のCyMA‑dに変換しました。これらのアセンブリは物理的にゴルジの構造とそこへの小胞の流れを攪乱します。通常、小胞体からゴルジへ、そこから細胞表面へと移動するタンパク質は滞留したり誤配送されたりします。細胞表面からゴルジへの輸送経路やゴルジから他のオルガネラへの経路も阻害されます。その結果、主要な表面受容体やシグナル分子は目的地に到達できなかったり、細胞内の誤った場所に蓄積したりします。
細胞のシグナルと分泌メッセージの混乱
多くのタンパク質はゴルジで糖鎖や脂質鎖といった重要な仕上げを受けます。CyMA‑dアセンブリはRasや主要な受容体チロシンキナーゼのような著名ながん駆動因子を含む多数のタンパク質の適正な脂質付加や糖鎖付加を低下させます。これらの変化はAKTやmTORといった成長促進経路を脱線させます。同時に、細胞の分泌機能は減弱し、腫瘍が免疫抑制や血管新生を促すために用いるTGF‑β1やVEGFのような重要因子が効率的に放出されなくなります。この崩壊のストレスは小胞体ネットワークのもつれ、ミトコンドリアの異常、オートファジー(細胞のリサイクル機構)の停滞、損傷を受けユビキチンで標識されたタンパク質の増加を引き起こし、これらが合わさってがん細胞を死へと追い込みます。
腫瘍への選択的圧力と治療の可能性
CyMA‑dは多くのがん細胞が使い過ぎている共通の酵素群や代謝物に依存するため、非常に低用量で薬剤耐性卵巣がんモデルを含む幅広い腫瘍タイプを殺すことができます。しかし特定のエステラーゼレベルが高い細胞はCyMA‑dを速やかに分解してダメージを受けにくく、これが選択性の内在的な原因となります。三次元の腫瘍スフェロイド、患者由来培養、マウスモデルにおいて、CyMA‑dは腫瘍を縮小させ、転移を減らし、腹水の貯留を軽減しました。免疫チェックポイント療法と併用すると、腫瘍制御と生存期間がさらに向上しました。本質的に、この研究は単一のタンパク質を標的にするのではなく、ゴルジ内に動的な材料を構築することで、がんにとって重要な複数のプロセスを同時に停止できることを示しています。
今後の治療への意味
専門外の人にとっての要点は、著者らがゴルジを受動的な傍観者から能動的な治療標的へと変えたことです。細胞自身の酵素を動員してこの中枢ハブで小さな分子を組み立てて再循環させることで、無害に可視化することも、段階的にその機能を圧倒することも可能になります。この二重用途のプラットフォームは、新しい治療の概念を示唆します。すなわち一つのタンパク質に一つの薬を作るのではなく、細胞が変換して自己組織化する材料へと導く小さな前駆体を設計し、がんが成長・転移に依存する通信と輸送のネットワーク全体を妨害するというアプローチです。
引用: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
キーワード: ゴルジ体, 分子アセンブリ, タンパク質輸送, がん治療, オルガネラ標的化