Clear Sky Science · ja
フォーク逆転とF-boxヘリカーゼ1を核とするSCFユビキチンリガーゼ複合体によるRAD51制御の構造基盤
停止したDNA複写装置を細胞はどう救うか
細胞が分裂するたびに、何十億ものDNA塩基を迅速かつ正確に複製しなければなりません。しかし、複製装置はしばしば問題に直面します—DNA損傷、複製が難しい配列、薬剤処理などによって進行が停止することがあります。そうしたとき、細胞は非常対応援チームに頼ってフォークを安定化し再起動します。本論文は、ヘリカーゼFBH1を中心に構成されるタンパク質複合体というチームリーダーが、停止したDNAをどのように形づくり、別の重要な修復タンパク質RAD51をどのように厳密に制御しているかを、前例のない構造詳細で明らかにします。この協調的な働きを理解することは、細胞が危険なゲノム切断を回避する仕組みや、これらの因子の破綻ががんと関連する理由を説明する助けになります。
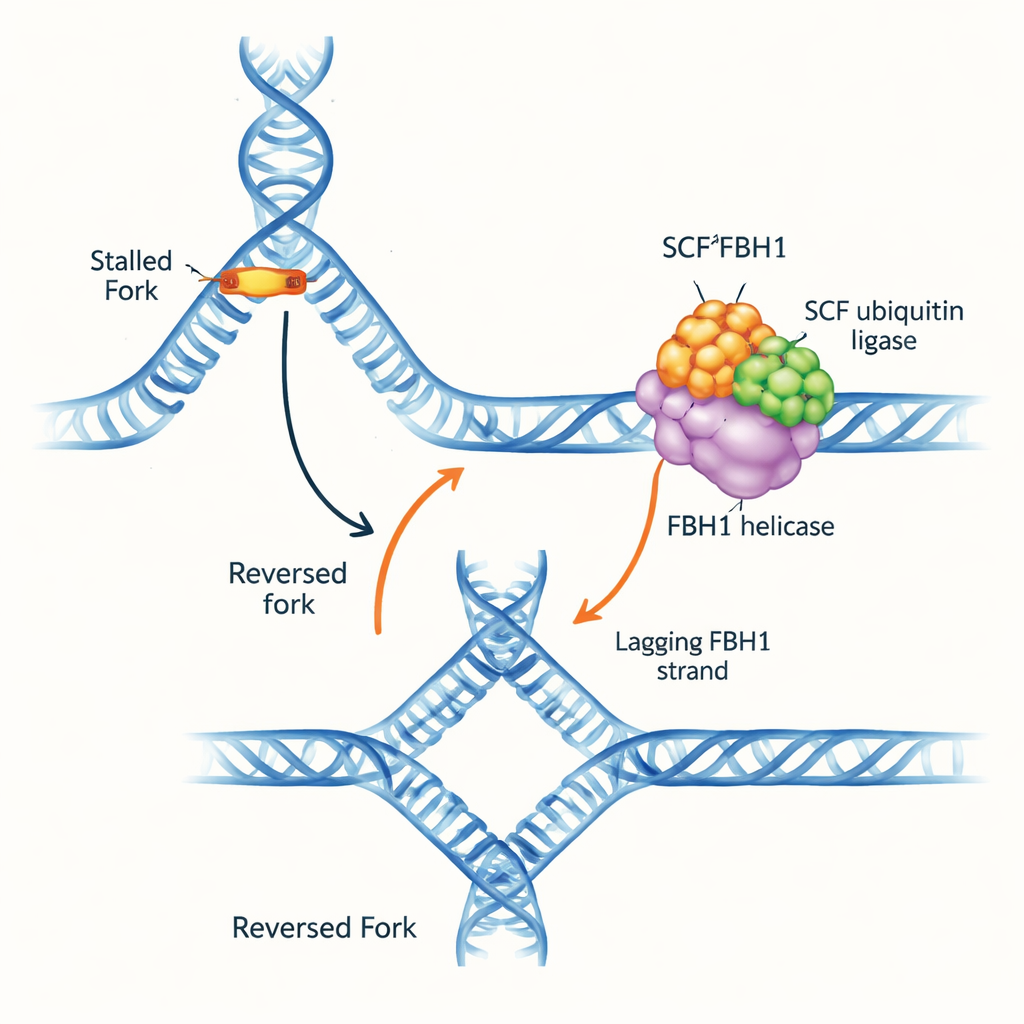
DNAハイウェイでの交通渋滞
DNA複製フォークは、二重らせんがほどかれて複製されるY字型の構造です。フォークが障害物に遭遇すると、方向を逆にすることがあります:親鎖が再び対合し、新しく合成された鎖同士が結合して四方向のDNA接合を形成します。この「フォーク逆転」は、修復と安全な複製再開の猶予を与えることができますが、誤って扱われると壊れやすいDNAを生じることもあります。いくつかの分子モーターは、フォークの前方にある二本鎖DNAを掴むことでフォークを後退させることが知られています。しかしFBH1は異なる振る舞いを示し、腫瘍で頻繁に変化が見られるため、別個で医学的に重要な経路で作用していることが示唆されていました。
片側を好むフォーク専門家
著者らは、FBH1ヘリカーゼとユビキチン付加モジュール(SCF)を組み合わせたヒトのSCFFBH1複合体を精製しました。まずFBH1がどのようなDNA形状を好むかを調べました。結合および解離アッセイにより、SCFFBH1は実際のフォーク様構造、特に「ラギング」鋳型鎖(短い断片で複製される側)に短い一本鎖DNAの伸びがある箇所を強く好むことが示されました。これらの構造上で、FBH1は単純な遊び端に比べて何百倍も速くDNAをほどくため、フォーク接合部での適切な結合がそのモーター活性を著しく高めることを示しています。単分子磁気ピンセット実験は、この複合体が一本鎖DNA上を何千塩基も外れずにほどきながら移動できる、強力で持続的なモーターであることを確認しました。
後ろから引くことでフォークを逆転させる
このモーターが実際にフォークをどう逆転させるかを解明するため、研究チームは一本鎖ギャップの有無を含む人工フォーク基質を用いて試験しました。他のフォーク再編成酵素とは異なり、SCFFBH1は完全に対合したフォークでは作用できず、ラギング鋳型のギャップを必要とし、その一本鎖上を3′→5′方向に移動しました。この「後ろから引く」動きが、酵素がフォーク接合部にクランプされたまま親鎖の再対合を駆動します。SCFFBH1が停止フォークに結合したクライオ電子顕微鏡構造はその仕組みを示しています:FBH1のあるサブドメインにある正に帯電した特別なパッチ、「接合部結合モチーフ」が、三つのDNA腕が合流する分岐点にぴったり収まっています。研究者らがこのモチーフの重要なアミノ酸二つを変異させると、試験管内でのフォーク逆転活性は約25倍低下しましたが、基本的なほどき動力は比較的良好に働き続けました。細胞内では、同じ変異がストレス誘導薬に対する複製フォークの通常の減速を妨げ、これはフォーク逆転が失敗した特徴です。
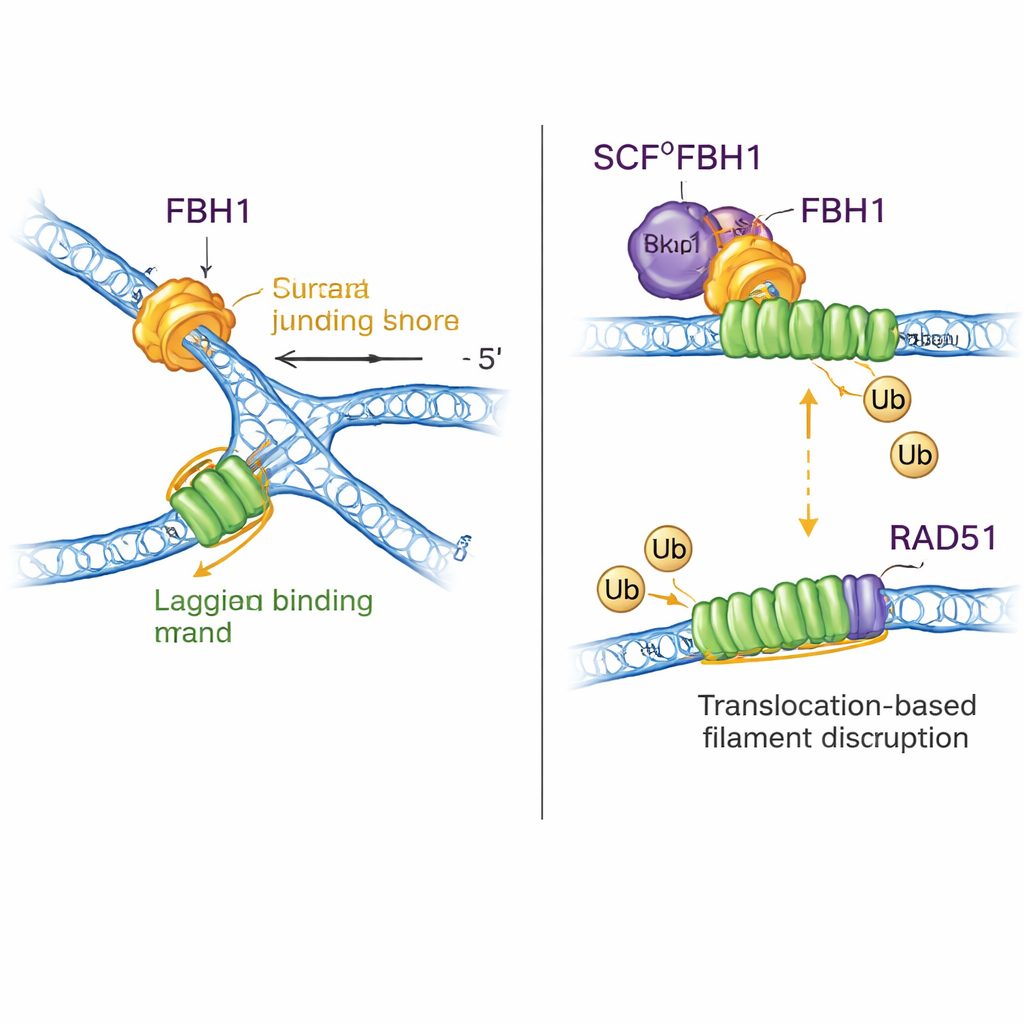
二重の役割:DNAの再形成とRAD51の除去
FBH1は単なるモーターではなく、SCF複合体を介してタンパク質に小さなユビキチンタグを付ける働きも担います。新しい構造はほぼ完全なSCFFBH1–DNA複合体を組み立て、リガーゼのユビキチン移送“ヘッド”がFBH1から出てくるラギング鎖のDNAから45オングストローム未満の距離に位置していることを示します。他のユビキチンリガーゼの既知構造を当てはめることで、著者らはこの幾何配置が、DNA上でフィラメントを形成して組換えを促進する酵素RAD51を、停止したフォークのラギング鎖上の標的に直接向けることを提案します。以前の研究は、FBH1がRAD51を機械的にDNAから剥ぎ取り、再結合しにくくするためにユビキチン修飾を付けることができると示していました。新しいモデルはこれらの考えを統一します:FBH1がラギング鎖に沿って引きながらフォークを再形成する際、近接するSCFモジュールがRAD51サブユニットにタグを付け、過剰なRAD51フィラメントを解体または再形成を抑えて、フォーク処理を妨げないように助けます。
ゲノム安定性とがんへの意味
総合すると、本研究はSCFFBH1が既知の他のフォーク再編成因子とは異なる機構で停止した複製フォークを逆転させることを示しています:分岐点をしっかり掴みながらラギング鋳型に沿って後方から移動し、長期的で可動性の高い四方向接合を形成することなく親鎖の安全な再巻き戻しを促進します。同時に、内蔵のユビキチンリガーゼは同じ鎖上のRAD51を除去するのに有利な位置に配置されており、複製ストレス時の暴走的な組換えを防ぎます。FBH1ががんで頻繁に喪失または変異することを考えると、これらの構造的・機構的知見は、なぜそのような腫瘍がDNA損傷を蓄積しやすいのか、また複製ストレスを誘発する薬剤や関連経路を標的にした治療に対して異なる応答を示すのかを説明する助けになります。
引用: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
キーワード: DNA複製ストレス, フォーク逆転, FBH1ヘリカーゼ, RAD51制御, ゲノム安定性