Clear Sky Science · ja
1032件の脳転移のプロテオゲノミクス・アトラスが示す分子サブタイプ、免疫景観、治療上の脆弱性
なぜがんは脳に転移するのか
がん治療が進歩するにつれて、患者はより長く生きられるようになり、その結果、腫瘍が肺や乳房、皮膚、結腸などの原発部位から離れて新たな場所、とりわけ脳へ広がる機会が増えています。脳転移は現在、一般的でしばしば深刻な合併症ですが、医師は依然として主に原発部位に基づいて治療を行っており—肺や乳房など—脳内でがんがどのように適応しているかには十分対応していません。本研究は1,000を超える脳転移の詳細な“アトラス”を作成し、それらの隠れた生物学、脳固有の細胞や免疫系との相互作用、そして新たな治療機会の所在を明らかにすることを目的としました。
脳腫瘍の大規模マップを作る
研究チームは、多様な原発がんに由来する1,032件の脳転移のデータを収集し、これに対応する原発腫瘍や比較用の悪性原発脳腫瘍も含めて解析しました。DNA・RNAシーケンシング、大規模なタンパク質と代謝物の測定、腫瘍および免疫細胞の単一細胞・空間マッピング、患者由来の小型オルガノイド(培養で育てた試料)など、最先端の手法を組み合わせました。これらの層を統合することで、単に遺伝子を列挙するだけでなく、脳転移の中で生物学的システム全体がどのように振る舞っているかを見ようとしました。
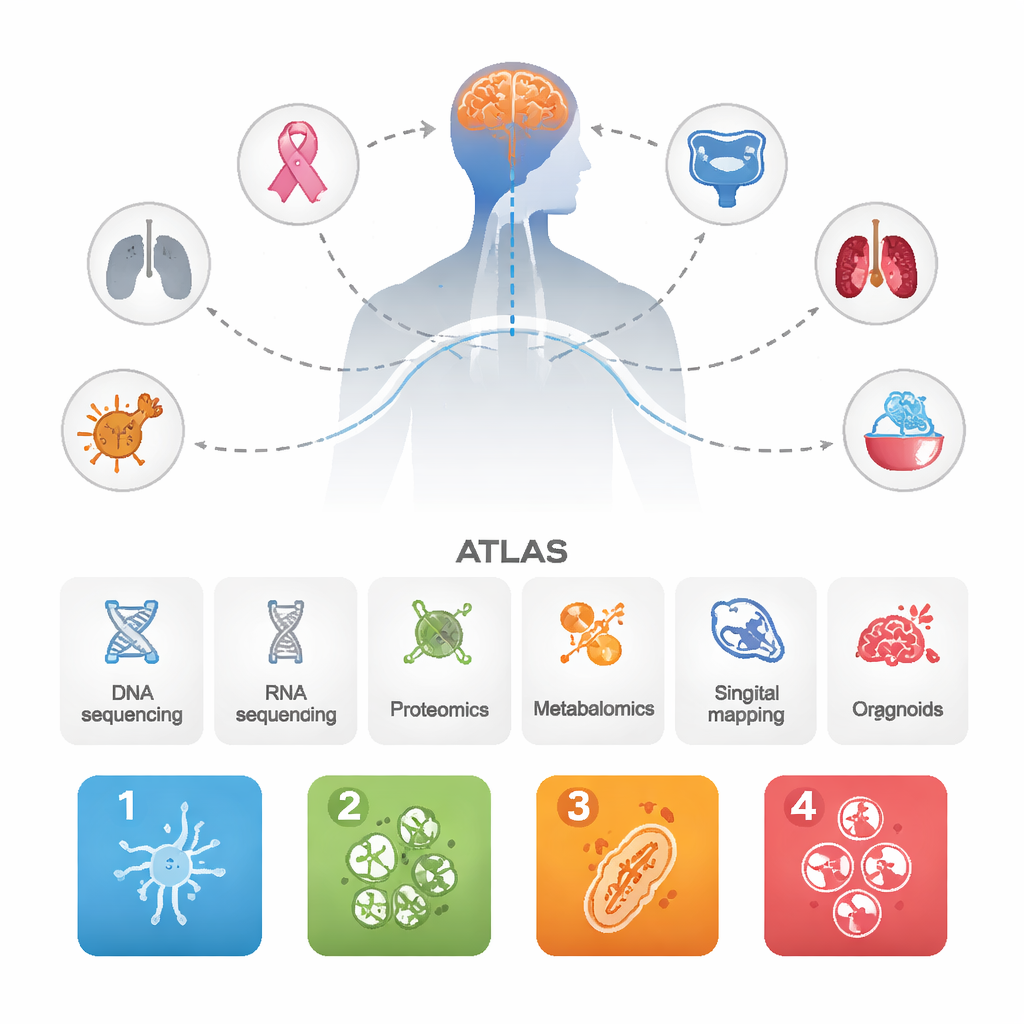
繰り返し現れる4つの「性格」
多様な原発臓器に由来するにもかかわらず、脳転移は繰り返し4つの主要な分子サブタイプに分類されました。ひとつはBrMS1と呼ばれる“ニューロン様”で、腫瘍細胞と周囲組織が多くの脳・神経細胞プログラムを発現し、比較的活発な免疫監視が見られます。BrMS2は“免疫浸潤型”で、特にT細胞を中心に免疫細胞が豊富に存在し、細胞結合を緩め局所環境を再構築するエピテリアル–間葉系転換(EMT)と呼ばれるプログラムを示します。BrMS3は“代謝型”で、脂肪酸代謝や酸化的リン酸化などの経路を通じてエネルギー利用を再配線する非常に活発ながん細胞が支配的です。BrMS4は“増殖型”で、急速な細胞分裂、幹様特徴、高いゲノム不安定性を特徴としますが、著しく免疫細胞が少ない点が際立ちます。
腫瘍の環境が示すこと
単一細胞レベルと空間分解能で詳細に見ると、各サブタイプは脳内の異なる“近隣”に住んでいることがわかりました。BrMS1病変はアストロサイトやニューロンのような脳の支持細胞に富み、腫瘍が正常な脳組織を模倣し共利用していることを示唆します。対照的にBrMS2腫瘍はPD-1などのチェックポイント分子を発現する“疲弊した”T細胞を含む密集したT細胞クラスターが点在し、活性化した血管や炎症シグナルを伴います。BrMS3は代謝的に活発な領域に位置し、BrMS4は急速に分裂する細胞の島を形成し、周囲は比較的免疫の少ない領域です。全体として、本研究は脳転移(原発腫瘍ではない)において、EMTの強い活性化が高いT細胞浸潤と結びつく傾向があり、このプログラムが免疫細胞の侵入を助ける可能性を示唆しました。
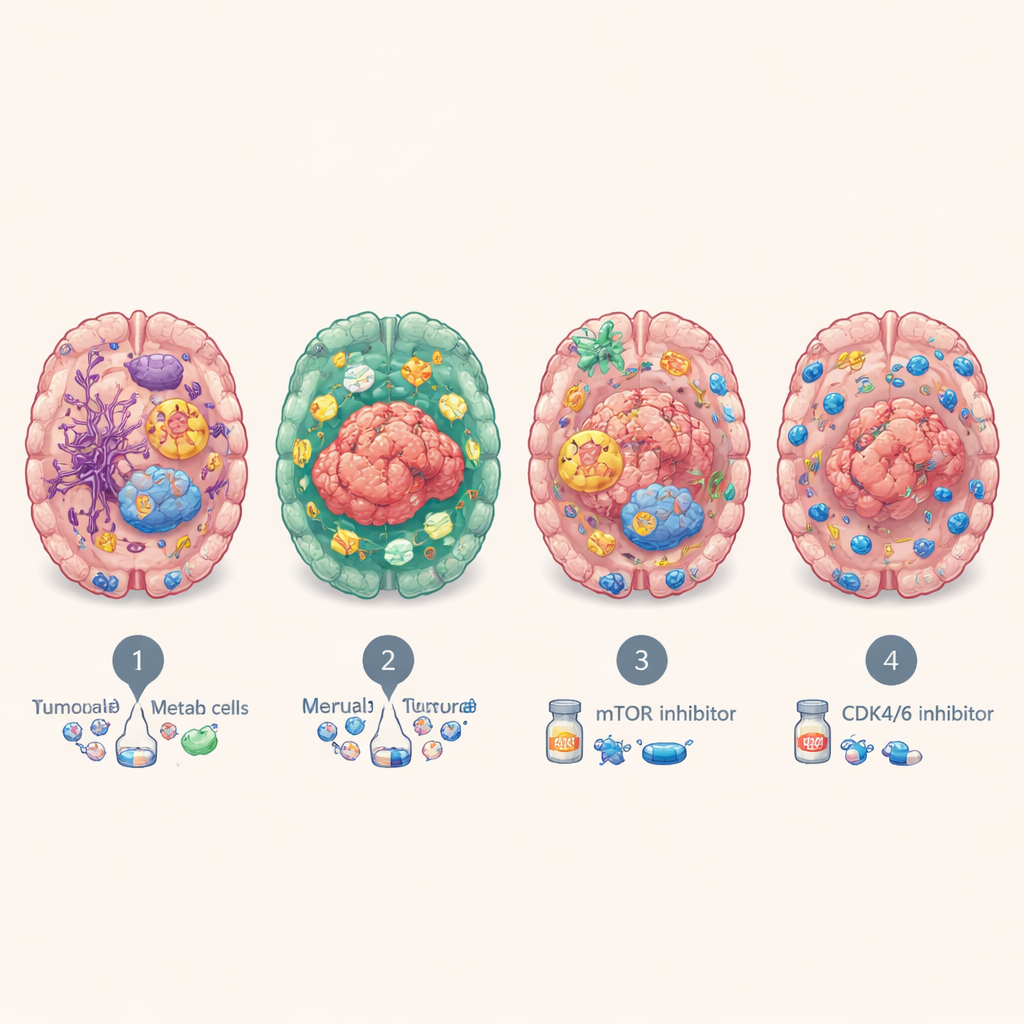
治療と患者予後への手がかり
これらの分子“性格”は単なる学術的な分類にとどまりませんでした。免疫浸潤型のBrMS2を持つ患者は、増殖型のBrMS4を持つ患者よりも生存が長い傾向があり、BrMS4は一貫して最も成績が悪い群でした。患者由来オルガノイドで薬剤を試験した結果、代謝型のBrMS3腫瘍は細胞成長と代謝を制御するmTORシグナル経路の阻害に特に感受性があり、急速増殖するBrMS4腫瘍は細胞周期を遅らせるCDK4/6阻害剤に対して脆弱であることが示されました。別の解析では、BrMS1は放射線療法により良く反応する可能性が示唆され、BrMS2の炎症を伴うチェックポイント豊富な環境は疲弊したT細胞を再活性化する免疫療法の恩恵を受けやすいかもしれないと示唆されました—ただし、これは脳転移患者で直接確認する必要があります。
脳転移をもつ患者にとっての意義
このアトラスは、がん細胞が脳に到達すると、原発部位にかかわらずいくつかの共有された生物学的状態に収束する傾向があることを示しています。個々の脳転移がニューロン様、免疫豊富、代謝型、あるいは高増殖性のどれに当てはまるかを理解することは、放射線療法、免疫療法、代謝や細胞分裂を標的とする薬剤といったより個別化された治療の選択につながる可能性があります。本研究はまだ標準治療を直ちに変えるものではありませんが、これらの分子上の脆弱性を患者にとってより良く、より精密な治療につなげるための将来の研究と臨床試験のための詳細なロードマップを提供します。
引用: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
キーワード: 脳転移, 腫瘍サブタイプ, 腫瘍微小環境, がん免疫療法, がん代謝