Clear Sky Science · ja
マウスの年齢に依存しない組織適応をミクログループRNAがECMと発生経路を介して宇宙飛行で形作る
なぜ宇宙旅行は私たちの体を変えるのか
月や火星への旅がSFから現実的な計画へ移る中で、ひとつ大きな疑問が残ります:長期の宇宙飛行は分子レベルで体をどのように再構築するのか?宇宙飛行士は骨や筋肉を失い、心臓や免疫系が変化し、その一部は地球上の加齢に伴う疾患に似ています。本研究は国際宇宙ステーションで数週間過ごしたマウスを用い、マイクロRNAと呼ばれる小さな遺伝子調節因子が、軌道上で臓器全体の適応――あるいは機能不全――にどう寄与するかを明らかにします。
軌道上のマウスを全身的に見る
単一臓器の研究を越えるために、研究者たちは宇宙ステーションで3〜6週間過ごした雌マウスの13の異なる臓器から686のサンプルを解析しました。これらの動物は、通常の飼育条件下の地上対照群と、ステーションの狭い空間、温度、湿度、上昇した二酸化炭素を模した特殊なケージで飼育された対照群の2つと比較されました。この入念な実験設計により、微小重力や放射線といった“宇宙そのもの”に由来する変化と、マウスが経験した特異な飼育・取扱いに起因する変化とを切り分けることが可能になりました。焦点はマイクロRNAにあり、タンパク質を作らない短いRNA配列が、多くの遺伝子の働きを同時に調節します。
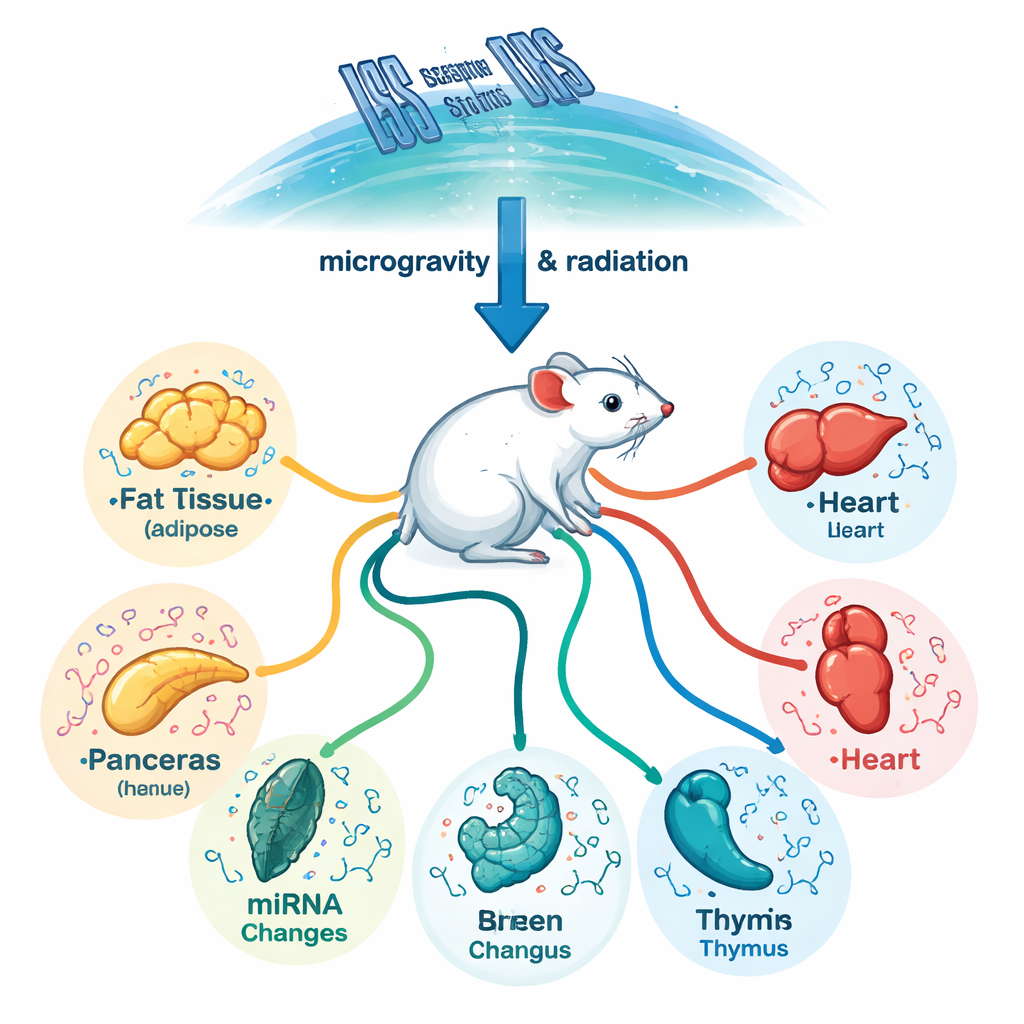
主要臓器でのマイクロRNAはマスタースイッチとして働く
各臓器はそれぞれ固有のマイクロRNAの「設定」を持っていましたが、宇宙飛行はこれらの設定を特定のパターンで変化させました。皮膚下や内臓周りの脂肪、肝臓、膵臓、脾臓、胸腺が最も強い宇宙依存の変化を示し、一方で脳、腎臓、いくつかの脂肪部位は地上の飼育条件に対してより敏感でした。研究チームは、宇宙にさらされた動物で一貫して変動した73種のマイクロRNAを見出し、多くは臓器特異的でした。関連するマイクロRNA群、特にMIR-17/92やMIR-1/133のファミリーが主要な役割を示しました。これらのファミリーは地球上で心機能、がん、代謝に結び付けられており、比較的小さな調節分子群が惑星外での生活に対する多くの応答を統括している可能性を示唆します。
組織のリモデリングと損傷修復
マイクロRNAはメッセンジャーRNAの量を調整してタンパク質の設計図に影響を与えるため、研究者たちは同じ動物から得た単一細胞の遺伝子発現マップとマイクロRNAデータを組み合わせました。これにより、脂肪組織、肝、肺、心、脾臓で特に一致する数千の遺伝子変化が明らかになりました。影響を受けた遺伝子は、組織の構造を再構築しストレスに対処する経路に集中していました:細胞をつなぐ細胞外マトリックスの構築・分解、細胞の増殖や移動の誘導、神経やシナプス構造の調節、放射線によるDNA損傷への応答などです。例えば脂肪組織では、マイクロRNAが血管新生や細胞の物理的足場に関わる遺伝子に影響を与え、代謝器官の大規模なリモデリングを示唆しました。胸腺や他の免疫器官では、マイクロRNAがDNA修復や免疫細胞の成熟を制御する転写因子を標的にしており、感染防御や潜在的ながんリスクに対する複雑な影響を示唆しています。
宇宙ストレスと単純な加齢の違い
多くの宇宙飛行士の症状は加齢による虚弱を連想させるため、研究チームは宇宙飛行が通常の加齢過程を単に加速しているのかを問いました。彼らは若年成体マウス(約3か月)と中年マウス(約8か月)を比較し、さらに地上での年齢関連マイクロRNA変化の大規模アトラスと照合しました。年齢は影響しましたが、宇宙飛行そのものほど大きな要因ではありませんでした:ほとんどの組織で宇宙は両年齢群に類似した変化を引き起こしました。明確な年齢依存性を示したのは膵臓、横隔膜(主要な呼吸筋)、特定の腹部脂肪貯蔵などごく一部の臓器だけでした。これらの組織では、MIR-8、MIR-15、MIR-154の3つのマイクロRNAファミリーが特に活発で、細胞増殖、筋維持、がん関連プロセスを制御する遺伝子を標的にしていました。驚くべきことに、全体像は単純に加齢が加速したものには一致せず、いくつかのマイクロRNAは加齢に似た傾向を示す一方で、他は明確に宇宙特有の経路をたどっていました。
将来の探検者にとっての意義
専門外の読者にとっての核心的なメッセージは、軌道上での数週間が多くの臓器を協調したリモデリングプログラムへと押し進め、その舵取りをするのは数種類のマイクロRNAであり、これらは一度に何百もの遺伝子を調節する、ということです。これらの変化は微小重力や放射線に対する組織の応答を助けますが、糖尿病、心疾患、がんで見られるような病態へと傾かせる可能性もあります。重要なのは、本研究が単なる急速な加齢よりもむしろ特徴的な“宇宙状態”の証拠を示しており、中年のマウスでも強固な応答が見られた点です。もし人間でも同様のパターンが成り立つなら、少数の主要なマイクロRNAファミリーを標的とする薬や遺伝子療法がいつか宇宙飛行士の臓器を保護し得ること、そして分子スイッチを適切に制御できれば中年の探検者も長期ミッションに参加できる可能性があることを示唆します。
引用: Grandke, F., Rishik, S., Wagner, V. et al. MiRNAs shape mouse age-independent tissue adaptation to spaceflight via ECM and developmental pathways. Nat Commun 17, 1387 (2026). https://doi.org/10.1038/s41467-026-68737-1
キーワード: 宇宙飛行生物学, マイクロRNA, 組織リモデリング, 細胞外マトリックス, 加齢と宇宙