Clear Sky Science · ja
プロパルギル炭酸塩のニッケル触媒を用いた分岐スルホネーション反応
この化学が研究室を越えて重要な理由
硫黄含有分子は、多くの現代医薬品、作物保護剤、先端材料の中心的存在です。しかし、これらの化合物を精密かつ効率的に、かつ柔軟に合成することはしばしば困難です。本論文は、簡便な出発物質を複数の異なる硫黄含有分子群へと変換でき、しかも立体配座を厳密に制御できるニッケル触媒法を記載しています。こうした制御性は医薬品探索を加速し、化学者が複雑な分子をよりクリーンかつ持続可能に構築するのに役立ちます。
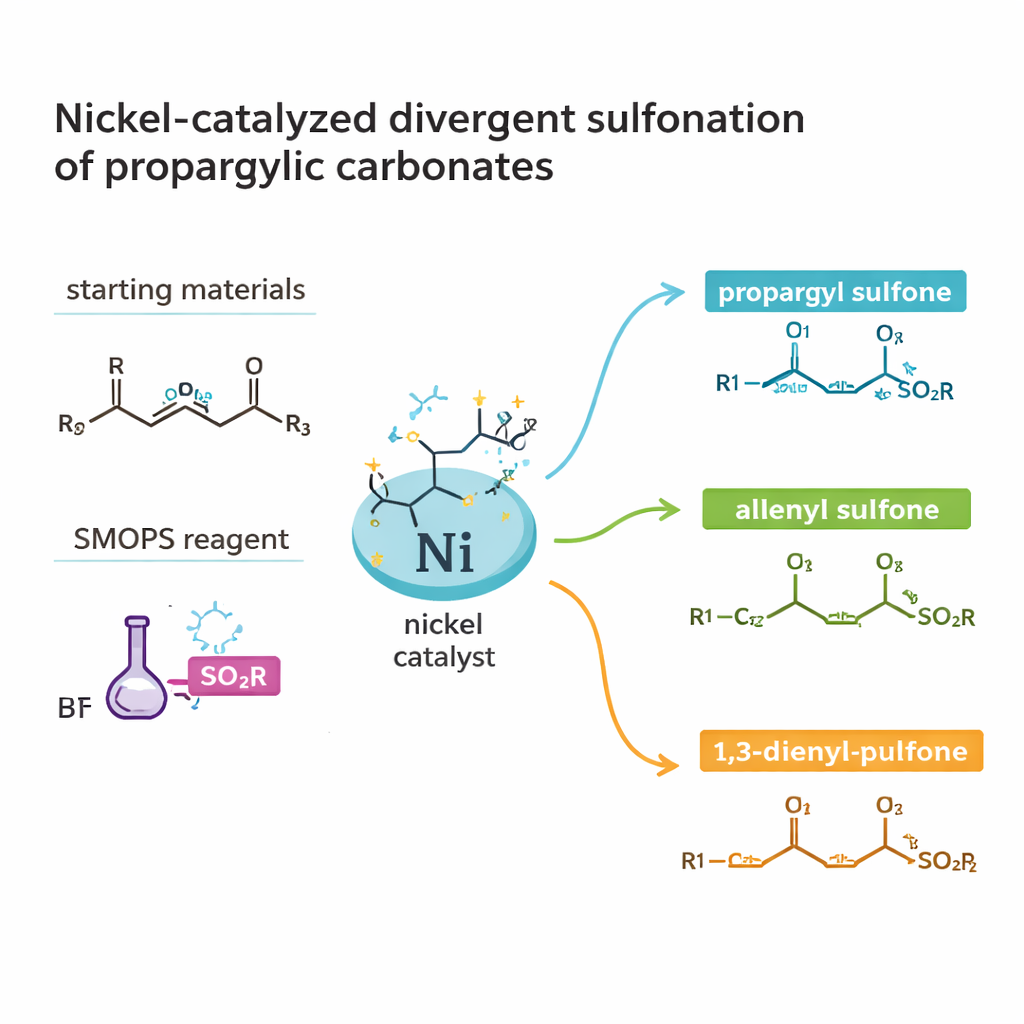
単純な部品から有用な分子を組み立てる
本研究は、硫黄が酸素や炭素と結合したスルホンおよびスルフィネートと呼ばれる分子群に焦点を当てています。これらの構造は生理活性天然物や医薬品に広く見られますが、従来の合成経路は長く廃棄物を生みやすいことが多いです。著者らは特に有用な亜種であるキラルスルフィネートに注目しています。鏡像異性体が生体内で大きく異なる挙動を示すことがあるためです。既に複雑な出発物質を用いる代わりに、彼らは入手容易な2つの反応相手、すなわちプロパルギル炭酸塩(出る基を備えた小さな炭素骨格の一種)と市販の硫黄供与体SMOPSを用います。これらをニッケル触媒下で組み合わせることで、1〜2段階で高付加価値な硫黄含有生成物を得ることを目指しています。
一つの触媒系で三つの生成物群を選択
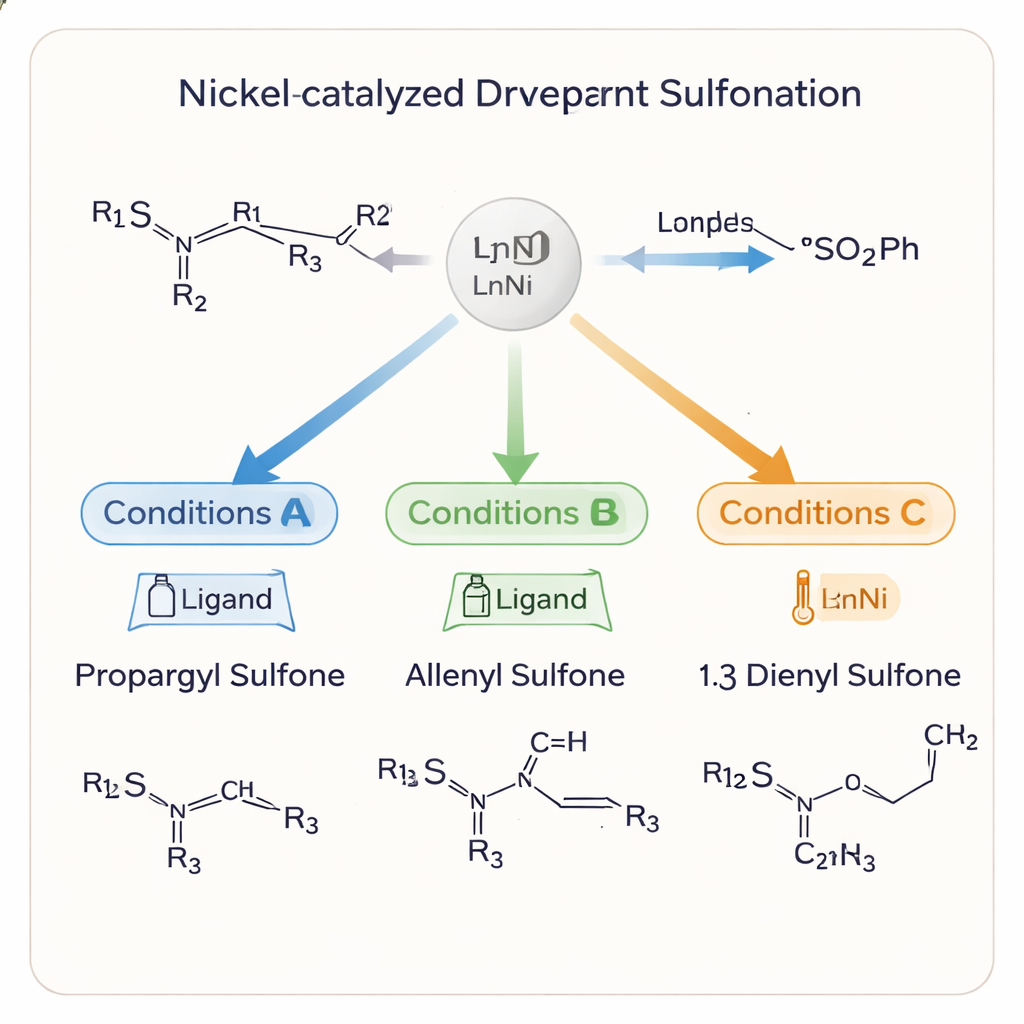
本研究の顕著な特徴は、同じ基本的成分からプロパルギルスルホン、アレンイルスルホン、1,3-ジエニルスルホンという三種の異なる生成物を導くことができる点です。これらそれぞれの炭素骨格は、その後の化学変換や生物活性に異なる影響を与えます。ニッケルに結合する配位子、溶媒、温度、添加剤を慎重に選ぶことで、研究者は反応を特定の結果へ“誘導”できます。アセトニトリル中、キラルホスフィン配位子を用いる穏和な条件では、プロパルギルスルホンを高収率かつ優れたエナンチオ選択性で得られます。これらの生成物を酸化アルミニウムで処理すると、キラリティーを保持したまま三重結合が穏やかにアレンへと再構築されます。別の配位子と溶媒に切り替えると、反応は1,3-ジエニルスルホンへと進み、炭素骨格が延長されます。
適用範囲と柔軟性の検証
この手法がどれほど一般的かを評価するために、研究者らは両方の反応相手を変化させました。単純なアルキルやアリール、複雑な環状系を含む多様なナトリウムスルフィネートがクリーンに反応し、高いエナンチオ過剰でキラル生成物を与えることを示しました。同様に、芳香環や炭化水素鎖に異なる置換基を持つ広範なプロパルギル炭酸塩も良好に反応しましたが、非常にかさ高い基や末端アルキンをもつ基質はいくつか現行法の適用外でした。さらに、スケールアップしても効率や選択性を損なわないことを示しており、実用化への重要な一歩となります。この広い適用範囲により、化学者は多様な断片を差し替えて関連する硫黄含有分子のライブラリを迅速に構築できます。
構築単位を複雑な標的へ変換する
単にスルホンを合成するだけでなく、著者らはそれらを他の有用な構造へ容易に変換できることを示しています。水素化により三重結合をアルカンやアルケンに還元しても、硫黄に隣接するキラル中心は保持されます。簡単な後続反応でスルホン部分をスルフィネート、スルホンアミド、スルホニルフルオライドへと変換でき、いずれも医薬化学や“クリック様”結合形成反応で頻繁に用いられるモチーフです。ハイライトとして、彼らはこの方法を鍵段階として用い、キラルβ-スルフィニルヒドロキサム酸という細菌酵素を阻害することが知られる分子を簡潔に合成しています。この経路は従来の幾つかの煩雑な段階を回避しており、必要に応じてキラルスルフィネートを用いることの合成上の強みを示しています。
反応がどのように経路を選ぶか
研究チームは反応がなぜ生成物を切り替えるのか、その機序も探っています。経時観察により、プロパルギルスルホンが通常最初に形成され、条件によってはそれがアレンへ、さらに1,3-ジエンへと再配列することが示されました。ニッケル触媒は選択した配位子や添加剤とともに、どの中間体が有利か、どのように硫黄基が炭素鎖上を移動するかを制御します。例えば酸化アルミニウムは、アルキンからアレンへの型変換を非常に低温で進行させつつ、原子の三次元配列を保持することを可能にします。簡略化された機構モデルは、反応条件の微妙な変化が共通のニッケル中間体を別々の経路へと導き、一つの系で複数の精密に定義された生成物を与え得る理由を説明しています。
将来の医薬品や材料にとっての意義
専門外の方への主要な結論は、このニッケル触媒法が多用途の化学的“スイッチボード”を提供するという点です。同じ単純な出発物から、化学者は望む硫黄リッチな骨格を選び、一段階で高い選択性をもって得ることができます。これらの生成物は医薬品や他の機能性分子の優れた構築単位であるため、コンセプトから候補化合物への道のりを短縮する可能性があります。また、触媒と反応条件の慎重な設計が、かつては困難だった変換を日常的なツールへと変えうることを示しており、複雑でキラルな硫黄含有分子のより迅速でクリーンな構築への扉を開きます。
引用: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
キーワード: ニッケル触媒, キラルスルホン, 不斉合成, 有機反応設計, 医薬候補となる構築単位