Clear Sky Science · ja
大腸菌への分子蓄積をクリック反応で測定する方法
小さな薬が危険な細菌に届きにくい理由
現代医療は抗生物質に依存していますが、最も危険な細菌のいくつかは多数の薬剤を遮断する堅固な外膜で守られるようになりました。大腸菌のようなグラム陰性菌は特に有効な外膜バリアを持ち、実際に細胞内に入り標的に到達する薬を設計するのが難しくなります。本論文はCHAMPアッセイと呼ばれる新しい実験法を紹介しており、何千もの異なる小分子がこれらの防御をどれだけ回避して生きた大腸菌細胞内に蓄積するかを迅速に測定できます。
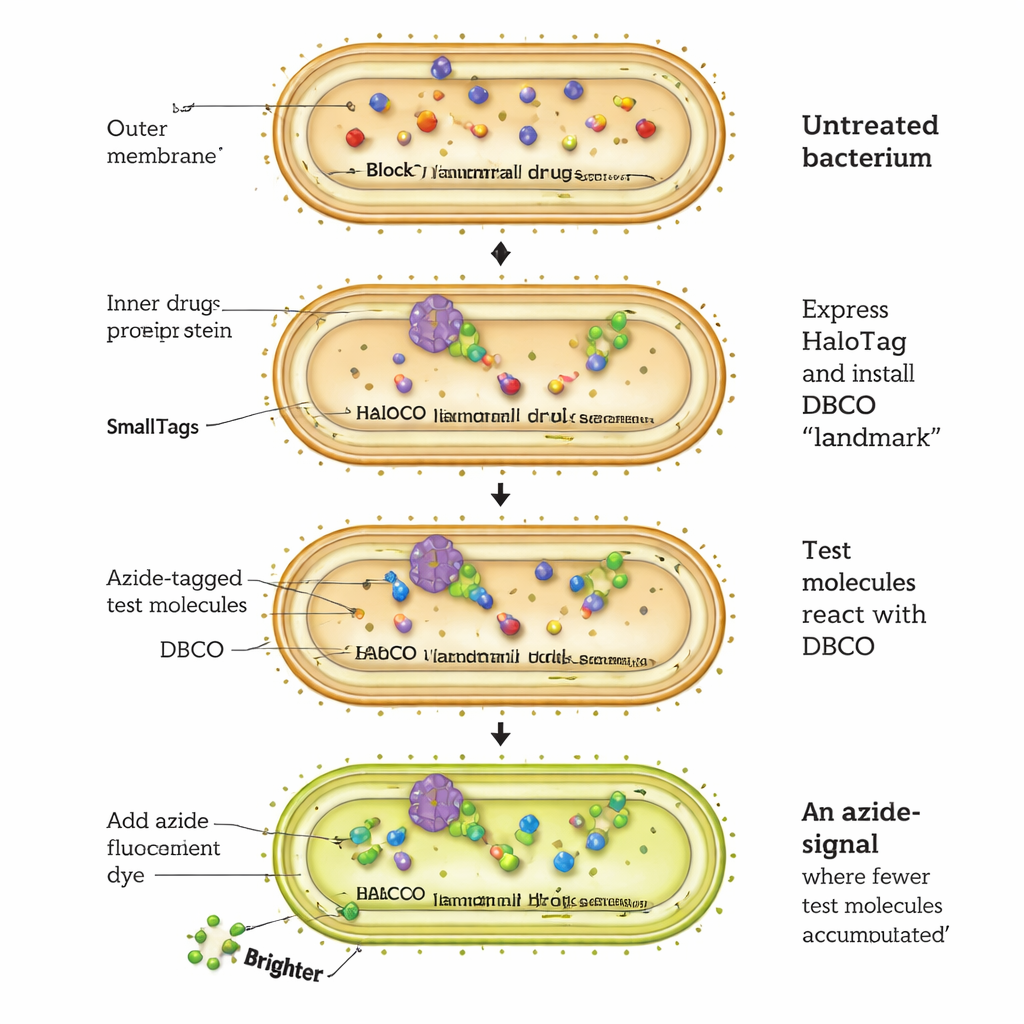
薬が細菌細胞に入る様子を観察する新しい方法
従来の抗生物質探索は天然由来化合物や細菌の生育試験に頼り、細菌が生きるか死ぬかを見ていましたが、そうした試験は実際にどれだけの薬が細胞内に入ったか、入った後にどこへ行ったかを明らかにしません。著者らは、抗生物質の多くの標的が存在する細胞質内への薬物侵入を直接かつ広く利用できる方法で追跡する手段を構築することを目指しました。彼らの目的は、薬の取り込み、標的結合、下流の生物学的効果が混ざった粗い指標(例えば最小発育阻止濃度)を超えて、細胞内蓄積をクリーンに測定することでした。
細菌を小さな化学記録器に変える
CHAMPアッセイはHaloTagと呼ばれる細菌タンパク質を分子の着地パッドのように作り変えることで機能します。大腸菌は細胞質にHaloTagを発現するように遺伝子改変されます。まず研究者は短いクロロアルカンリンカーを使ってHaloTagに「ひずんだ」アルキンであるDBCOという特殊な化学ハンドルを取り付けます。次に、非常に小さなアジドタグを持つ試験分子を細菌に曝露します。外膜を通過し、内膜を越えて細胞質に到達できた試験分子だけが、選択的な“クリック”反応でDBCOハンドルと反応してHaloTagを恒久的に標識します。最後に、残った未反応のDBCOにのみ結合できるアジド修飾蛍光色素で細胞を処理します。蛍光が明るいほど細胞質に到達した試験分子は少なく、蛍光が暗いほどより多くの蓄積があったことを示します。
化学と生物学が薬の侵入をどう左右するかを探る
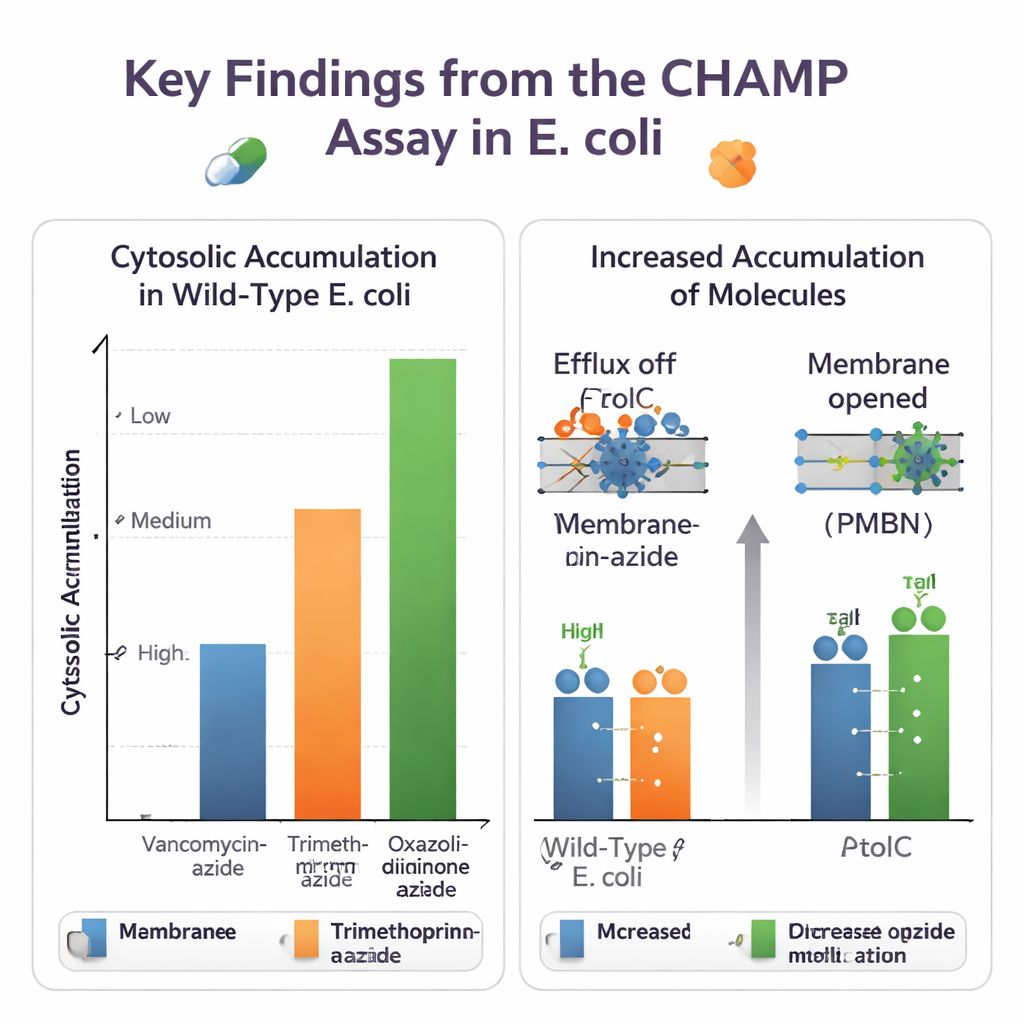
CHAMPを使って、研究チームはまずHaloTagの発現量、DBCOアンカーの量、蛍光色素の選択を最適化し、大きく信頼できる信号ウィンドウを確保しました。次に、化学的変更が侵入にどう影響するかを見るため、互いに類似した小分子セットを使用しました。カルボン酸をアミドに変えることや塩基性アミノ基の付加・除去は細胞質内レベルを目に見えて変えることがありました。多くの場合、一次アミンは蓄積を高め、他の研究グループが示した「eNTRyルール」と一致する結果が得られました。またこのアッセイは実際の抗生物質のアジドタグ付与版も扱うことができ、バンコマイシンのようなかさ高い薬はほとんど細胞質に到達しない一方で、トリメトプリム誘導体や一部のオキサゾリジノン系のような小さな抗生物質ははるかによく侵入する、という大きな差を明らかにしました。
薬を細胞外へ排出する防御機構を暴く
この方法は生きた遺伝学的に操作可能な細菌で動作するため、さまざまな細胞防御の役割を解明できます。著者らは通常の大腸菌と、主要な多剤排出ポンプの重要な構成要素であるTolCを欠く株、または小分子TolC阻害剤で処理した細胞を比較しました。ノボビオシンなどのいくつかのアジド付き抗生物質について、TolCが無効化されるとCHAMPは明確に高い細胞質蓄積を示し、これらの化合物が排出基質であることを確認しました。さらに、ペプチドPMBNで化学的に外膜を緩めるか、広口のポリンチャネルを過剰発現させるなどの方法で外膜バリアを緩和すると、多くの以前は蓄積が乏しかった分子が大きく増加し、侵入と排出が内部薬物レベルを共に決定していることを浮き彫りにしました。
数千の分子へスケールアップしてパターンとルールを掴む
真の高スループット性を示すために、研究者らは市販の404種類のアジド修飾化合物セットと、1,152種類のアジド含有分子を収めたカスタムライブラリをスクリーニングしました。彼らは未処理細胞、PMBN処理細胞、ハイパーポリン化細胞、そしてTolC欠損のハイパーポリン化細胞など、いくつかの細菌コンテキストで蓄積を測定しました。同じ分子をこれらの条件間で比較することで、クリック反応速度の違いに起因する特異性ではなく、細胞生物学に由来する変化を見分けることができました。CHAMPデータを計算解析と組み合わせることで、極性表面積、水素結合能力、特定の環状骨格などの物化学的特徴がTolCベースの排出による認識と結びつくことが明らかになりました。この種の大規模プロファイリングは、排出ポンプを回避するかポリンをよりうまく利用する分子設計のルールの輪郭を描き始めます。
将来の抗生物質にとっての意義
簡潔に言えば、この研究は大腸菌を大量処理可能なセンサーに変え、試験化合物が多くの薬物標的が存在する細胞内領域にどれほど入るかを正確に報告します。CHAMPは細菌が死ぬかどうかの試験に取って代わるものではありませんが、「入ること」と「損害を与えること」を分離して測定する重要なギャップを埋めます。数千の分子を突然変異や化学的に改変した株で数日内に測定できる能力により、どの化学的特徴が侵入を促進し排出を抑え、あるいは膜破壊剤と組み合わせて有利に働くかを体系的に学べるようになります。その知見は、グラム陰性病原体の強固な防御を突破できる新しい抗生物質や補助薬の設計を加速し、抗生物質の武器庫がさらに耐性に侵食されるのを防ぐ助けとなるはずです。
引用: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
キーワード: 抗生物質耐性, 大腸菌, 薬物透過性, 排出ポンプ, クリックケミストリー