Clear Sky Science · ja
教師なしアルゴリズムの展開による高速ブラインド構造化照明顕微鏡法
細胞内の生命をより鮮明なムービーで
現代生物学は生きた細胞の動態を観察することに大きく依存していますが、多くの重要な構造は通常の顕微鏡では小さすぎたり速すぎたりして鮮明に捉えられません。本論文は、ぼやけた高速取得画像をリアルタイムで鮮明な超高解像度ムービーに変換する新しい手法を紹介します。完璧に調整されたハードウェアを必要としないこの手法、展開型ブラインド構造化照明顕微鏡(UBSIM)は、高速で高度な細胞イメージングを一般的な研究室でも利用しやすくする可能性があります。
なぜ通常の顕微鏡は限界があるのか
従来の光学顕微鏡は回折という光の基本特性に制約され、数百ナノメートルより小さな細部はぼやけてしまいます。構造化照明顕微鏡(SIM)は試料にパターン化された光を照射し、その干渉パターンを利用して情報を引き出すことで解像度を概ね2倍に向上させます。しかし古典的なSIMは照明パターンを厳密に知らなければならず、慎重な較正が必要で、装置が高価で扱いにくくなることがあります。これに対し、ブラインド‑SIMはランダムなパターンでも許容し、データから試料と照明の両方を同時に推定することでハードウェア要件を緩和します。ただし、この推定プロセスは遅く反復的で、1フレームあたり数秒〜数分かかり、生きた細胞のリアルタイムムービーには到底間に合いません。
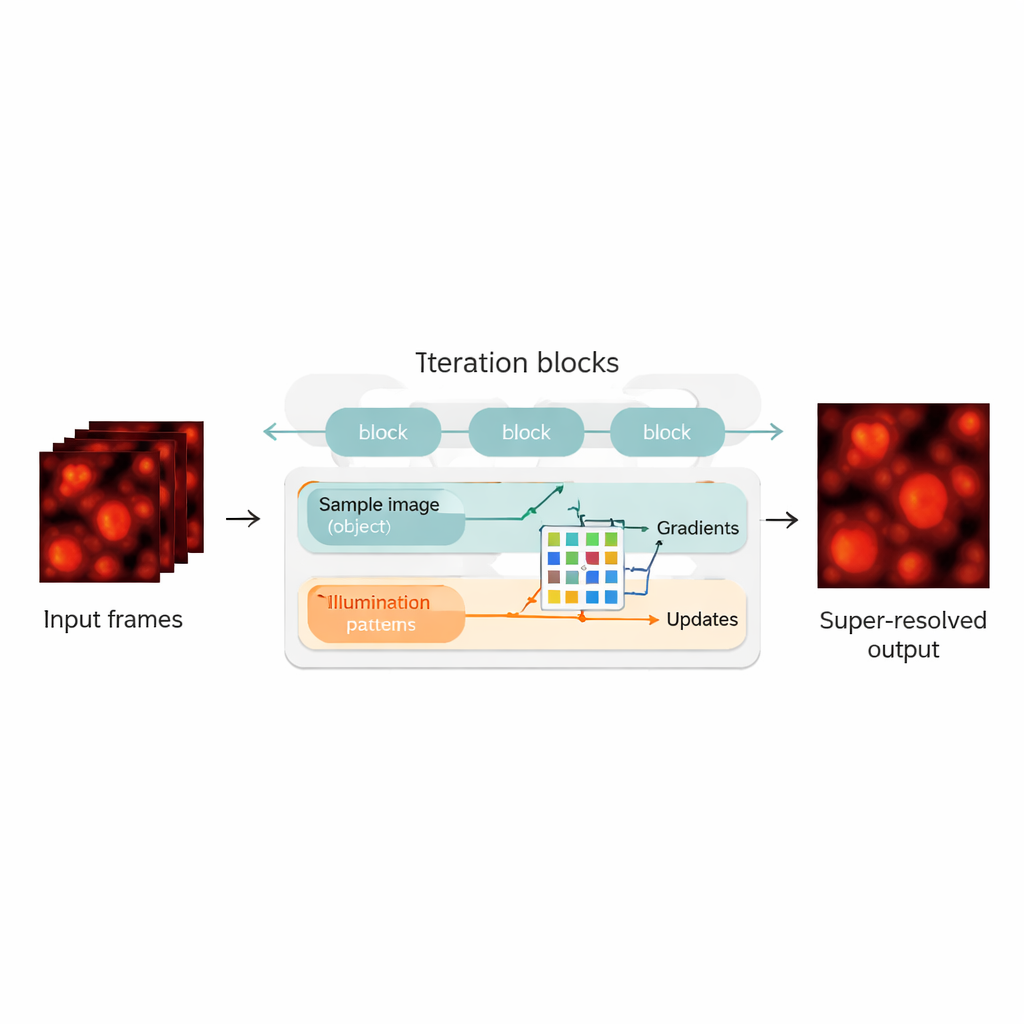
物理モデルとニューラルネットワークの融合
著者らは、ブラインド‑SIMの再構成を物理ベースのモデルとニューラルネットワークのハイブリッドとして再設計することでこのギャップを埋めます。彼らは元の反復アルゴリズムを「展開」し、各反復をニューラルネットワークの層に対応させ、一連の更新ブロックを形成します。各ブロック内で、現在の試料と照明の推定が測定画像をどれだけ説明しているかを評価し、改善方向(勾配)を計算し、それらをコンパクトな畳み込みニューラルネットワークに入力します。このネットワークは、元のアルゴリズムの自動調整された加速器のように、より賢い修正ステップを学習します。重要なのは、UBSIMが教師なしで訓練される点です:理想的な正解画像を必要とせず、顕微鏡光学がどのように光を通すかという物理モデルだけを用いるため、ネットワークが見かけ上もっともらしいが誤った構造を「幻覚」するリスクを減らします。
高速で正確、推測に頼りにくい
UBSIMを評価するため、研究チームはまず真の基盤構造が既知のシミュレーション画像を用いました。UBSIMは通常の広視野画像に比べて約2倍の解像度を回復し、標準的なブラインド‑SIMと同等の性能を示しつつ、2〜3桁高速に動作することが分かりました—256×256ピクセルの画像は数秒ではなく約10ミリ秒で再構成できます。誤差、類似度、信号対雑音比などの画像品質指標も従来法に比べて著しく改善しました。さらに、UBSIMは未知のデータに対して一般的な深層学習ベースの超解像ネットワークより信頼性が高いことが示されました。ある種類の構造で訓練された標準的ネットワークは異なる試料に対して訓練時のパターンを押し付け、微妙だが誤解を招くアーティファクトを生む傾向がありましたが、UBSIMは視覚例だけに依存せず基礎となるイメージング物理に根ざしているため一貫した忠実性を保ちます。
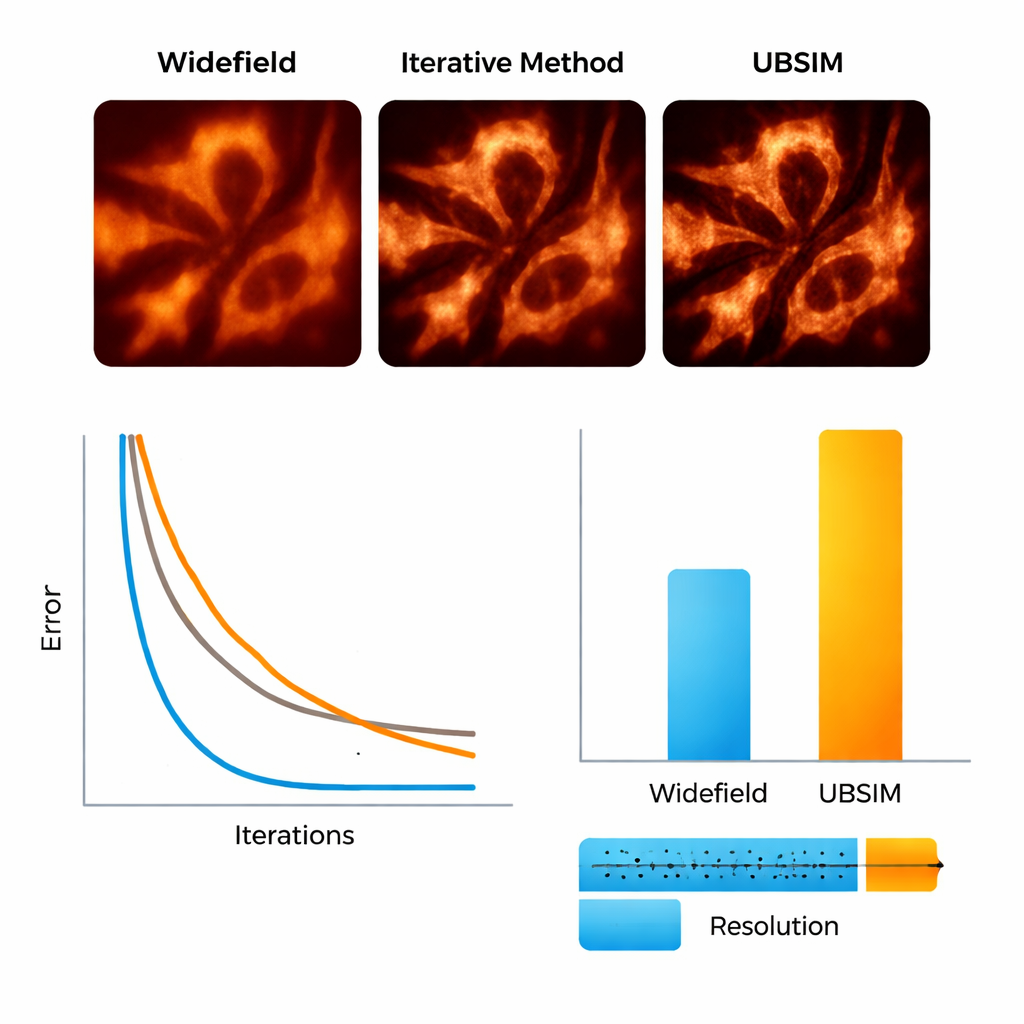
細胞の骨格と膜の動きを観る
研究者らは次に実際の生物学的試料へと移りました。ランダムなスペックルパターンを投影する柔軟な装置を用いて生細胞を撮像し、細胞内のタンパク質の「足場」であるアクチン線維や、タンパク質合成やストレス応答に関与する分岐膜ネットワークである小胞体(ER)を観察しました。UBSIMにより、通常の画像でぼんやり見えていたアクチン繊維がはっきりと分離した線として再現され、解像度はおおむね300ナノメートルから約150ナノメートルに向上しました。特に注目すべきは動画速度での超解像が可能になったことです:生データを最大100フレーム毎秒で取得し、最大50超解像フレーム毎秒で再構成することで、ERの管状構造が成長、崩壊、再編成する様子をリアルタイムで観察できました。こうした数分の一秒から数秒のスケールで起きる動態は、従来の手法では十分な詳細で可視化するのが難しいことが多いです。
今後の細胞イメージングへの意義
専門外の方への要点は、UBSIMにより微細な細胞構造の動きをリアルタイムで、通常の光学顕微鏡の限界を超えて実用的かつ明確に観察できるようになったことです。完璧なハードウェア較正や大規模な訓練データセットを要求しない点も重要です。物理ベースのモデルの信頼性と現代のニューラルネットワークの速度を組み合わせることで、ノイズの多いパターン化画像群を迅速に信頼できる超鮮明なムービーに変換します。手法がさらに洗練され、照明戦略と組み合わされることで、小胞体がストレスにどう応答するか、細胞骨格が移動や分裂の際にどう再編成されるか、疾患がどのように細胞の構造をナノスケールで変えるかなどの研究に貢献する可能性があります。
引用: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
キーワード: 超解像顕微鏡, 構造化照明, 深層学習, 生細胞イメージング, 小胞体ダイナミクス