Clear Sky Science · ja
β-アレスチン1とGαsあるいはGαi1の相互作用に関する機能的および構造的洞察
これが健康と医療にとって重要な理由
アレルギー薬から心臓薬、精神科治療薬に至るまで、現代の多くの医薬品はGタンパク質共役受容体(GPCR)と呼ばれる巨大な細胞表面タンパク質群を標的にしています。これらの受容体は、Gタンパク質とベータ-アレスチンという二つの主要な仲介者を用いて細胞内へメッセージを伝えます。本研究は、ひとつのベータ-アレスチン(ベータ-アレスチン1)が細胞内で二種類のGタンパク質にどのように直接的に接触するかを調べています。この隠れた“会話”を理解することで、細胞内の信号の流れを微調整し、副作用の少ないより精密な薬剤設計につながる可能性があります。
細胞内の二つの主要な伝達者
ホルモンや薬が細胞表面のGPCRに結合すると、広く二つの通信経路が誘導されます。一つはGタンパク質を介する経路で、これらはGDPをGTPに交換することで分子タイマーのようにオン・オフを切り替えます。もう一つはベータ-アレスチンを介する経路で、これはGタンパク質シグナルを遮断すると同時に独自のシグナル経路を開始することができます。長い間、研究者たちは受容体がGタンパク質とベータ-アレスチンに個別に働きかける様子を主に研究してきました。最近の研究は、Gタンパク質とベータ-アレスチンが互いに結合したり、受容体とともに大きな「メガ複合体」を形成したりする可能性を示唆しましたが、これらタンパク質がどのように結びつき、それがシグナル伝達に何を意味するかの細部は不明でした。
誰が誰に結合するかの測定
本研究では、研究者たちはベータ-アレスチン1と二つのGタンパク質αサブユニット、すなわち通常は細胞活性を刺激するGαsと一般にそれを抑制するGαi1に注目しました。高感度の結合測定法を用いて、精製したベータ-アレスチン1と各Gタンパク質が異なる条件下でどれほど強く結合するかを調べました。その結果、鍵となる要因はGタンパク質が「オン」か「オフ」かではなく、ベータ-アレスチン1がより活性化された柔軟な形をとっているかどうかでした。尾部が欠けているベータ-アレスチン1のバージョン—これは自由で活性に近い形のアンサンブルとして振る舞う—はGαsおよびGαi1の両方に強く結合しました。対照的に、休止形のベータ-アレスチン1や受容体尾部様ペプチドによってロックされた形は弱く、あるいはまったく結合しませんでした。これは、Gタンパク質が受容体活性化後に存在し得る活性様の形をとる際のベータ-アレスチン1を優先的に認識することを示唆しています。 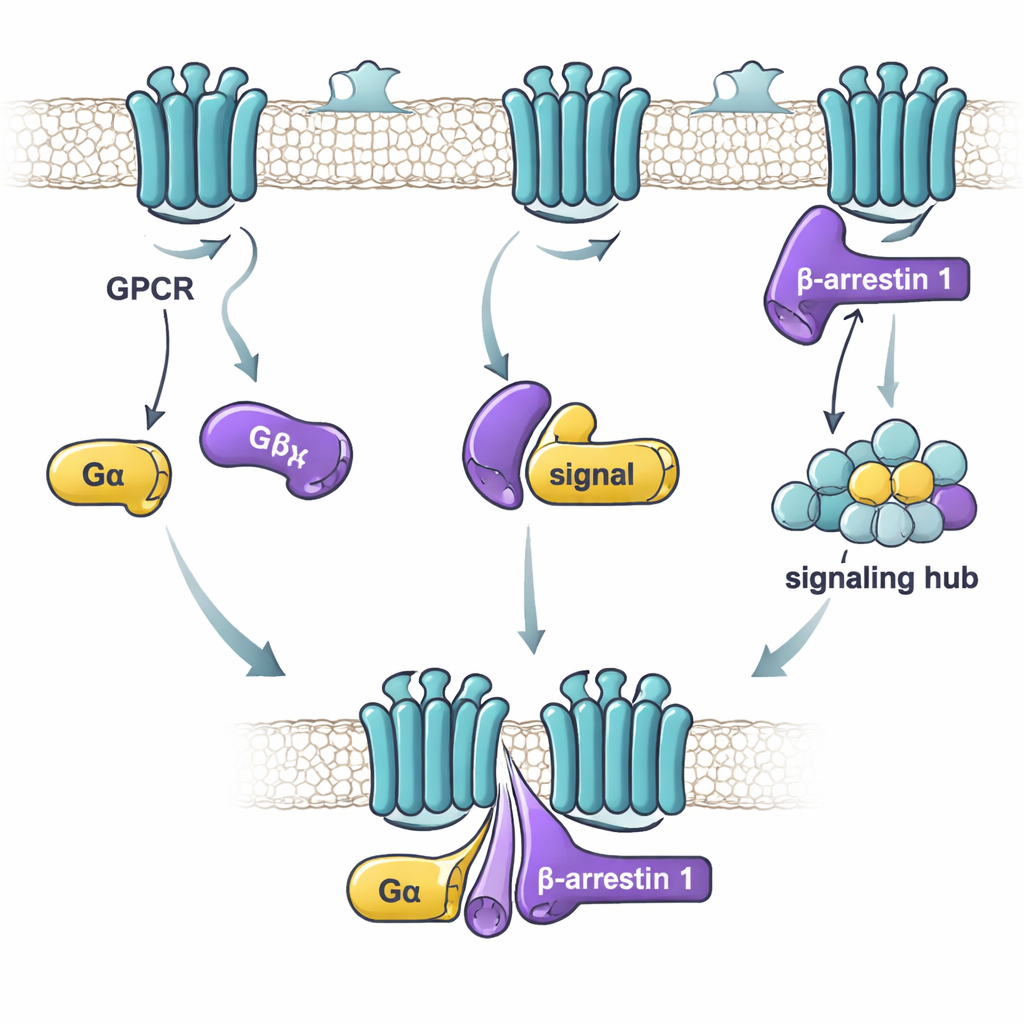
微妙な形状変化の観察
結合がタンパク質の立体構造にどのような影響を与えるかを見るために、研究チームはタンパク質の主鎖上の水素原子が溶媒中の重水素とどれだけ速く入れ替わるかを追跡する手法を使用しました。入れ替わりが遅い部分は通常より保護され硬くなったことを意味し、速い部分はより柔軟か露出したことを意味します。活性様のベータ-アレスチン1断片がGαsまたはGαi1に結合すると、両方のGタンパク質でいくつかの領域に明確なパターン変化が生じ、複合体周りで再配置が起きていることを示しました。対照的に、ベータ-アレスチン1自身の変化はわずかで、主に柔軟なループ領域に限られていました。さらにGタンパク質の分離ドメインを用いることで、主要な触媒的“Ras様”部分とそれを取り巻くαヘリカル部分の両方が結合に寄与することが示されました。Gαsではヘリカル領域が特に重要な役割を果たし、Gαi1では両領域がほぼ同等に重要でした。
主スイッチを切り替えずに働く機能
次に、これらの直接的接触がGタンパク質のオン化に影響するかを調べました。研究チームは、Gタンパク質がGDPからGTPに切り替わる際に光る蛍光GTP模倣プローブを用い、活性化の速度と程度を標準的に測定しました。驚くべきことに、ベータ-アレスチン1を加えてもGαsやGαi1のヌクレオチド交換の速度や程度は変わりませんでした。言い換えれば、ベータ-アレスチン1はGタンパク質に対する古典的な“オンスイッチ”酵素のようには振る舞わないのです。代わりに、その影響はベータ-アレスチン1自身の構造に現れました。尾部の動きを蛍光で追跡できるように工夫したベータ-アレスチン1を用いると、受容体由来のペプチドが存在する場合に活性化されたGαsはベータ-アレスチンのC末端尾部の解放を促進しますが、Gαi1はそうしないことが分かりました。生細胞における追加のイメージングとエネルギー移動センサーの測定でも、ホルモン刺激によりGαsとベータ-アレスチン1が近接し、Gαsがベータ-アレスチン1をより活性化された構 conformation(尾部が解放された形)へと押しやることが確認されました。 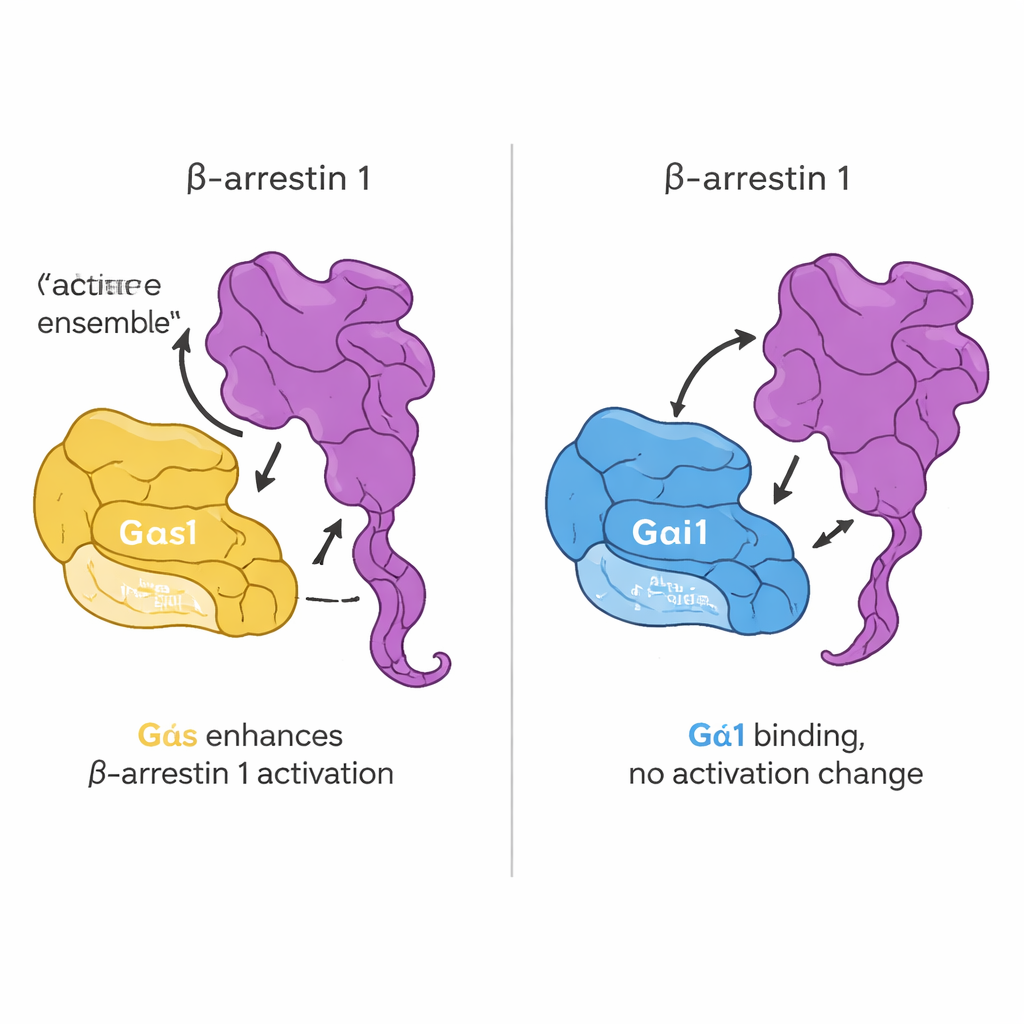
細胞シグナル伝達における新たな制御層
これらの結果を総合すると、研究はGαsとGαi1がどちらもベータ-アレスチン1に直接結合するが、結合様式や結果にわずかな違いがあることを提案しています。どちらのGタンパク質もこの接触によって主要な“オン/オフ”挙動が変わるわけではありません。むしろ、特にGαsの場合、この相互作用はベータ-アレスチン1の尾部解放を促したり安定化したりする微調整のノブとして作用します。これはGPCRシグナル伝達にこれまで過小評価されていた層を追加するものです。すなわち受容体がGタンパク質とベータ-アレスチンを調整するだけでなく、Gタンパク質とベータ-アレスチンが互いに直接的に変調し合うことがあり得るということです。長期的には、こうした微細な相互作用をマッピングすることで、薬剤設計者が有益な経路を促進しつつ副作用を引き起こす経路を避けるようなシグナルの舵取りを行える可能性があります。
引用: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
キーワード: Gタンパク質共役受容体, ベータ-アレスチン, Gタンパク質シグナル伝達, 細胞シグナル伝達メカニズム, 構造生物学