Clear Sky Science · ja
シャペロン工場における共翻訳的四次構造の決定
細胞の「組立ライン」は巨大な機械をどう保つか
私たちの細胞内では、DNAを複製するエンジンから他のRNAを合成する工場に至るまで、数千ものタンパク質部品が複雑な分子機械へと組み合わさる必要があります。本研究は、一見単純だが重要な疑問を投げかけます:新しい部品が作られるその瞬間に、どの補助タンパク質がどの部品を護衛すべきかを細胞はどう決め、混沌とした細胞質の液相でこの過程をどのように整理しているのか?
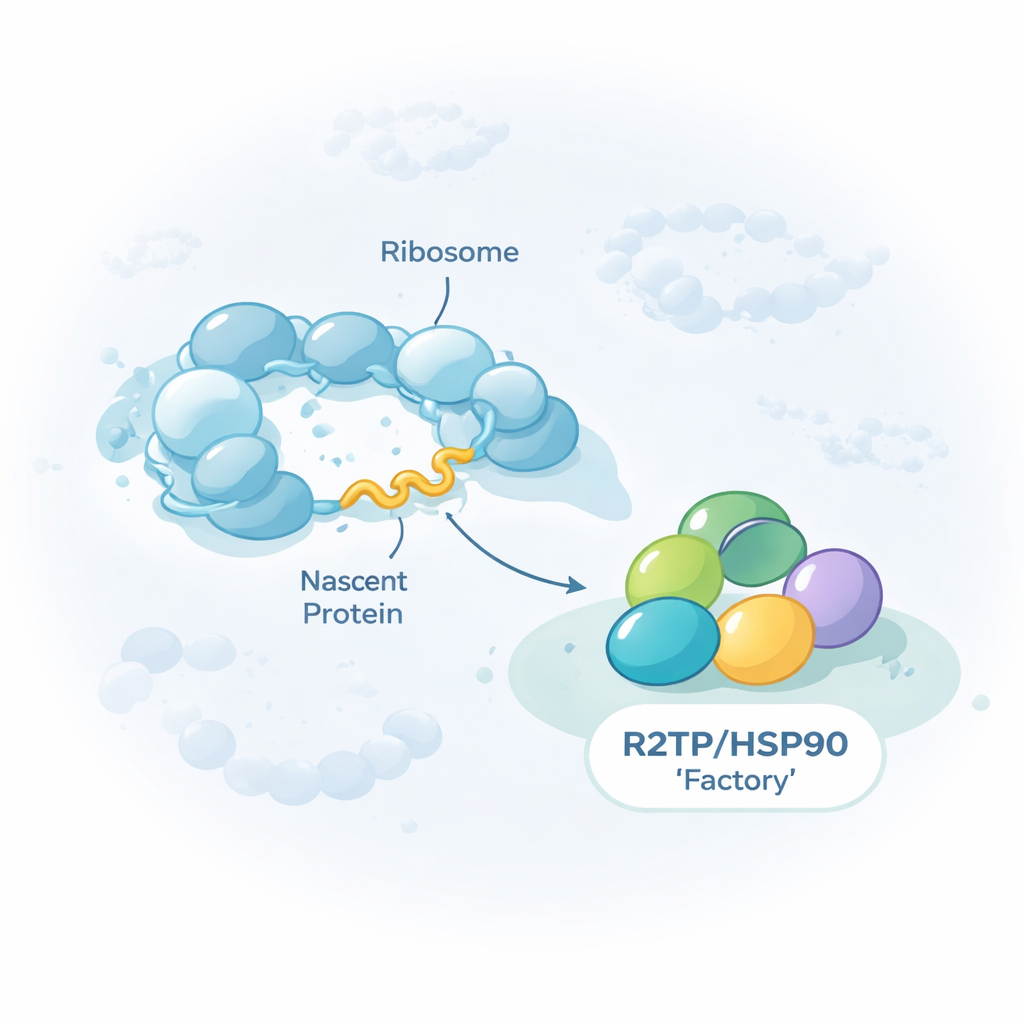
細胞巨大機械のための汎用ヘルパー
本論文はHSP90/R2TPとして知られる一群のヘルパータンパク質、いわゆるシャペロンに焦点を当てます。個々のタンパク質の折りたたみだけを担うのではなく、このシャペロンは三種類の核内RNAポリメラーゼや特定のRNA–タンパク質複合体、DNA包装を再構成する大型リモデリング機構など、巨大で多部品からなる複合体の組立てを専門にします。著者らはR2TPがこれらのクライアントタンパク質に完成後にだけ出会うわけではないことを示します。むしろ、多くの場合で各クライアントがリボソーム上で作られている最中にR2TPが付着します。ヒト細胞からR2TPを引き出して同時に回収されたRNAをシーケンスすると、約150種類のメッセンジャーRNAが見つかり、これらのコードするタンパク質が翻訳中にR2TPと接触していることが分かりました。
伸長するタンパク質鎖に寄り添うヘルパー
この結合が本当にタンパク質合成中に起きるかを検証するため、研究チームは翻訳を凍結または撹乱する薬剤を用いました。伸長中のポリペプチド鎖をリボソームから剥がす化合物を使うと、多くのメッセンジャーRNAはR2TPの結合から消えました。一方、リボソームを一時停止させてナサント鎖(新生鎖)をリボソームに残す薬では、R2TPの結合が増加しました。設計されたリポーターRNAでも確認されました:翻訳が人工的に早期に停止されると、シャペロンはそのメッセージに結合しなくなります。これらの結果は一貫した関与ルールを示唆します:R2TPは主にリボソームから現れてくる伸長中のタンパク質鎖を通じてクライアントを認識し、RNA配列そのものでは認識していないということです。
特定のメッセージが集まるシャペロン製「工場」
先進的な単一分子イメージングを用いて、著者らは驚くべき発見をしました。多数の異なるクライアントメッセージがランダムに散在するのではなく、特にRNAポリメラーゼIIの主要サブユニットや大きなスプライシング因子PRPF8をコードする重要なメッセージのいくつかが、細胞質の明るい焦点に集まることが観察されたのです。これらの焦点はR2TPおよびそのパートナーであるHSP90、リボソーム成分、そしてまさに作られているタンパク質に富み、活発な翻訳サイトであることを示していました。翻訳やR2TP/HSP90のATPase活性が阻害されると、これらの焦点は解消しました。著者らはこれらの構造を「R2TP工場」と呼びます:選択されたメッセンジャーRNAとシャペロンが濃縮され、新しく現れるタンパク質鎖と組立ヘルパーとの迅速で保護的な接触が促進される特殊な凝縮体です。
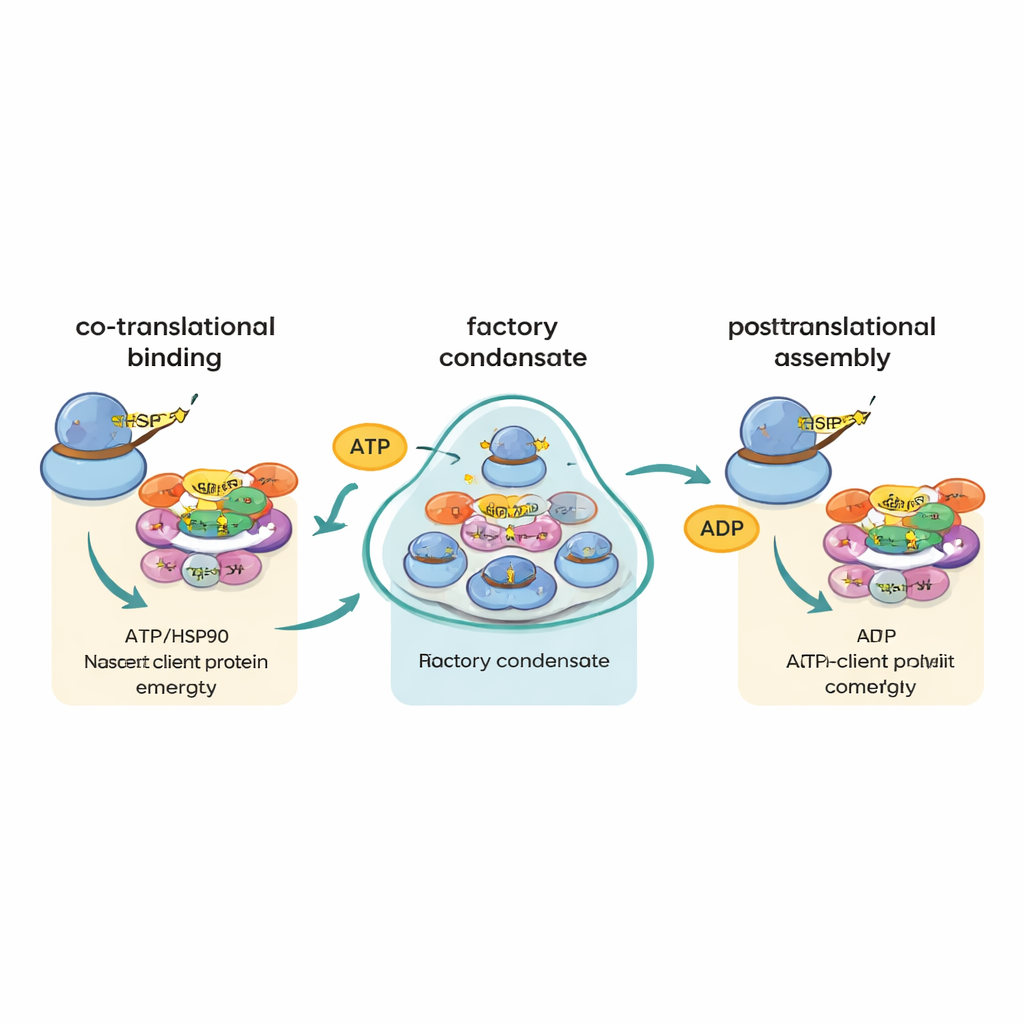
設計図を揃えずに部品を回す経路
以前の考えの一つに、同じ複合体の異なる部品をコードするメッセージが互いに出会い並んで翻訳されることで、それらのタンパク質産物が即座に組み立てられる、というものがありました。新しい研究はこの「共局在化設計図」モデルをほとんど否定します。同じ機械に結合することが知られているタンパク質対でさえ、そのメッセンジャーRNAが一緒に見つかることはまれでした。代わりに、著者らは「共翻訳シャペロンチャネリング」、通称「cha-cha」と呼ぶ別の戦略を支持するデータを提示します。このスキームでは、大きなタンパク質や組立てに脆弱なタンパク質がリボソームから出始めると、R2TPとHSP90が取り付きその運命を決め、後続の組立て段階へと導きます。工場そのものは主として対応するメッセージ同士を集めるわけではなく、むしろ新しく生まれた脆弱なタンパク質が適切なシャペロンと迅速に出会う確率を高めます。
この隠れた組織が健康と病気に関わる理由
R2TPとHSP90が壊れやすいタンパク質部品を守るだけでなく、それらがどこでどのように翻訳されるかをも形づくることを明らかにしたことで、本研究は細胞内組織化の予期せぬ層を暴きます。cha-chaメカニズムは、部品のメッセージ同士がほとんど同じ場所を共有しないにもかかわらず、細胞が巨大な分子複合体を確実に組み立てられる理由を説明します。また、シャペロンやそれらのエネルギーサイクルの欠陥がRNAポリメラーゼやスプライシング因子などの重要な機械を不安定化させ、発達障害からがんに至るまでの結果を引き起こし得ることも示唆します。本質的に、この研究は細胞が動的なシャペロン「工場」に依存して、新しく作られた部品を適切なアセンブリへと経路誘導し、内部機構の効率と秩序を保っていることを示しています。
引用: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
キーワード: タンパク質シャペロン, 共翻訳アセンブリ, 分子機械, RNAポリメラーゼ, 細胞の品質管理