Clear Sky Science · ja
抗菌薬耐性に対する多段階・多目的学習を通じた強力な高分子抗生物質の反復的発見
なぜ新しい抗生物質が誰にとっても重要か
薬剤耐性感染症は世界的に増加しており、よくある病気が治療しにくく、場合によっては治療不可能になることもあります。本研究は、従来とは異なる種類の抗生物質を迅速に発見する新しい方法を示します。それは、難治性細菌を殺すだけでなく、ペニシリンのような古い薬の効果を取り戻す小さな合成高分子です。本研究は高度な人工知能を化学と動物実験と組み合わせ、試行錯誤だけでは不可能な巨大な化学空間を探索します。
混雑した化学宇宙で新たな防御因子を探す
従来の抗生物質は通常特定の細菌タンパク質を標的とし、細菌はそれを徐々に回避することができます。それに対して本研究の高分子は、我々の体内にある防御ペプチドを模倣し、細菌膜に物理的なダメージを与えることで作用し、耐性が生じにくいという特長があります。課題は、数万種類に及ぶ可能な高分子構造が存在し、その挙動は陽イオン性、親水性、疎水性成分の微妙なバランスに依存することです。安全で強力なものを見つけるために候補を手作業で十分に試験するには何年もかかります。著者らは約10万種の関連高分子からなる組合せライブラリ、poly(β‑amino ester)(ポリ(ベータ‑アミノエステル))を構築し、それぞれが細菌細胞表面と強く相互作用できる自己集合させたナノサイズ粒子になるよう設計しました。
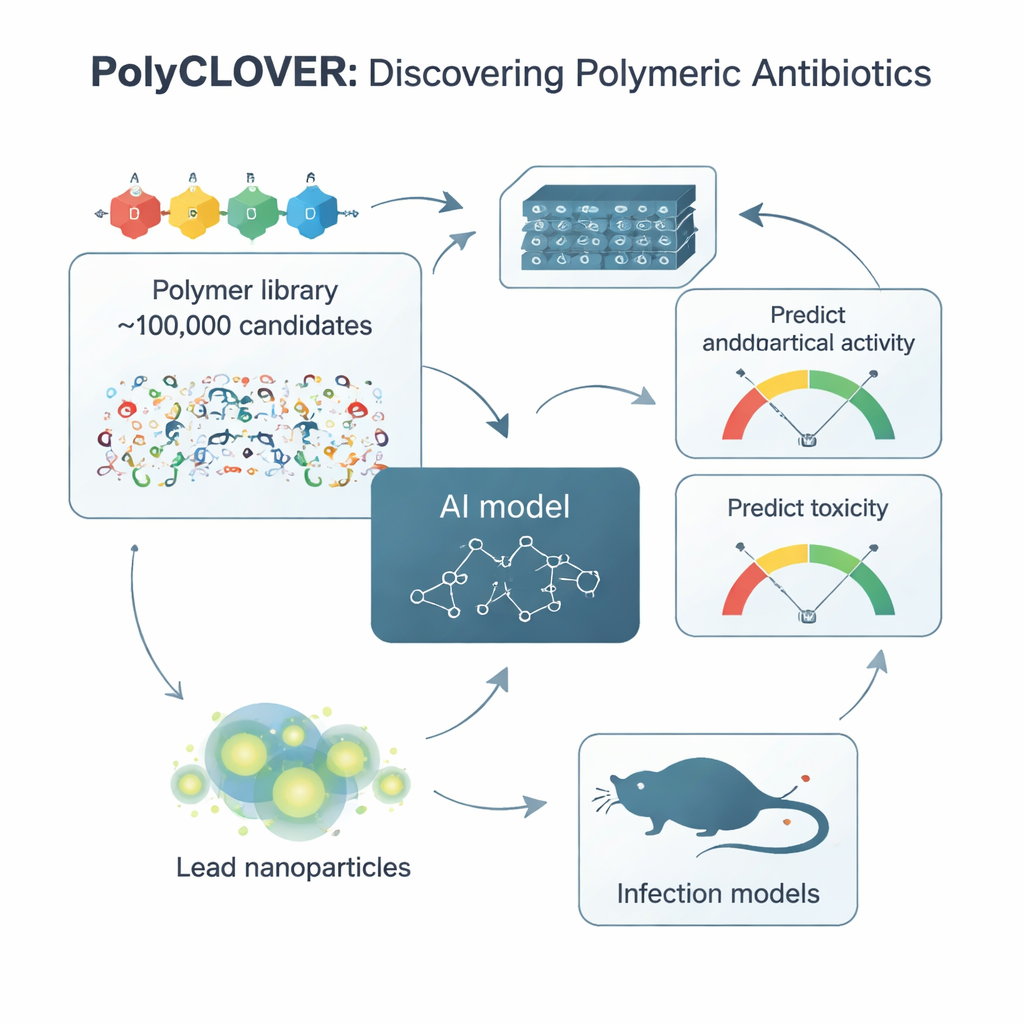
高分子の「ボディランゲージ」を読み取るAIを教える
このライブラリをナビゲートするために、チームはPolyCLOVERと呼ぶ枠組みを作りました。中核には各高分子を結合した原子のネットワークとして扱うグラフベースのニューラルネットワークがあり、構造の微妙な差異を感知できます。良好/不良の高分子についてラベル付きの例が非常に少なかったため、研究者らは多段階の自己教師あり学習戦略を採用しました。まず、約100万個のラベルなし高分子構造でモデルを訓練し一般的な化学パターンを捉え、次にラベルなしの10万メンバーのライブラリでさらに訓練し、最後に抗菌活性と赤血球への損傷について合成・試験済みの220種の小さなデータセットでファインチューニングしました。この段階的学習により、新しい高分子が強力かつ安全であるかを予測するモデル能力は飛躍的に向上しました。
実験とアルゴリズムがお互いから学ぶ仕組み
PolyCLOVERは一度の予測で終わりません。AIが最も有望かつ情報価値の高い候補を提案し、化学者がそれらを高スループットで合成・試験し、新しい結果をモデルにフィードバックして改良するループで動作します。選択ステップには「上側信頼限界(upper confidence bound)」の手法を用い、利用(うまく働くと予測される高分子を優先)と探索(モデルが最も学べる不確実な領域を探る)をバランスさせます。約4回の反復ラウンドを経て、提案された高分子は着実に改良され、メチシリン耐性黄色ブドウ球菌(MRSA)に対する効力が増しつつ、赤血球に対する許容できる毒性を維持しました。実験はわずか20日程度で収束し、少数の優れた候補が絞り込まれました。
細菌に穴を開ける自己集合する小さな粒子
最終的に選ばれた3つの主要高分子(H1、H2、H3)は自然に正に帯電した直径約100ナノメートルのナノ粒子を形成しました。in vitro試験では、これらは標準的な抗生物質ストレプトマイシンと同等にMRSAを殺し、しかもはるかに速く作用しました—タンパク質を多く含む血清中でも数分から数時間で細菌数を数桁減少させました。電子顕微鏡と蛍光プローブは、これらの粒子が細菌表面に素早く付着し、膜の一体性と電位を破壊して細胞内成分を漏出させることを示しました。重要なことに、MRSAをほぼ1か月にわたってこれらの高分子に曝露しても、細菌はほとんど耐性を獲得しませんでした。これは同期間に投与量が劇的に上昇したストレプトマイシンとは対照的です。
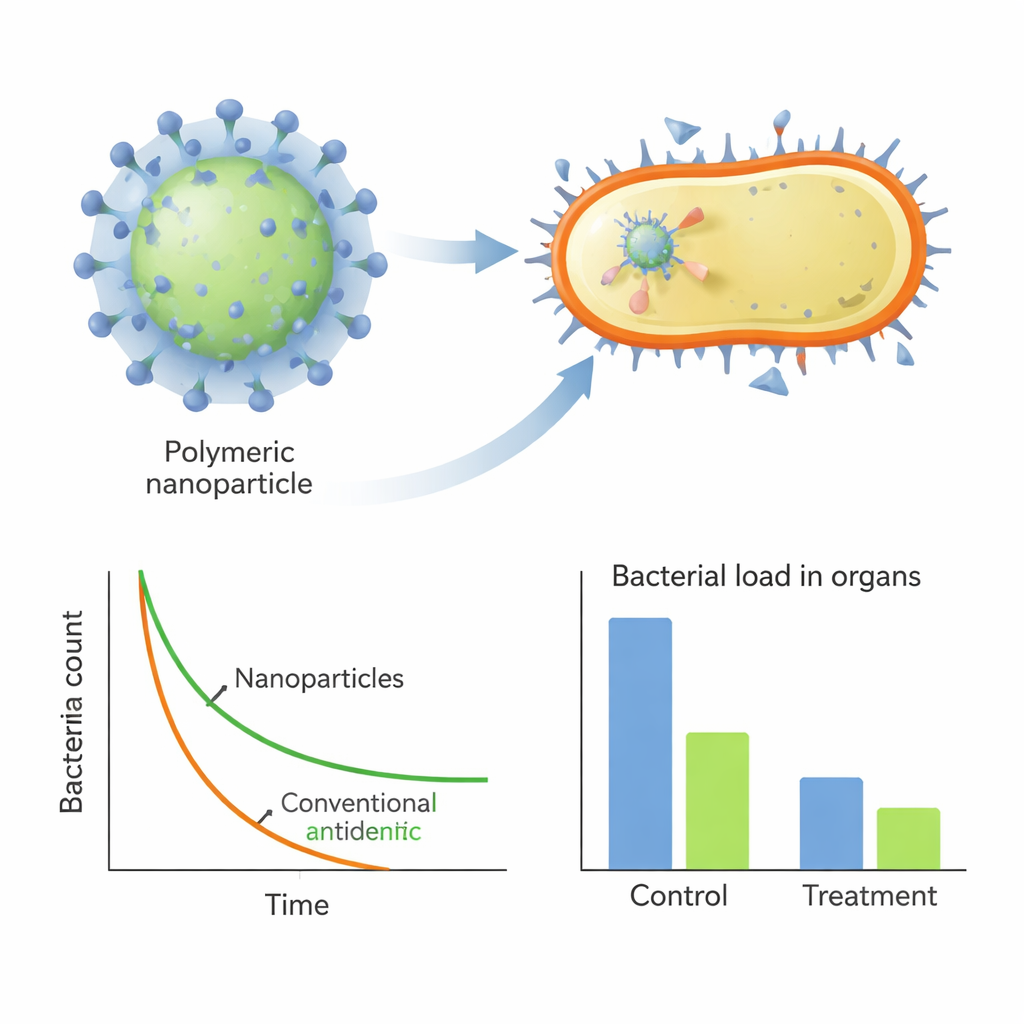
動物感染で古い抗生物質を再び効かせる
単独で作用するだけでなく、これらのナノ粒子は従来薬の強力な補助剤としても働きました。MRSAが通常強く耐性を示すペニシリンGと組み合わせると、最良の高分子(H2)は抗生物質を粒子内に閉じ込めるナノ複合体を形成しました。これらの複合体はin vitroで強い相乗効果を示し、MRSAを抑えるために必要なペニシリン量を大幅に減らしました。肺感染と重度腹部感染のマウスモデルでは、主要高分子(単独またはペニシリン併用)が臓器内の細菌量を大幅に減らし、血中の炎症シグナルを低下させ、組織損傷を抑え、明らかな毒性は見られませんでした。
より賢い抗生物質探索の新たな手引き
専門外の読者への要点は、PolyCLOVERがAIと自動化実験を組み合わせることで、従来よりはるかに速く全く新しいタイプの抗生物質を発見できることを示した点です。偶然と遅いスクリーニングに頼る代わりに、このアプローチは各バッチの結果から学習して、薬剤耐性細菌を攻撃すると同時に従来の抗生物質をより効果的に運搬する高分子に的を絞ります。これらの材料が臨床に到達するまでにはさらなる研究が必要ですが、本研究は耐性感染症に対する減少しつつある武器庫を補充する有望な道筋を示し、多くの他のスマートなバイオマテリアルを設計するための一般的な戦略を示唆します。
引用: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
キーワード: 抗菌薬耐性, 高分子抗生物質, ナノ粒子, 機械学習, 薬剤耐性細菌