Clear Sky Science · ja
Cas12aのブリッジヘリックスはRループ形成とRuvC活性化のアロステリック調節因子である
なぜ遺伝子編集に重要なのか
新しい治療法や迅速な診断検査の基盤となる強力な遺伝子編集ツールの多くは、標的とする場所でDNAを切断するCRISPRタンパク質に依存しています。しかし、これらの分子ハサミが誤った箇所を切断すると、有害な副作用を引き起こす可能性があります。本研究はCas12a編集酵素の内部にある小さな可動部位、ブリッジヘリックスを詳しく解析し、その形状変化が正しい標的認識とDNA切断を結びつける内部の安全スイッチのように機能することを示しています。このスイッチを理解することで、医療やバイオテクノロジー用途でより正確かつ安全なCRISPRツールを設計するための指針が得られます。
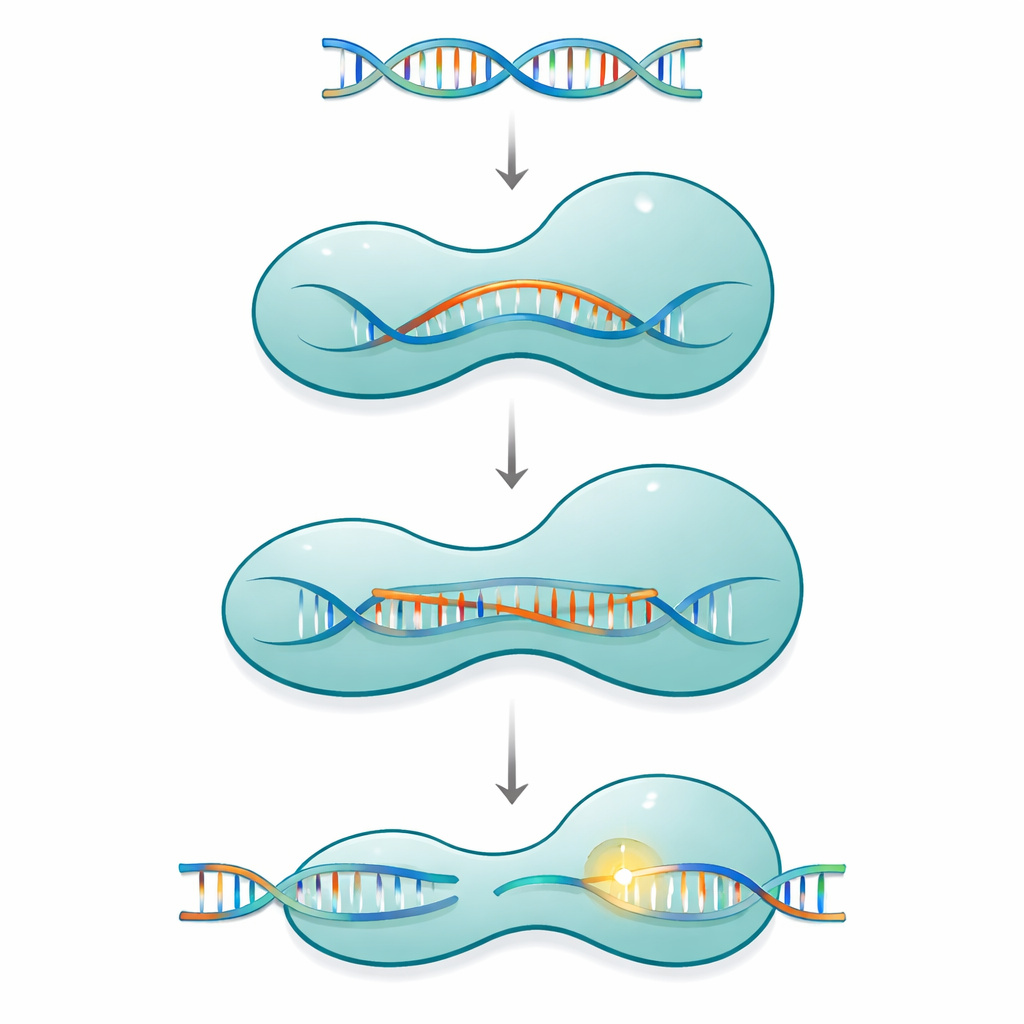
可動部を備えた分子クランプ
Cas12aは単一タンパク質で構成されるCRISPR系に属し、短いガイドRNAを使ってウイルスや細胞ゲノムの一致するDNAを見つけて切断します。タンパク質は二本のアームを持つクランプのような形をしており、配列を確認する認識側と化学的切断装置を収める切断側に分かれます。これら二つの半分は、ブリッジヘリックスと呼ばれる細く正に帯電したセグメントでつながっています。Cas12aがガイドRNAに結合し、その後DNA標的に結合する過程で、タンパク質は剛直な道具として振る舞うわけではありません。むしろ、Rループとして知られる増大するRNA–DNAハイブリッドを徐々に取り囲むように、大きな形状変化と小さな形状変化の連続を経ていき、十分な塩基対が形成されて初めて切断部位が完全に活性化します。
内蔵安全スイッチの探査
研究者らは細菌Francisella novicida由来のCas12aと、ブリッジヘリックス中の二つのアミノ酸をプロリンに置換した既存の設計変異体に注目しました。プロリン置換はヘリックスを硬くしたり断片化したりすることで知られ、この変異体(FnoCas12aKD2P)は天然型よりも選択的に切断する一方で反応が遅くなります。クライオ電子顕微鏡を用いて、ガイドRNAと標的DNA断片に結合したこの変異体の5つの異なる構造スナップショットを捉えました。これらは、初期のDNA認識段階から、RNA–DNAハイブリッドの一部が形成されているが完全な切断準備が整っていない後期の状態まで、活性化経路に沿った異なる段階を示しています。
形状変化が精密な切断を駆動する仕組み
変異体と既に決定されている通常のCas12a構造を比較すると明確なパターンが現れました。天然型では、ブリッジヘリックスの一部がゆるいループからより長く直線的なヘリックスへと変化し、成長するRNA–DNAハイブリッドに向かって曲がり、密接に接触します。同時に、切断ドメインの隣接するヘリックスが緩み、通常は活性部位をふさぐ小領域「リッド(蓋)」がループからヘリックスへと変わり開く方向へ回転します。これらの協調運動がポケットを開き、一本鎖DNAが入り込んで切断されます。プロリン含有変異体では、ブリッジヘリックスがこのループ→ヘリックス変換や適切な曲がりを完全に実行できません。その結果、RNA–DNAハイブリッドは歪んだまま遠ざかり、リッドは閉じたループ状のまま留まり、複合体は完全な触媒前構造に到達することがまれになります。この機械的なボトルネックが標的での切断を遅らせ、不一致を含むDNAが内部チェックポイントをすり抜けるのを困難にします。
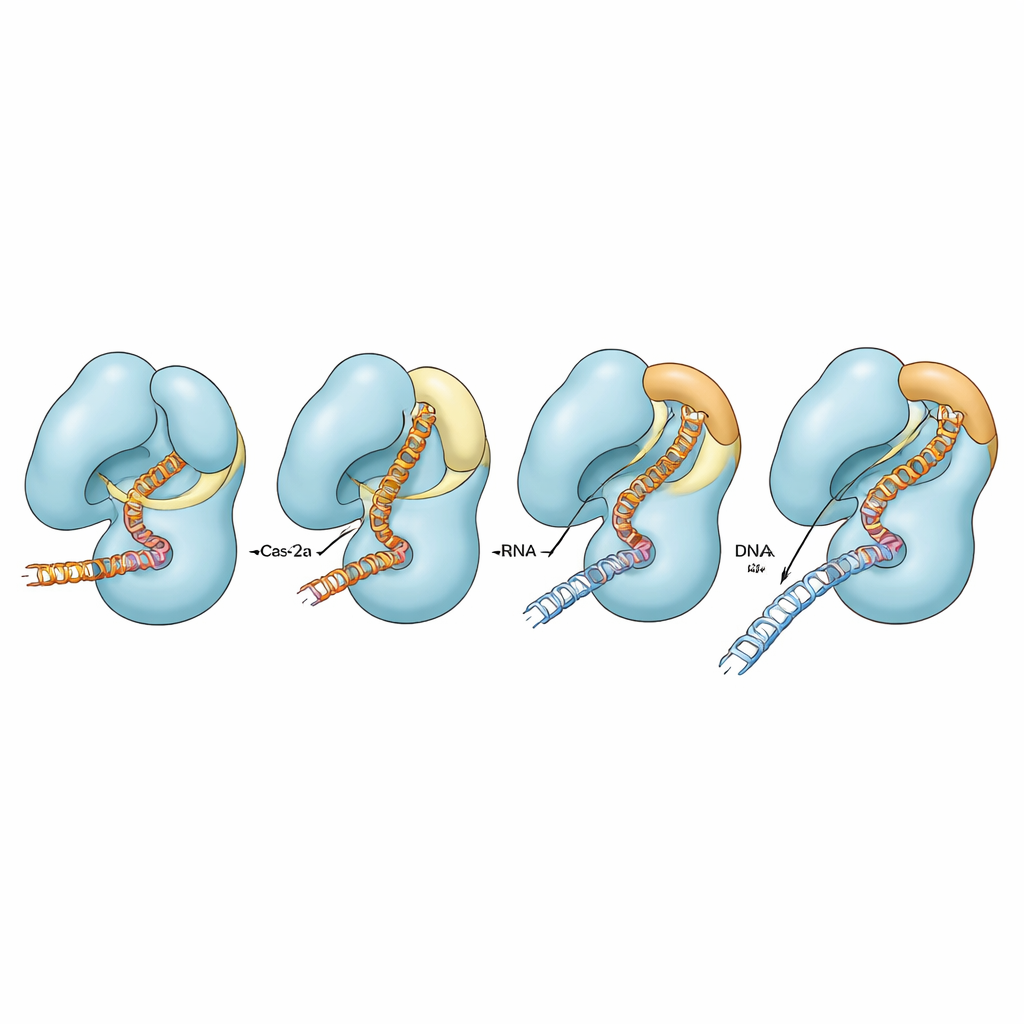
接触部を調整して精度を微調整する
著者らはリッドとブリッジヘリックス周辺のさまざまな接触が活性にどう寄与するかを試すため、これらの領域をつなぐ特定の帯電残基を変えました。通常のCas12aでは、これらの接触を壊しても完全に一致するDNAの切断には大きな影響はほとんどありませんでしたが、一部の条件では不一致がある場合の第二鎖の切断効率に影響が出ました。しかし、機能が損なわれたブリッジヘリックス背景では、同じ置換が二本鎖の切断を著しく低下させ、特にガイドとDNAが完全には一致しない場合にはほぼ消失させました。計算機シミュレーションもこれを支持し、ブリッジヘリックスが完全にヘリックス形状を取れる場合に限り、ブリッジ、隣接ヘリックス、リッド、および核酸が強く協調した動きを示すことを示しました。ヘリックスが損なわれると、これらの運動は部分的または完全に連動しなくなり、酵素は触媒サイクルを完了するのに苦労します。
次世代CRISPRツールのための設計指針
総じて、この研究はブリッジヘリックスがRNA–DNAハイブリッドの長さと品質をCas12aの切断ポケットの開口に結びつける内部制御レバーであることを明らかにしました。タンパク質に切断前に特定の一連の形状変化を完了させることを強いることで、この仕組みは不一致の識別を自然に強制します。この知見は、ブリッジヘリックスの小さな領域を標的にした改変が、オフターゲット切断や“コラテラル” DNA活性を低減するCas12a変異体を生む理由を説明する助けとなり、より安全なゲノム編集や診断向けの特性をもたらします。より広くは、短いヘリックスの微妙な変化が大きな分子機械内での長距離コミュニケーションをいかに調整するかを示し、高忠実度の核酸処理酵素を設計するための一般原理を提供します。
引用: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
キーワード: CRISPR-Cas12a, 遺伝子編集の精度, ブリッジヘリックス, Rループ形成, アロステリック調節