Clear Sky Science · ja
NeoPrecis: 質的な免疫原性とクローン性を考慮したネオアンチゲン全景の統合による免疫療法反応予測の向上
なぜ一部のがんは免疫療法に反応し、他はしないのか
免疫療法はがん治療を一変させましたが、多くの患者は未だ恩恵を受けられず、一部には重篤な副作用が出ることもあります。大きな疑問は、なぜある腫瘍は免疫系に認識されて破壊されるのに対し、別の腫瘍はやり過ごされてしまうのかという点です。本研究はNeoPrecisという計算手法を紹介します。これは腫瘍が免疫系に示す“目印”であるネオアンチゲンをより精緻に解析し、その情報を用いて現代の免疫療法に反応しやすい患者をより正確に予測することを目指します。
がん細胞に現れる新しい目印
がん細胞はDNA変異を蓄積してタンパク質の構成を変えることがあります。これら変化したタンパク質の短い断片、ネオアンチゲンは細胞表面に提示され、T細胞――免疫系の実行部隊――に異物として認識され得ます。長年、臨床では腫瘍変異負荷(tumor mutation burden:変異の総数)のような粗い指標を用いて、チェックポイント阻害薬に対する反応性を推定してきました。しかしそれは粗雑な道具です:すべての変異がT細胞にとって可視的かつ魅力的な標的を生むわけではなく、腫瘍は多様な細胞亜種の寄せ集めであることが多いからです。NeoPrecisは単に変異数を数えることを越え、腫瘍全体にわたって真に有望な標的がどれだけ存在するかを評価するよう設計されました。
三つの重要な要素を同時に見る
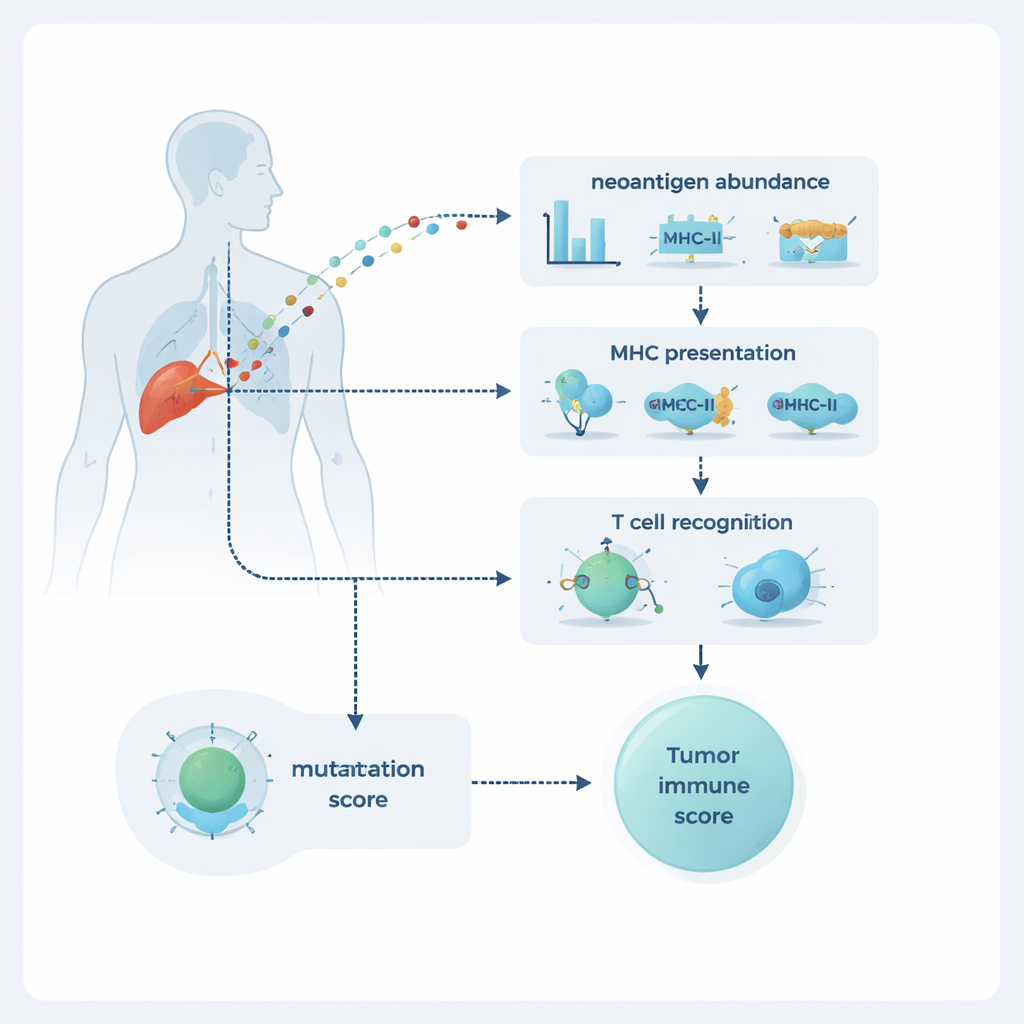
NeoPrecisは各変異を三つの次元で評価します:腫瘍内での豊富さ(存在頻度)、細胞表面に提示される可能性(提示能)、そしてT細胞に認識される可能性(免疫原性)。豊富さはDNAおよびRNAシーケンシングから推定され、変異がどれほど広く存在し、どれほど強く発現しているかを示します。提示はMHCクラスIおよびクラスIIと呼ばれる分子への結合を通じてモデル化され、これらはT細胞にペプチド断片を見せる掲示板のように機能します。最も新しい要素はT細胞認識のコンポーネント、NeoPrecis-Immunoです。このモデルは既知のT細胞–ペプチド相互作用の大規模データベースから学習し、変異断片が正常な対応断片からどれだけ異なっているか(T細胞認識にとって重要な差)を評価するとともに、個々人が持つ特定のMHC多型も考慮します。
T細胞が「見る」ものをコンピュータに教える
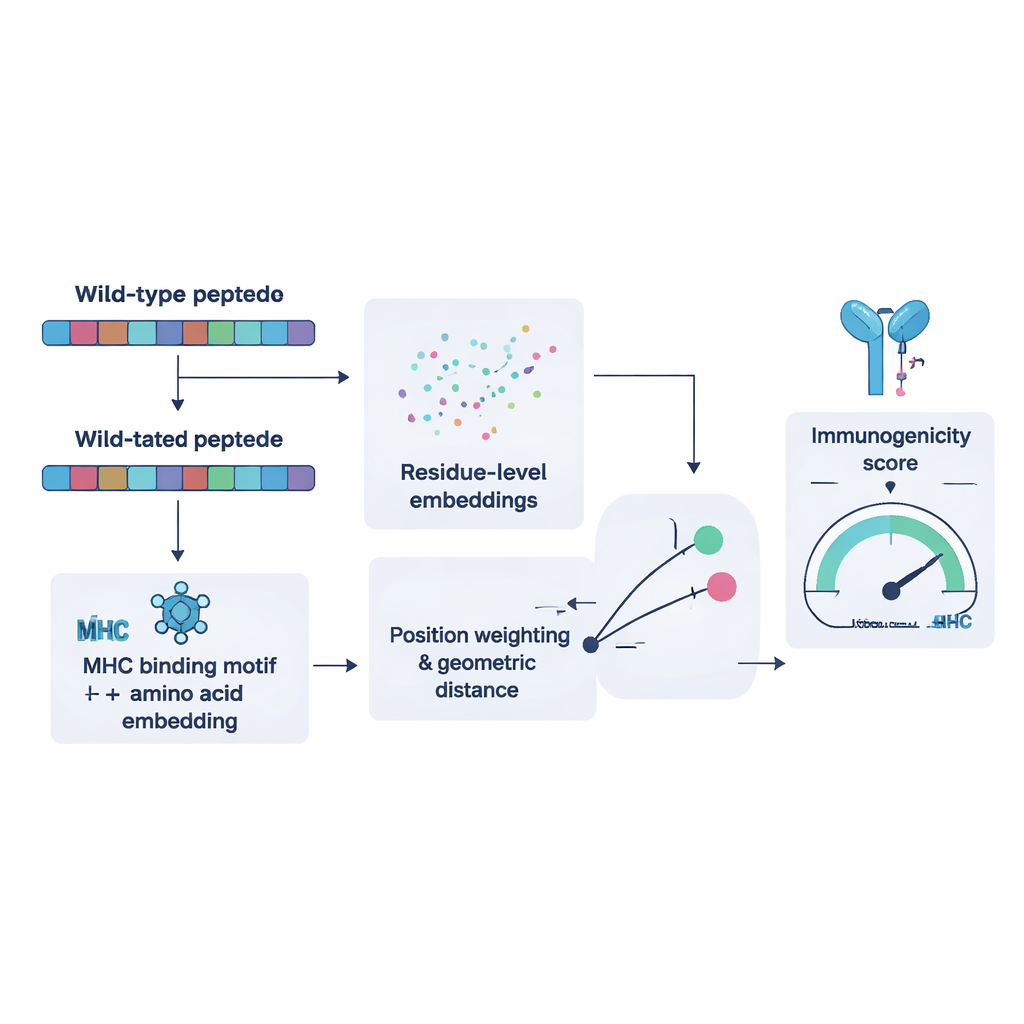
NeoPrecis-Immunoを訓練するために、研究者らはまず同じT細胞が複数の類似ペプチドを認識する例と認識しない例を何千も集めました。これらを用いて、変異断片が正常断片に非常に似ている場合はT細胞応答を引き起こしにくいことをモデルに学習させました。これは自己類似な標的はT細胞の発達過程で通常除外されるためです。モデルは各ペプチドをアミノ酸配列と個人のMHC分子の結合嗜好によって形作られる数学的空間の一点として表現します。次に変異ペプチドが元のペプチドからどれだけ離れているかを測ります。より大きくモチーフに依拠した距離は免疫原性が高い可能性に対応します。独立したがんデータセットで既存のツールと比較したところ、NeoPrecis-Immunoは特にヘルパーT細胞に提示され、抗腫瘍応答の支援と維持を担うMHCクラスIIにおいて優位か同等の性能を示しました。
単一の変異から腫瘍全体へ
個々の変異は物語の一部に過ぎません。それらが腫瘍内でどのように分布しているかも重要です。ある変異はほぼすべてのがん細胞に見られる「クローナル(全般的)」であり、他は特定の領域にのみ存在する「サブクローナル(亜系)」です。NeoPrecisは各変異の免疫原性スコアを合算し、それらがどのサブクローンに属し、そのサブクローンがどれほど一般的かという情報を重ね合わせることで「ネオアンチゲン地形」を構築します。これにより、強力で広く共有されるネオアンチゲンが豊富な腫瘍、特にMHCクラスIとクラスIIの両方で提示され得て、ヘルパーT細胞とキラーT細胞の協調した応答を誘導できる可能性のある腫瘍を強調する腫瘍レベルのスコアが得られます。メラノーマや非小細胞肺がんのチェックポイント阻害薬治療患者群では、これらNeoPrecisに基づくスコアは標準的な変異カウントよりも反応者と非反応者を正確に区別し、特に複雑で異質な肺腫瘍において有用でした。
患者にとっての意義
患者にとってNeoPrecisの期待は、免疫療法を利益を得やすい人により精緻に適合させることと、なぜ一部の腫瘍が治療に抵抗するのかをより明確に理解することです。ネオアンチゲンの量だけでなく質と分布に注目することで、類似した変異負荷を持つ腫瘍がなぜ大きく異なる振る舞いを示すのかを説明する助けになります。将来的には、このような腫瘍の免疫可視化地図が、チェックポイント阻害薬の使用指針となるだけでなく、個々のがん内で最も強力かつ広く共有される標的を優先する個別化がんワクチンの設計にも貢献する可能性があります。
引用: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
キーワード: がん免疫療法, ネオアンチゲン, 腫瘍の異質性, チェックポイント阻害薬, 計算腫瘍学