Clear Sky Science · ja
NR6A1は神経堤細胞の指定、形成、生存に不可欠である
初期の細胞決定が顔と体をどう形作るか
私たちが生まれる前、神経堤細胞と呼ばれる特殊な細胞群が胚内を移動して顔、心臓、神経などを形作るのに寄与します。これらの細胞が正しく機能しないと、深刻な先天異常が生じることがあります。本研究は、NR6A1というタンパク質という、神経堤細胞が哺乳類の胚でいつどこで形成されるかを決めるのに関わる、これまであまり注目されてこなかった分子スイッチを明らかにし、このスイッチが失敗したときに何が起きるかを示します。
胚の“放浪する建築者”
神経堤細胞は発生の非常に早い段階で、形成中の脳と脊髄の境界沿いに生じます。この組織から離脱した後、彼らは長距離を移動して、顔面の骨や軟骨から末梢神経系の一部、皮膚の色素細胞に至るまで、多様な構造を作り出します。多くの器官に寄与するため、形成過程のわずかな乱れでも、Treacher Collins症候群のような頭顔面奇形を含む広範な疾患群、いわゆる神経堤病(ニューロクリストパシー)を引き起こす可能性があります。したがって、これらの細胞が最初にどのように現れるかを理解することは、正常な発生と先天異常の両方を説明するうえで極めて重要です。
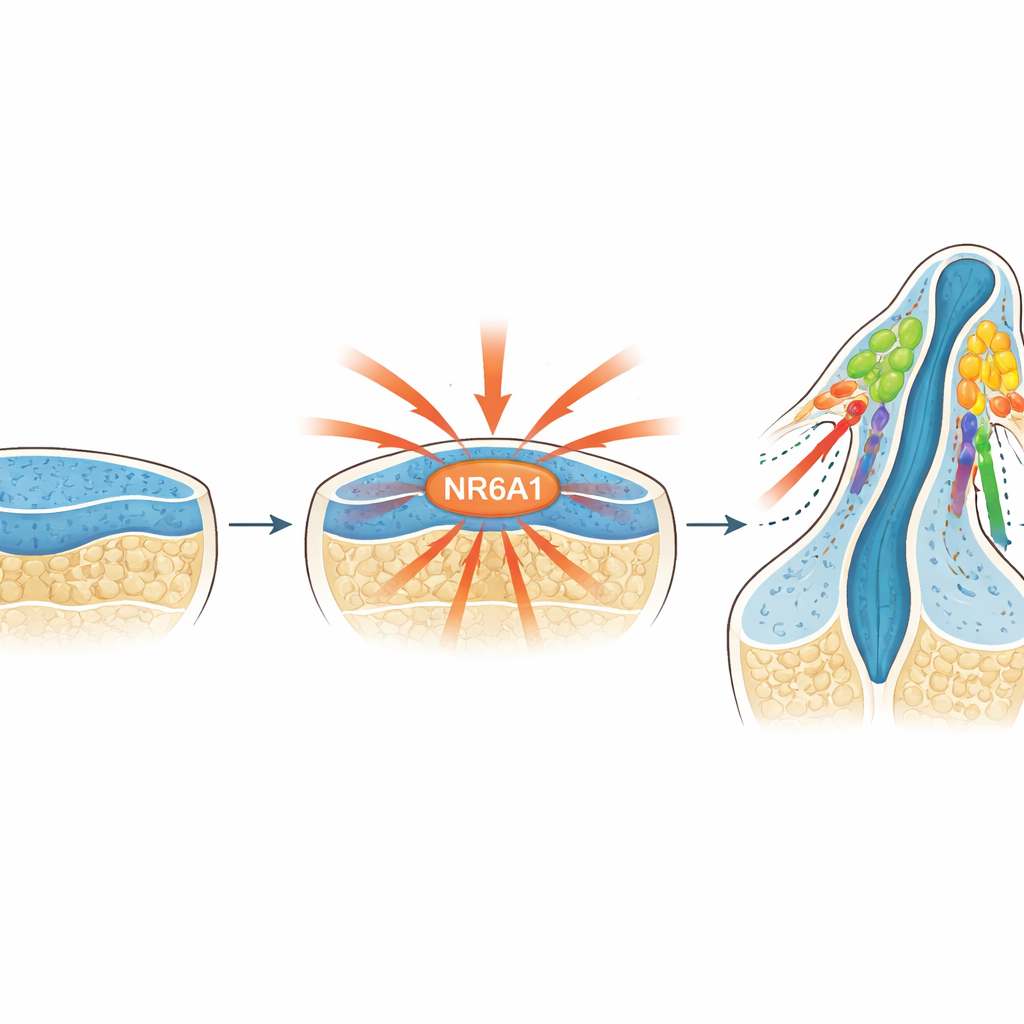
新たに認識されたマスタースイッチ
研究者たちはNR6A1に注目しました。NR6A1は遺伝子活性を制御する核内受容体ファミリーの一員です。以前の研究はNR6A1が頭部や顔面の欠損に関与する可能性を示唆していましたが、神経堤細胞におけるその役割は不明でした。着床直後からのマウス胚でNR6A1を追跡したところ、その存在は神経堤細胞が通常生じる場所と時期に緊密に一致しました。NR6A1は初期の神経組織に現れ、発生中の脳と脊髄の背側に濃縮し、この組織を離れて移動を開始する直前の細胞にも見られました。
スイッチが欠けると何が起きるか
NR6A1を完全に欠くマウスは発生の早い段階で致死となるため、研究チームはその直前の胚を解析しました。彼らは神経堤細胞が著しく不足していることを観察し、特に顎や頸部の一部を形成する第一鰓弓の背後で、移動性の神経堤細胞がほとんど存在しないことが分かりました。通常は神経堤の同定と細胞の剥離・移動を可能にする重要な遺伝子プログラムが大幅に低下していました。一方で、細胞を幹のような高増殖状態に保つ遺伝子はオンのままで、多くの神経堤様細胞は形成されてもすぐに死んでしまいました。これらの結果は、NR6A1がないと神経幹細胞が移動性の神経堤細胞へ適切に移行できず、生存できないことを示しています。
多能性をオフにし、移動性をオンにする
NR6A1がどのようにこの制御を行うかを理解するため、著者らはシングルセルRNAシーケンシング、クロマチンアクセシビリティ解析、ターゲットを絞ったDNA–タンパク質結合アッセイなど、いくつかの強力な分子手法をマウスおよびヒトの幹細胞由来神経堤細胞で組み合わせました。NR6A1は、相反する2つのプログラムを支配する遺伝子の近傍にある特定のDNAモチーフに物理的に結合することが分かりました。1つは多能性(多様な細胞型になれる能力)を維持するプログラム、もう1つは神経堤の同一性と細胞移動を駆動するプログラムです。NR6A1が存在すると、Oct4やNanogのような幹性遺伝子を取り巻くクロマチンはよりアクセスしにくくなり、これらの遺伝子は抑えられます。一方、神経堤や上皮間葉転換に関わる遺伝子近傍の領域はより開いて活性化されます。神経堤形成の重要な窓でOct4を過剰発現させるとNR6A1欠失を模倣し、多能性を消すことが神経堤細胞出現に必須であることをさらに示しました。
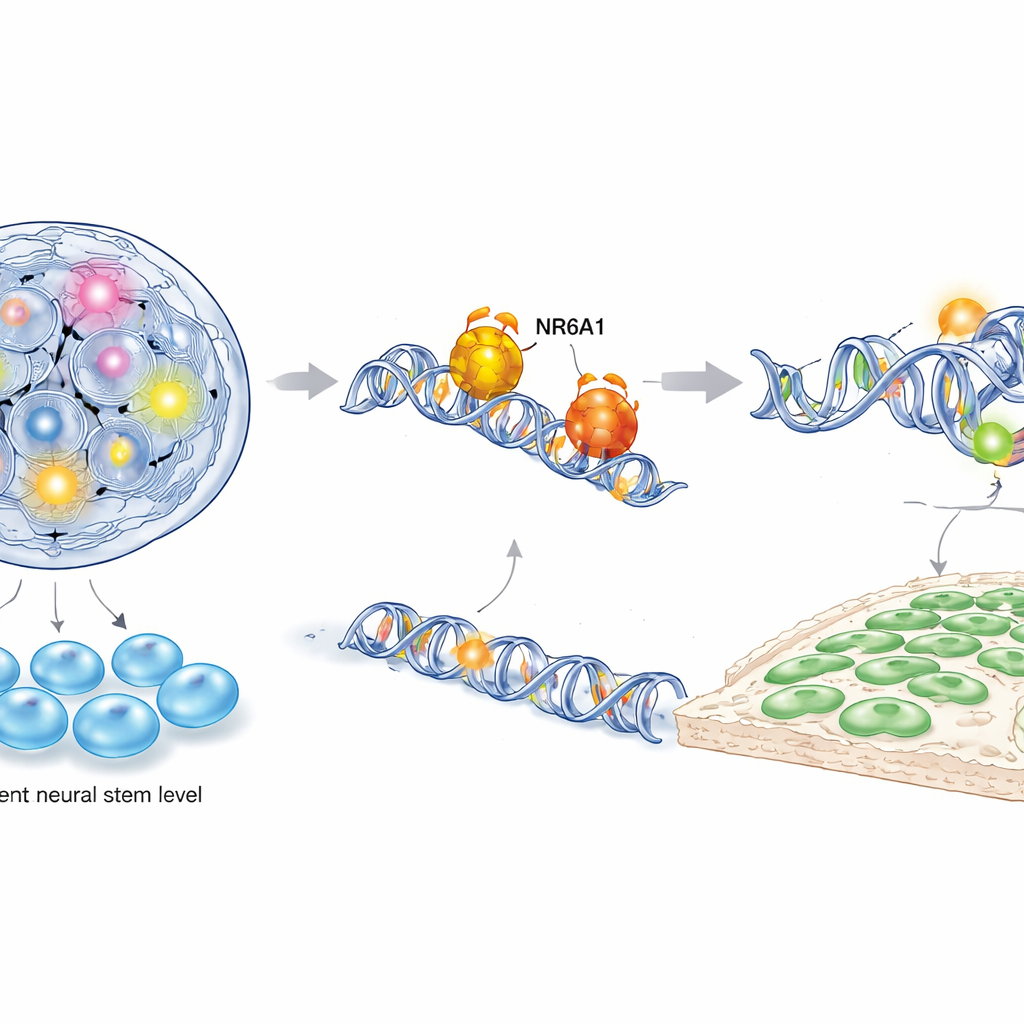
初期発生のタイムラインを書き換える
この研究はまた、哺乳類で神経堤細胞がいつ指定され始めるかの時間表を改訂します。誘導性の遺伝学的システムを用いて異なる時期にNR6A1を削除したところ、中期原腸形成期までにこれを削除すると—従来考えられているよりも早い段階で—神経堤遺伝子の活性化が阻害されることが示されました。対照的に、広く使われる神経堤特異的なドライバーラインを含め、より後の時期にNR6A1を削除しても明らかな欠陥は生じませんでした。これは、神経堤運命に関する重要な決定がこれらの標準的なツールが作動し始める前に行われていることを意味し、過去のいくつかのマウス研究が初期の必要性を見逃していた理由を説明します。
先天異常と病気にとっての意義
総じて、この研究はNR6A1を中心的な調整因子として明らかにしました。NR6A1は神経幹細胞が多能性プログラムを同時にシャットダウンし、移動と生存のプログラムをオンにすることで「大人になる」ことを助け、神経堤細胞へと導きます。この二重の作用は、従来考えられていたよりも早い中期原腸形成期に始まるようで、マウスの発生を他の脊椎動物とより近づけます。このスイッチがいつどのように働くかを明確にすることで、本研究は先行する遺伝学的実験の再解釈の枠組みを提供し、神経堤生物学を研究するためのより適切なツールの特定、そしてこの初期発生の決定が誤ることで生じる神経堤病(ニューロクリストパシー)の理解と最終的な予防につながる可能性を示します。
引用: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
キーワード: 神経堤細胞, NR6A1, 胚発生, 多能性スイッチ, 神経堤病(ニューロクリストパシー)