Clear Sky Science · ja
統合的な計算–実験フレームワークによる効率的なゲノム編集のためのMmeFz2-ωRNAシステムの設計
大きな医療課題に対する小さな遺伝子ハサミ
遺伝子編集はすでに疾患研究の方法を変えていますが、安全で実用的な医療に転換するには依然として大きな課題があります。最大の障壁の一つは、CRISPR–Cas9のような現在最も強力な“DNAハサミ”が物理的に大きく、患者に使われる小さな輸送手段に詰め込むのが難しいことです。本研究は、Fanzor2と呼ばれるあまり知られていない酵素群に由来する新しい小型の遺伝子編集ツールを紹介し、人工知能がそれを迅速に再設計して将来の遺伝子治療の有望候補に仕立て上げる方法を示します。
コンパクトな新しいクラスの遺伝子編集酵素
現在の多くのゲノム編集酵素、例えばCas9やCas12aは、千個以上のアミノ酸から成る大型タンパク質です。その大きさが、遺伝子治療の主要な輸送手段であるアデノ随伴ウイルス(AAV)に詰めるのを難しくしています。対照的にFanzor2タンパク質はずっと小さく、動物や人間を含む真核生物に自然に存在します。著者らはこのファミリーの一員であるMmeFz2に着目しました。MmeFz2はωRNAと呼ばれる短いRNAを用いて特定のDNA配列を見つけて切断します。理論上はMmeFz2は小型でプログラム可能なため治療に理想的に見えましたが、実際にはヒト細胞での活性は低く、標的サイトの1%未満しか編集できませんでした。チームはこの性能不良な酵素を実用的なツールに変えることを目指しました。
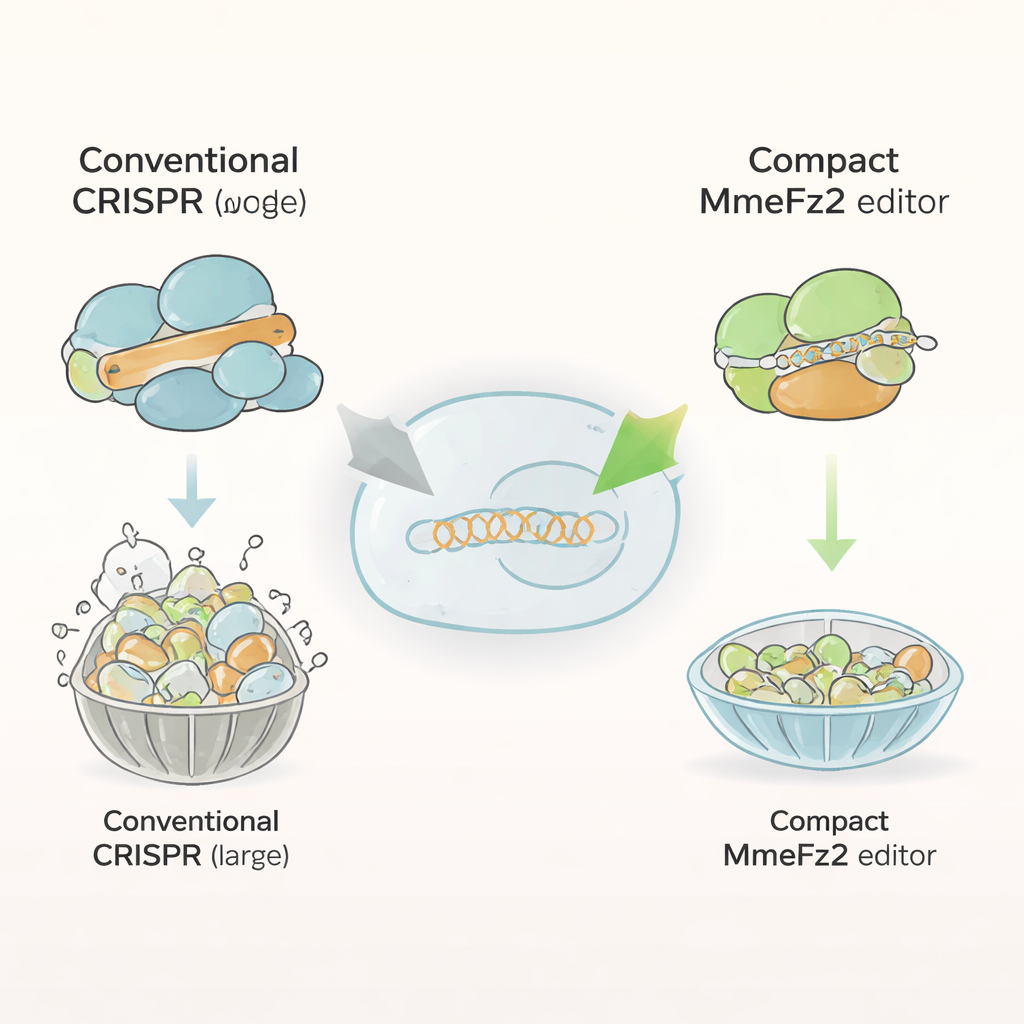
ガイド分子をAIで再設計する
最初の標的はωRNA、すなわちMmeFz2に切断位置を指示するガイドでした。研究者たちはAlphaFold3という、タンパク質–RNA–DNA複合体の三次元構造を予測する最先端プログラムを用いて、MmeFz2がωRNAとDNA標的に結合したモデルを構築しました。この仮想構造から、ωRNAの一部が不安定で対合が弱く、タンパク質とほとんど接触していないことが明らかになりました。その情報をもとに、チームは系統的に不安定な結合を置き換え、転写の妨げとなる可能性のあるウリジンの長い連続配列を除去しました。次に数十の変異体をヒト細胞で試験し、最良の変更を組み合わせ、不要な茎領域を切り詰めることで、サイズを30%短縮しつつ多くのDNAサイトでほぼ20倍の編集効率向上をもたらす短縮ωRNAを作り上げました。
機械学習でタンパク質を微調整
次にチームはタンパク質自体の改良に取り組みました。再びAlphaFold3を用いてMmeFz2がRNAやDNAと接する部位をマップし、接触を強化したり柔軟性を改善したりすることを狙って100を超える単一アミノ酸変異を設計しました。これらを細胞でスクリーニングした後、性能データをEVOLVEproという機械学習システムに投入しました。EVOLVEproは何百万もの自然配列から学んだプロテイン言語モデルに基づくもので、どの特徴が活性を高めやすいかを学習し、さらに良く働くと予測される変異の組み合わせを提示しました。こうした計算–実験のループを数回繰り返すことで、改良されたωRNAと組み合わせると出発点に比べて編集活性を60倍以上に高める二つの最適化酵素バリアントに到達しました。
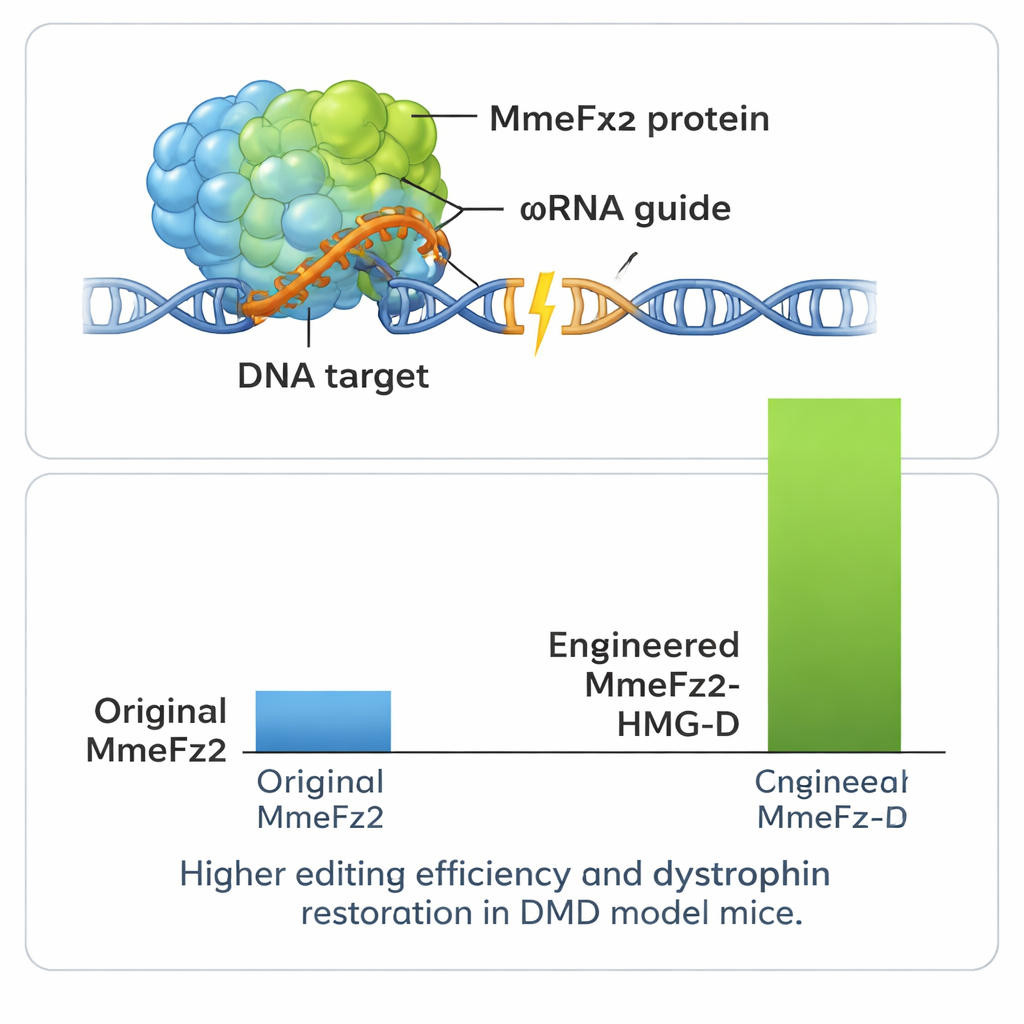
出力を高め、疾患モデルで検証する
システムの性能をさらに引き出すために、著者らはMmeFz2に遺伝子へ結合するのを助ける小さなDNA結合ドメインを融合しました。そのうちの一つ、HMG-Dと呼ばれるドメインは、設計した酵素の末端に結合させると特に効果的で、一部のサイトで80%を超える編集率を示しました。重要なことに、予測されるオフターゲット部位での検査は、この出力増強が精度の大幅な低下を伴わないことを示しました。タンパク質とガイドRNAを含めた編集複合体全体が非常にコンパクトであるため、単一のAAVベクターに十分収まる点は多くのCRISPRシステムでは不可能な利点です。チームはこの利点をデュシェンヌ型筋ジストロフィーのマウスモデルで実証しました。この致命的な筋萎縮疾患はジストロフィン遺伝子の欠陥によって引き起こされます。脚筋への一回のAAV注入により、遺伝子のRNAに可検出な修復が生じ、相当数の筋繊維でジストロフィンタンパク質が回復しました。
将来の遺伝子療法にとっての意義
非専門家向けの要点は、著者らが弱くてあまり注目されていなかった遺伝子切断酵素を、単一のウイルスパッケージで送達でき、現実的な動物モデルで深刻な遺伝病を修復できるコンパクトで高性能な編集酵素に変えたことです。同様に重要なのは、その到達方法です。AIベースの構造予測と機械学習を実験に緊密に組み合わせることで、タンパク質とそのガイドRNAの両方を従来の手探り的手法よりはるかに効率的に改良しました。この統合戦略は次世代の多くのゲノム編集酵素の創出を加速し、筋ジストロフィーや他の遺伝性疾患の患者に対して、より正確で安全な遺伝子治療をより早く届ける可能性を高めます。
引用: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
キーワード: 遺伝子編集, CRISPRの代替, デュシェンヌ型筋ジストロフィー, ウイルス遺伝子治療, 生物学における人工知能