Clear Sky Science · ja
展開状態を明示的に考慮したタンパク質折りたたみ安定性の推定
なぜタンパク質の安定性が重要か
体内のすべてのタンパク質は、適切に機能するために正確な三次元形状に折りたたまれる必要がある小さな分子機械です。その折りたたみが脆弱だと、タンパク質は誤作動したり、凝集したり、まったく産生されなくなったりします――これらは疾病やタンパク質ベースの医薬品や酵素の製造失敗と関連します。実験室でタンパク質の安定性を測るのは時間がかかり難しいため、研究者たちは配列だけからタンパク質がどれほど容易に展開するかを信頼性高く予測できる計算手法を探しています。
折りたたまれた状態と展開状態を新たに見る
現在の多くのアルゴリズムは、タンパク質の折りたたまれた形状にほとんど注目しています。多くはAlphaFoldのようなAIが予測した単一の構造を出発点とし、その構造を安定性の主要な決定因子として扱います。しかし、安定性とは本質的に二つの広い集合体間のエネルギー差、すなわちコンパクトな折りたたまれた状態と多様で柔軟な形状をとる展開状態の差です。著者らは、展開側を無視することが、既存のツールが実験で測定される折りたたみ自由エネルギー(ΔG)に一致しない主な理由であると論じています。
両方の状態を学習する新しいモデル
研究者たちはIFUMという、ΔGを推定しつつ各タンパク質における折りたたまれた状態と展開状態のバランスを学習するディープラーニングシステムを導入します。展開状態を漠然とした背景として扱う代わりに、IFUMは高分子物理学の概念を用いてそれを「ランダムコイル」として表現し、折りたたまれた状態と展開状態の両方をアミノ酸対間の距離のマップとして符号化します。モデルは大規模な事前学習済み配列・構造ネットワークからの情報を取り込み、全体の安定性と、各残基対においてどれだけの集団が折りたたまれているか、あるいは展開しているかを示す確率マップを共同で予測します。多数の小さな実験的に特徴付けられたタンパク質と既知の無秩序タンパク質を含む非常に大きなデータセットでの学習により、IFUMはよく構造化された配列と柔らかい配列の両方を識別できます。
より良い数値と広い変異対応範囲
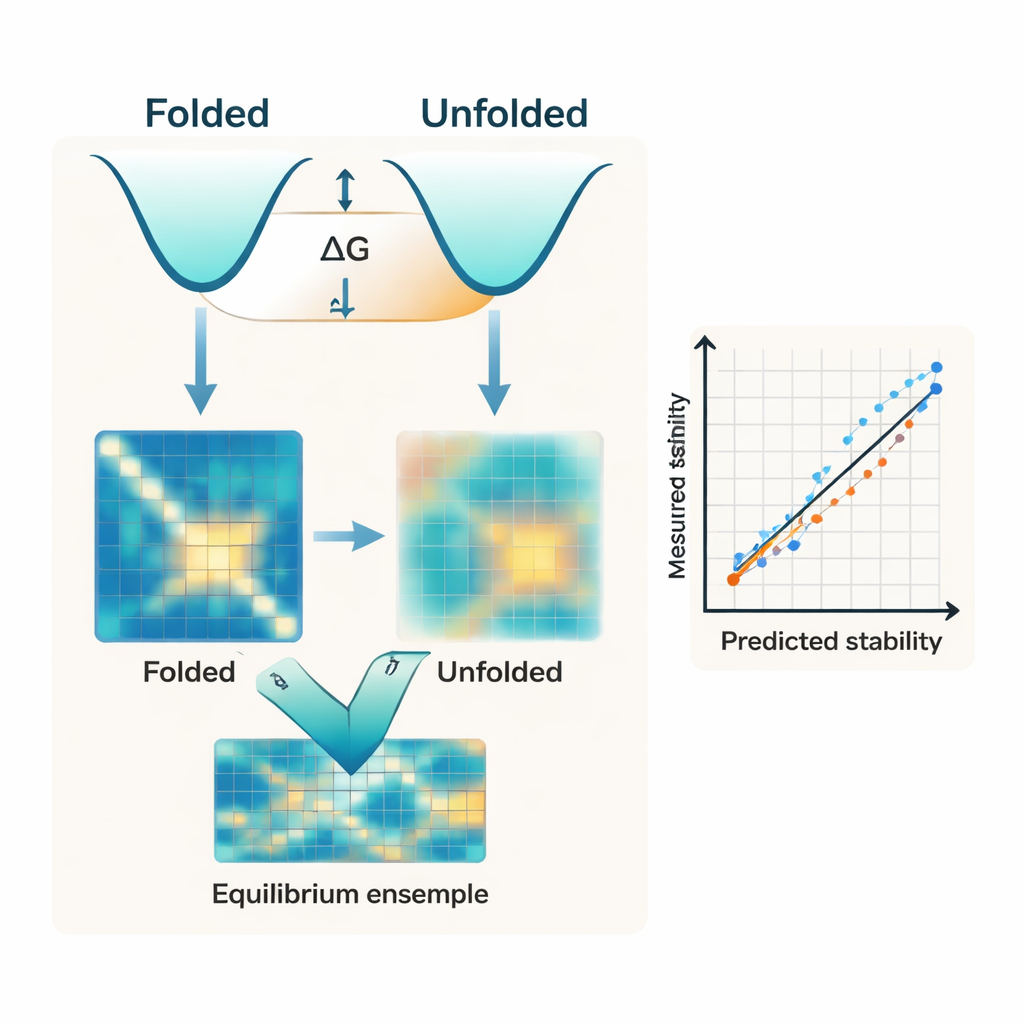
慎重に制御された小タンパク質のデータセットで評価したところ、IFUMは折りたたまれた構造だけに依存する従来のAI手法や配列に基づく言語モデルよりも、実験的なΔG値をより低い誤差で高い相関をもって予測しました。重要なのは、モデルが幅広い配列変化にも対応できる点です。単一および二重の点変異だけでなく、タンパク質長を変える挿入や欠失の影響も正確に捉えており、これらは多くの既存ツールが失敗するか、そもそも設計されていない状況です。内部比較では展開状態の目的関数を取り除くと性能が著しく悪化することが示されており、展開集合を明示的にモデル化することは概念上のこだわりではなく、予測精度の中心であることが強調されています。
設計ベンチから実世界の検証へ
IFUMが実際のタンパク質工学に役立つかを確かめるため、著者らはIFUMを三つの困難な設計課題に適用しました:インターフェロンλタンパク質の安定化、免疫シグナルタンパク質IL‑10の形状変換、そして糖修飾酵素UGT76G1の改良です。これら三例すべてで、IFUMが予測した安定性は、タンパク質が熱によってどれだけ変性しにくいかを示す融解温度の測定値と良く一致しました。モデルはまた、何百にもおよぶ完全に新しい計算設計されたタンパク質をスクリーニングして、細胞内で正しく折りたたまり可溶である可能性が高いものを選抜するのに役立ち、構造予測ネットワークの一般的な信頼度スコアよりも優れた性能を示しました。これらの結果は、IFUMが現代のタンパク質設計ワークフローにおいて、構造ベースのチェックと並んで実用的な「安定性フィルター」として用いられ得ることを示唆しています。
限界と今後の方向
どのモデルにも限界はあります。IFUMは主に短く単一鎖で可溶性のタンパク質を中心に訓練されており、極めて大きいタンパク質や広範な柔軟ループ、膜貫通領域を持つタンパク質に対しては絶対的な安定性の数値は信頼性が低くなります。また、展開状態の記述は依然としてすべての可能な形状を完全に再現する実際的な描像ではなく、簡略化された統計モデルに留まります。それでも、折りたたまれた集合と展開した集合の双方を考慮するようAIに学習させるアプローチが、より信頼できる安定性推定をもたらすことを示しています。非専門家にとっての重要な結論は、IFUMにより「このタンパク質設計は本当に崩れずに保てるか?」と定量的な自信をもってコンピュータに問える可能性が近づき、安全なバイオ医薬品やより堅牢な産業用酵素の開発を加速する助けになる、という点です。
引用: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
キーワード: タンパク質安定性, タンパク質折りたたみ, ディープラーニング, タンパク質設計, 変異