Clear Sky Science · ja
G9aを介したH3K9me2は細胞周期関連遺伝子のエピジェネティックサイレンシングを通じて腸上皮の再生を調整する
腸の自己修復が重要な理由
腸の内膜は毎日、胃酸や食べ物の粒子、そして数兆もの微生物という過酷な環境にさらされています。それでもこの組織は生き延びるだけでなく、常に自らを修復しています。その修復機構が放射線療法後、炎症性腸疾患、あるいは重篤な感染症の際に破綻すると、痛み、出血、生命を脅かす合併症を招くことがあります。本研究は、腸細胞が休止から再生へ切り替えるタイミングを決める隠れた「スイッチ」を明らかにし、腸の自然な修復を強化する新しい治療法への手がかりを提供します。
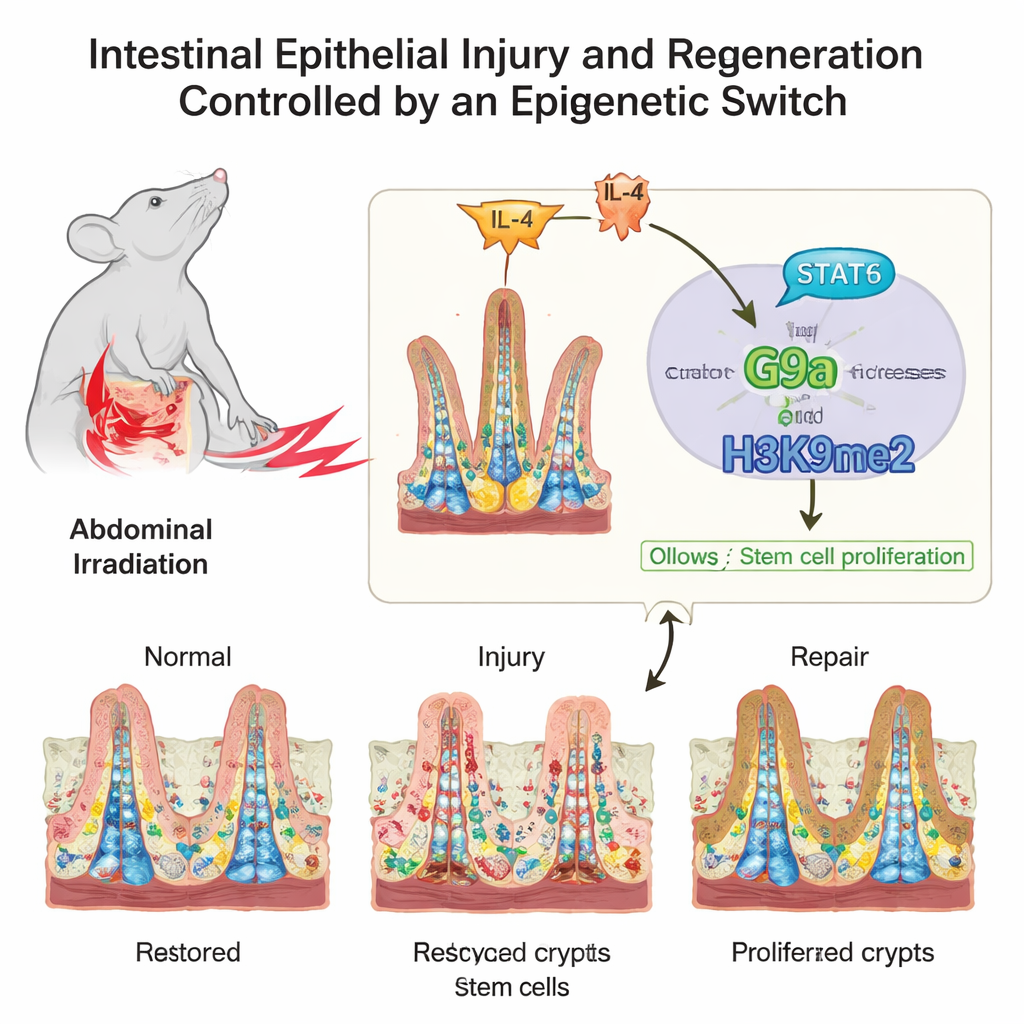
絶え間ないストレス下の繊細な構造
顕微鏡で見ると腸の内面は毛足の長いカーペットのようで、栄養を吸収する指状の絨毛と、幹細胞が存在するクレフト(crypt)という窪みがあります。これらの幹細胞とその速やかに分裂する子孫細胞は、安定した更新と緊急修復のバランスを保たねばなりません。著者らは、DNAを包むタンパク質であるヒストンに付く化学的なタグがこのバランスにどう影響するかに注目しました。これらのタグは遺伝子配列を変えるわけではなく、むしろ調光スイッチのように、腸が正常状態から損傷、そして回復へと移行する際に遺伝子群の活動を上下に調節します。
損傷と治癒を追うエピジェネティックマーク
研究者たちは、癌治療時の腸損傷の一般的原因である放射線にさらしたマウスを用い、幹細胞が豊富なクレフトで複数のヒストンマークをスキャンしました。その中でH3K9me2というマークが、腸が損傷から修復へと移る過程で顕著に増加しました。その付与酵素であるタンパク質G9aも同様の増加を示しました。研究チームは次に、骨盤部放射線療法を受けた患者やクローン病の患者からのヒトサンプルを調べました。いずれの状況でも、腸細胞におけるH3K9me2とG9aの高レベルは組織修復の良好な指標と一致し、この仕組みがマウスとヒトで保存されていることを示唆しました。
修復スイッチが壊れたとき
このマークが単なる随伴現象か治癒を駆動する実因かを検証するため、科学者たちはマウスの腸上皮からG9aを特異的に除去するか、その活性を薬剤で阻害しました。どちらの場合もH3K9me2のレベルは低下しました。放射線や化学的損傷後、これらのマウスはより多く体重を失い、腸が短く損傷が酷く、再生するクレフトや幹細胞が通常の個体より少ないことが示されました。意図的な損傷がない場合でも、G9a欠損マウスの腸内膜は発達不良で、クレフトは浅く、絨毛は短く、幹細胞とその分化子の数は減少していました。これらの細胞から培養皿で作られた小さな“ミニ腸”も十分に成長せず、この分子機構が腸の日々の更新に中心的役割を果たしていることを裏付けました。
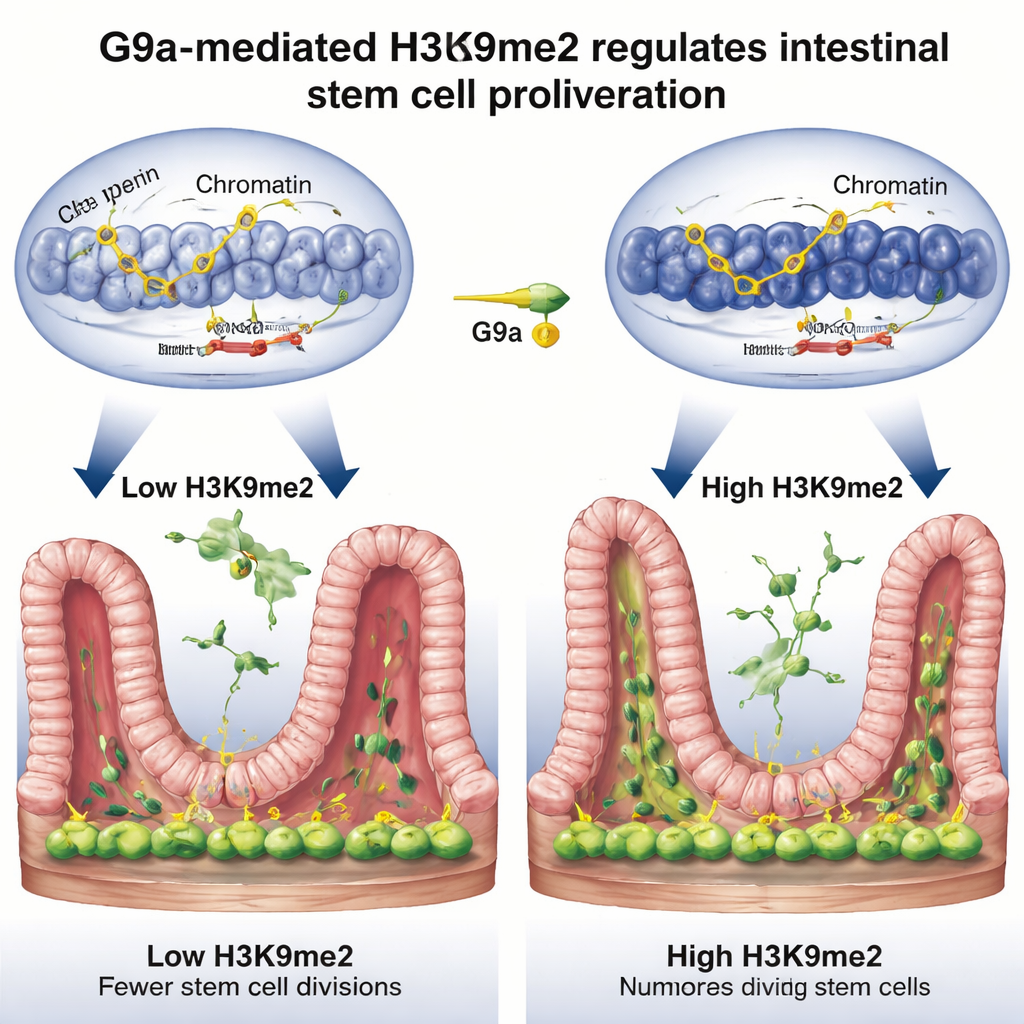
細胞分裂のブレーキを解く
さらに解析を進めると、研究チームはこの修復スイッチがどの遺伝子を制御しているかを調べました。三つの強力なゲノムワイド手法を組み合わせることで、G9aが付与するH3K9me2は通常細胞周期のブレーキとして働く領域、例えばRb1cc1、Rb1、Cdkn1a、Ptenのような遺伝子上に置かれる傾向があることがわかりました。G9aが欠けるとこれら領域から化学マークが消え、周辺の染色質が開いてブレーキ遺伝子の発現が強まり、幹細胞の増殖が鈍化しました。損傷後の通常の修復過程では、これらの遺伝子上のH3K9me2レベルが上昇し、その活性が低下して幹細胞はより自由に分裂して内膜を再建します。本質的には、G9aとH3K9me2は組織が再生する間、”停止”シグナルを一時的に抑える役割を果たします。
免疫シグナルから修復への連鎖
腸は単独で働くわけではなく、常に免疫系からの信号に耳を傾けています。研究者たちはG9aの上流に位置する一つの信号経路をたどりました。損傷後、免疫メッセンジャーであるIL‑4のレベルが上昇し、腸細胞内でSTAT6と呼ばれるタンパク質を活性化しました。活性化されたSTAT6はG9a遺伝子の制御領域に直接結合してその産生を促進しました。これにより命令系が形成されます:IL‑4がSTAT6を活性化し、STAT6がG9aを増強し、G9aがH3K9me2を付けて細胞周期のブレーキ遺伝子を抑えることで、幹細胞が増殖して損傷した内膜を回復できるようになるのです。
将来の治療への意味
専門外の人にとっても、本結果は腸の修復が単に遺伝子に依存するのではなく、それらの遺伝子がいつ使われるかを微調整する可逆的な化学的マークによって導かれることを示しています。IL‑4–STAT6–G9a–H3K9me2経路は、幹細胞の分裂を治療に必要な短期間だけ緩め、その後リセットできる内部の制御パネルのように働きます。将来的には、適切な時間と場所でG9aレベルを上げる薬剤や遺伝子操作など、この経路を穏やかに強化する治療法が、放射線損傷や炎症性腸疾患の再燃、あるいは腸内膜を損なう他の状態からの回復を速めつつ、制御不能な細胞増殖のリスクを最小限に抑える助けになる可能性があります。
引用: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
キーワード: 腸の再生, エピジェネティクス, 幹細胞, ヒストンメチル化, 炎症性腸疾患