Clear Sky Science · ja
WDR5はNANOGの凝縮体を再形成して転写プログラムを駆動し幹細胞の同一性を維持する
幹細胞とがんにおいてなぜ重要か
幹細胞は多様な細胞型に分化できるという驚くべき能力を持ち、これは初期発生や組織修復、そして残念ながら一部のがんにも関与します。本研究は、NANOGとWDR5という二つの主要タンパク質が協調して幹細胞の可塑性を維持するしくみを明らかにします。WDR5がNANOGのDNA上での凝集の形を物理的に変えることを示すことで、核内のタンパク質の液滴(凝縮体)の物理学と、正常な幹細胞および白血病における遺伝子制御とがつながることを示しています。
細胞の運命を決めるタンパク質
胚性幹細胞が多能性、つまりほぼすべての細胞になりうる状態を保つのは、NANOG、OCT4、SOX2といったマスターレギュレーターのおかげです。これらは広範な遺伝子ネットワークをオン・オフにします。特にNANOGは中心的役割を担い、DNAに結合するだけでなく、ヒストンに活性化の化学修飾を付加する大きな酵素複合体をリクルートします。WDR5も重要な因子で、ヒストン修飾機構が活性遺伝子を示すマークを付けるのを助けます。NANOGとWDR5が幹細胞同一性を支えることは知られていましたが、分子レベルでどのように相互作用し、それが核内での小さな液滴(「凝縮体」)の形成に影響するかは不明でした。
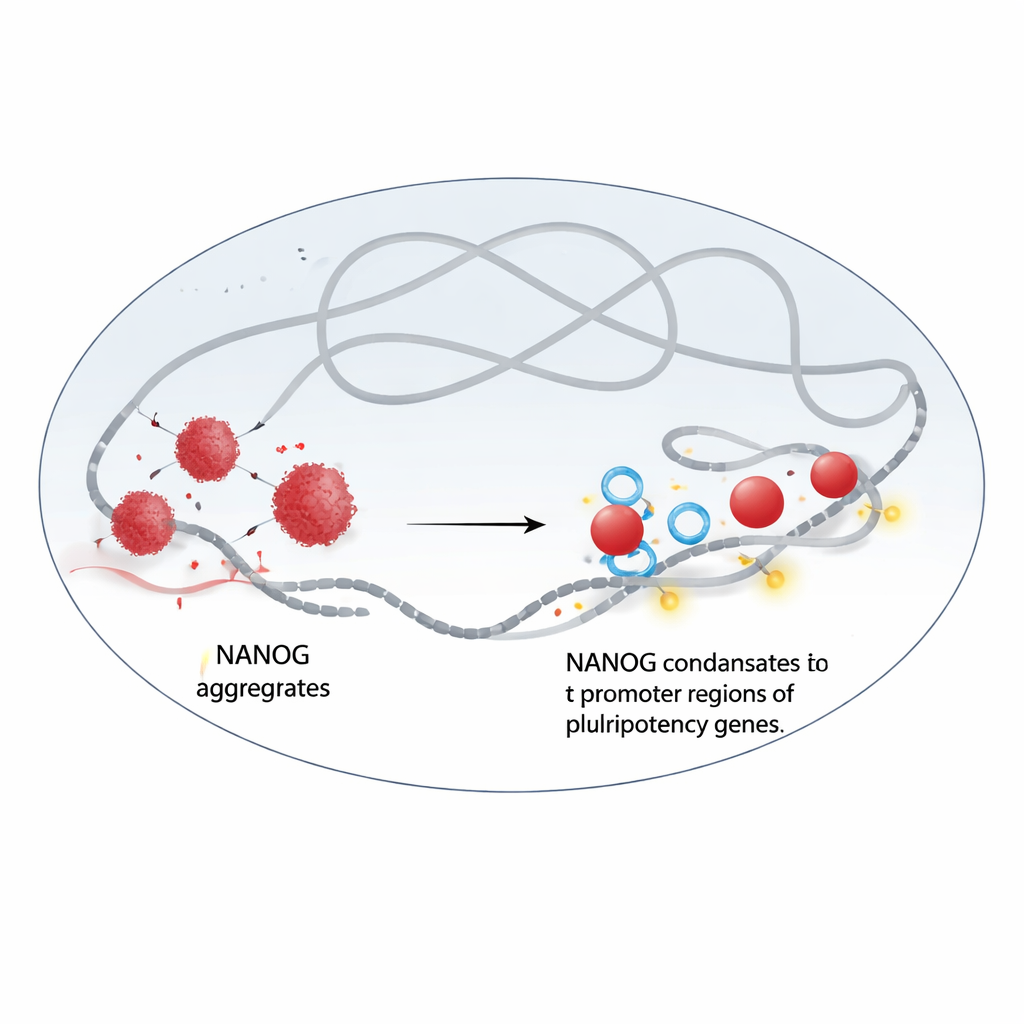
塊から液滴へ
研究者らはNANOGとWDR5が直接相互作用することを発見しました。単独で精製したNANOGは不規則で固体状の凝集体を作りがちです。電子顕微鏡や蛍光実験により、WDR5を加えるとこれらの凝集体が丸く流動性のある液滴に再編成され、動的な凝縮体として振る舞うことが示されました。生細胞では、NANOGとWDR5は明るい核内の点状構造として集合し、液–液相分離を壊す化学物質で処理すると急速に消失します。このとき、両タンパク質はクロマチン(遺伝情報を格納するDNA–タンパク質複合体)への結びつきを大きく失い、主要な多能性遺伝子における存在が急落しました。
特別な分子レベルの握手
原子レベルでの協奏を理解するため、研究者らはNANOGのDNA結合領域とWDR5の結晶構造を解きました。多くのWDR5のパートナーが短い柔軟なループを使うのに対し、NANOGは非構造的な腕と近接するヘリックスを含む広い表面を介してWDR5と結合します。NANOGの位置153にある一つのアルギニン残基がWDR5の中心チャネルに深く挿入され、「鍵と鍵穴」の相互作用の重要な部分を形成します。この残基をアラニンに変える(R153A変異)は結合をほぼ消失させます。重要なのは、変異NANOGは依然としてDNAには結合できるものの、WDR5はその凝集体を流動的な液滴に効率的に再形成できなくなり、この特異的接触が機能的な凝縮体形成に不可欠であることを示している点です。
幹細胞の若さを保つこと─失敗するとどうなるか
著者らがマウス胚性幹細胞をNANOG R153A変異体のみを発現するように改変したところ、影響は劇的でした。変異細胞は多能性細胞に典型的なきつく丸みを帯びたコロニーを失い、平坦化して分化の視覚的指標を示しました。アルカリフォスファターゼ陽性コロニーの形成は減少し、幹性の別の指標も低下しました。また、Nanog自身やSox2、Esrrb、Klf4などの主要な多能性遺伝子の発現が低下しました。同時に骨や発生に関わる系統特異的な遺伝子がオンになりました。ゲノムワイドなプロファイリングでは、NANOGとWDR5が何千ものプロモーターで共占有しなくなり、二つの主要な活性化ヒストンマークであるH3K4me3とH4K16acがこれら共有部位で特異的に失われていました。分化の初期段階で、これらの化学修飾と新たに作られるRNA転写産物は総mRNA量が減る前に先行して減少し、能動的なクロマチン維持の根本的な障害を示唆しました。
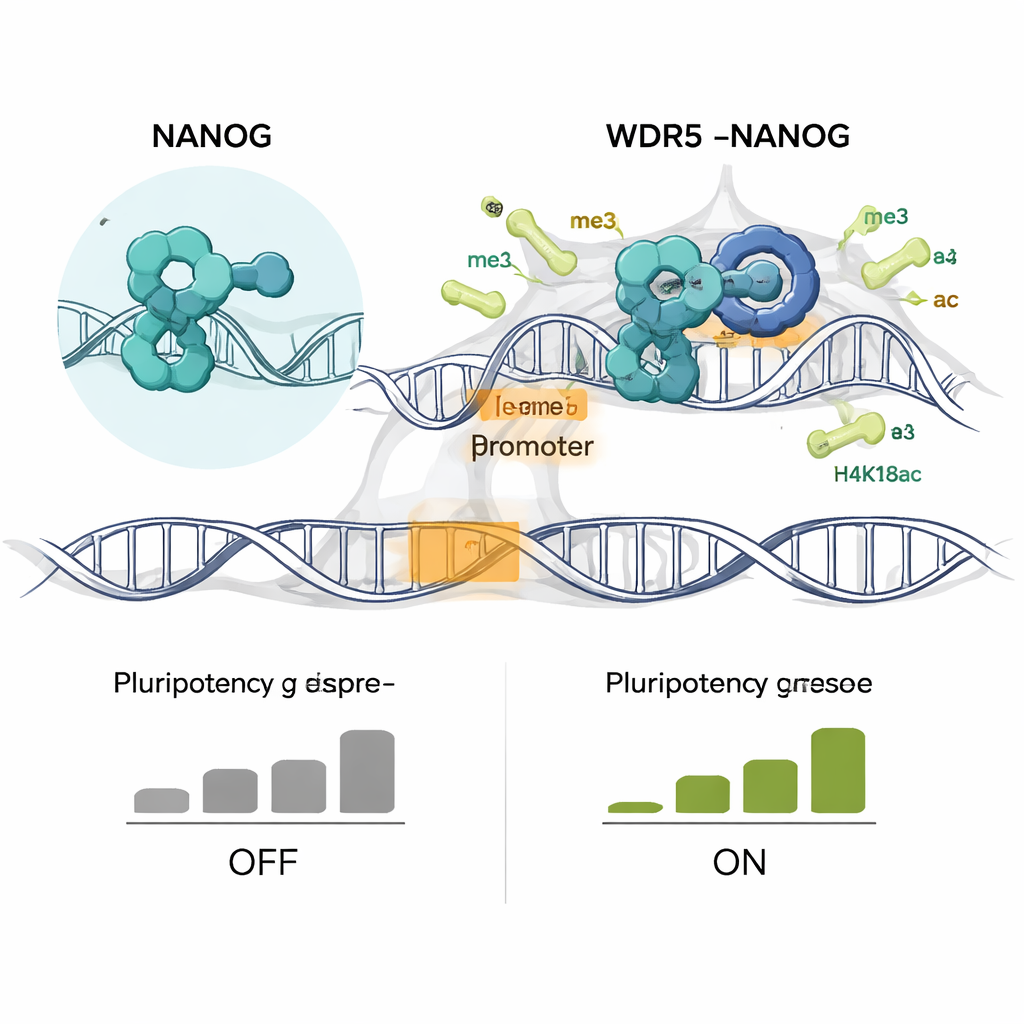
基本的な機構をがん治療へ転用する
類似の遺伝子ネットワークが一部のがん幹細胞を駆動することから、研究チームはNANOG–WDR5軸を妨げることで急性骨髄性白血病のマウスモデルにおける白血病幹細胞を抑制できるか検証しました。小分子化合物C16はNANOGが結合するのと同じWDR5のポケットに結合し、WDR5–NANOG相互作用を選択的に弱めました。白血病細胞ではC16がコロニー形成を著しく減らし、幹様の集団を枯渇させ、細胞を成熟した骨髄系運命へと押し進めました。一方で、既存の別のWDR5パートナーを標的にする白血病薬に比べて正常な血液幹細胞ははるかに温存されました。RNAシーケンシングはC16が幹性と自己複製の遺伝子プログラムを遮断し、分化経路を促進することを示しました。マウスではC16投与により白血病幹/前駆細胞集団が減少し、このタンパク質間相互作用を標的にする治療的有望性を裏付けました。
大局観:液滴が細胞同一性を決める仕組み
本研究はWDR5が単にクロマチンに座して酵素を呼び込む以上の働きをすることを示します。WDR5はNANOGを不活性な凝集体から可塑的な液体凝縮体へ物理的に再形成し、それらを多能性遺伝子のプロモーター上に位置させ、活性化ヒストンマークを引き寄せます。この再形成が—NANOGの精密な変異や二者の接触を乱す小分子により—妨げられると、幹細胞は同一性を失い、がん幹細胞は自己複製能を失います。一般読者に伝えたい主なメッセージは、DNA上でタンパク質がどのように液滴として集合するかの微妙な変化が、細胞が若く柔軟な状態を保つか、特定の運命へ成熟するか、あるいは疾患を促進するかという点で巨大な影響を及ぼし得る、ということです。
引用: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
キーワード: 幹細胞多能性, NANOG, WDR5, 相分離, 白血病幹細胞