Clear Sky Science · ja
初産取りのない乳腺と多産の乳腺の発達差が示すIL33+ハイブリッド上皮細胞
妊娠が生涯の乳がんリスクをどう変えるか
なぜ若いうちに出産することが女性の生涯の乳がんリスクを下げる一方、単に年を取ることはリスクを高めるのか?本研究はマウスを用いて、妊娠したことのない個体と妊娠を経験した個体の乳房の細胞“生態系”が時間とともにどう変わるかを調べる。個々の細胞が加齢や出産でどう変化するかを追跡することで、妊娠による長期的な乳がん予防を説明しうる、まれで形を変える細胞群を明らかにしている。
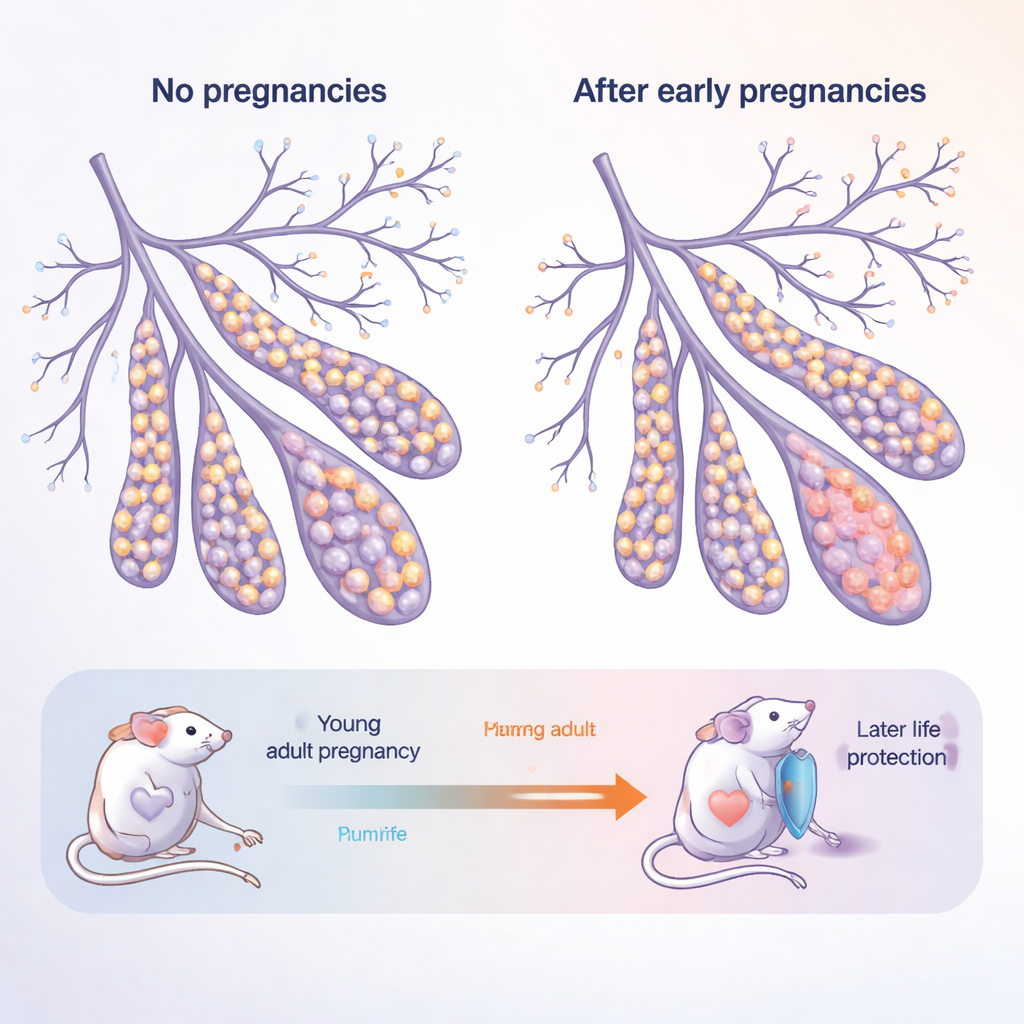
変化し続ける生きた組織としての乳腺
乳腺は静的な器官ではなく、思春期、妊娠期、授乳期の終わりにかけて著しく成長・再編される。導管を内面から覆う『内腔(ルミナル)』細胞と、外側で構造を支え幹様細胞を含む『基底(バザル)』細胞という二つの主要な上皮層から構成される。著者らは、若い成体マウスと年配の“閉経後様”マウスを、いずれも未妊(初産なし)または多回出産(有産)という条件で比較した。この実験デザインは、20代で出産し50代以降まで年を取る女性を模している。
加齢と妊娠が組織を異なる方向へ引っ張る
妊娠を経験せず年を取ったマウスでは、乳腺は基底細胞の割合が増え、ルミナル細胞が減る方向へ変化した。これらの高齢・未妊の乳腺は、単一細胞から育てたミニ3D構造であるオルガノイドを多く作り、細胞が異常に増殖志向であることを示した。一方、妊娠を経験したマウスではバランスが“正常化”し、加齢による基底細胞の増加は抑えられ、オルガノイドの形成も減少した。これは妊娠が持続的な痕跡を残し、細胞の運命決定や再生能(ひいてはがんになりうる潜在性)を抑えることを示唆している。
ハイブリッドで形を変える細胞の発見
より詳しく見るために、研究チームは単一細胞RNAシーケンシングを用い、数千の個々の乳腺細胞でどの遺伝子が活性化しているかを読み取った。期待されるルミナル、バザル、免疫、間質細胞に加え、どちらの主要層にもきれいに当てはまらないまれな集団が見つかった。これらの細胞はルミナルとバザルの両方のマーカーを発現し、『ハイブリッド』上皮細胞と名付けられた。注目すべきは、これらのハイブリッドは未妊のマウスで加齢とともに蓄積したが、同等に年を取った有産のマウスでははるかに少なかったことだ。ハイブリッドはシグナル分子IL-33をコードする遺伝子Il33を強く発現し、初期発生段階や高い可塑性――同一性や振る舞いを切り替える能力――に関連するマーカーも示していた。
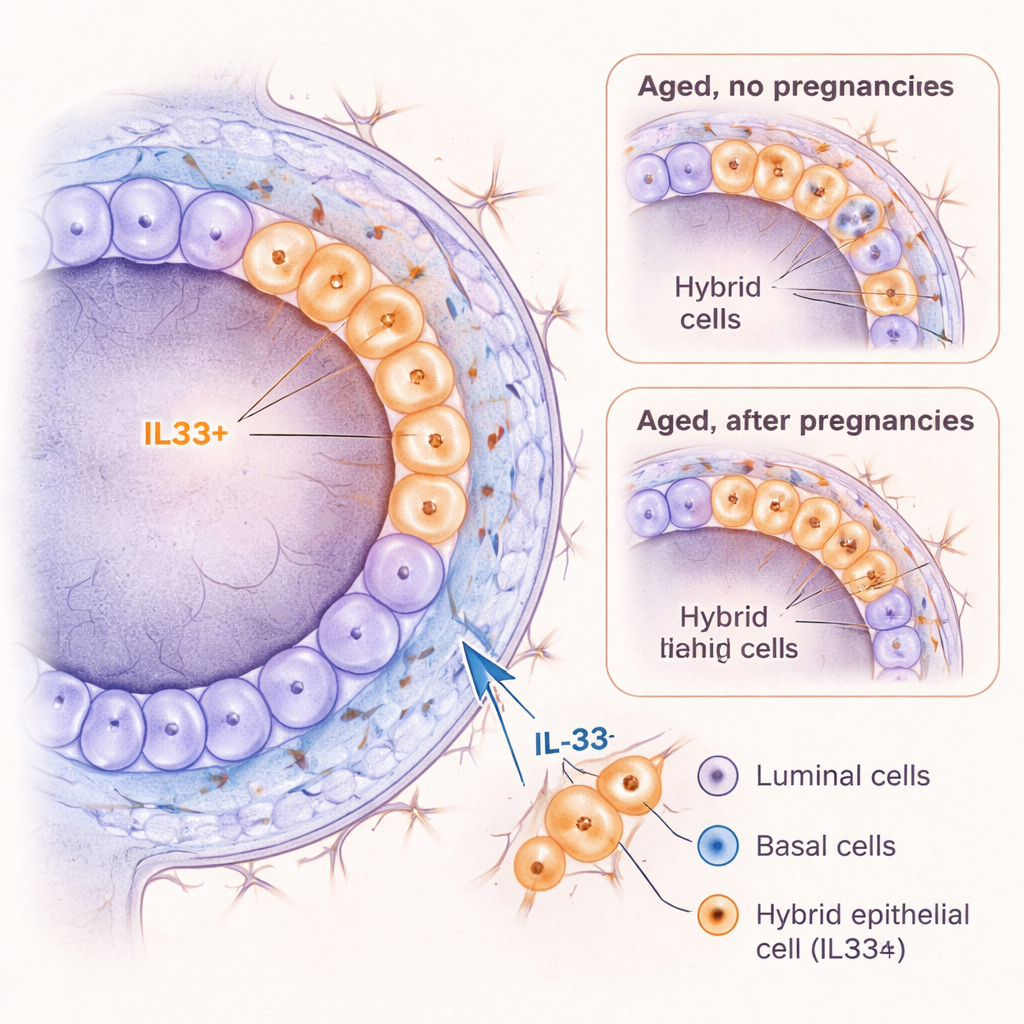
リスクの高い細胞状態を促すIL‑33
IL‑33は他の臓器で炎症やがんに結びついているため、研究者たちはIL‑33が乳腺細胞を積極的にハイブリッド様の状態へ押しやるかどうかを調べた。若いマウス乳腺細胞を3D培養でIL‑33処理すると、基底層細胞がより多くのオルガノイドを形成し、より原始的な同一性を保持し、ハイブリッドマーカーKRT6A陽性の細胞が増えた。生きた若いマウスに短期のIL‑33注射を行うと、導管が拡張し分裂の急増が引き起こされ、一時的にKRT6A陽性ハイブリッド細胞が増え、基底様細胞へのシフトが見られた。重要な点として、がんに関連する突然変異(腫瘍抑制遺伝子Trp53の喪失)を持つ細胞では、IL‑33はさらに増殖を促進した。これらの所見は、IL‑33が可塑的で増殖志向の細胞状態を作り出し、特にがん化しやすい状態を助長する可能性があることを示唆している。
ヒト乳房組織からの手がかり
同様の細胞が人にも存在するかを確かめるため、著者らは正常なヒト乳房組織の大規模な単一細胞データセットを再解析した。マウスのハイブリッドと同様に、ルミナルとバザルの特徴を併せ持ち、IL33や関連遺伝子を発現する小さな上皮細胞集団を同定した。IL33陽性細胞は複数のデータセットで加齢とともに増加していた。一次ヒト乳腺細胞を培養した実験では、IL‑33処理によりオルガノイド形成が増え、細胞は基底様のプロファイルへと傾き、CD44陽性細胞(乳がんで未熟な幹様細胞と関連するマーカー)が濃縮された。利用可能なヒトサンプルでは早期妊娠がこの集団にどう影響するかを明確に検証することはできなかったが、マウスでの類似点は際立っている。
乳がん予防の理解にとっての意義
一般読者向けに言えば、中心的なメッセージは妊娠が乳腺の老化の仕方を書き換えるようだ、ということだ。マウスでは、若いうちの妊娠がルミナルとバザルの境界を曖昧にし、非常に柔軟で増殖しやすいIL‑33豊富なハイブリッド細胞の蓄積を防ぐ。IL‑33自体が特にがん関連変異がある場合に細胞をそのようなリスクの高い、形を変えやすい状態へ押しやることができる。妊娠がこれらのハイブリッド細胞の数や持続性を減らすことで、加齢した乳房組織において『不適切な』種類の細胞が『不適切な』時期に存在してがん化しやすくなる可能性を下げていると考えられる。この機構的洞察は、実際に妊娠しなくても若年出産の保護効果を模倣する戦略を将来導く手がかりになり得る。
引用: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
キーワード: 乳房の老化, 妊娠と乳がん, 乳腺幹細胞, IL-33シグナル伝達, ハイブリッド上皮細胞