Clear Sky Science · ja
自己崩壊性ホスホラミド酸エステルを介したヒドロキシル含有薬剤の輸送による抗体薬物複合体のペイロード範囲の拡大
がんに対するより賢い誘導弾
がん薬は非常に強力である一方、カーペット爆撃のように腫瘍と同程度に健康な組織にもダメージを与えがちです。抗体–薬物複合体(ADC)は、強力な薬をがん細胞に向かう抗体に結び付けることでこの問題を解決するために作られ、治療を誘導弾のようにします。本記事では、抗体と薬の間に挟まれる新しい化学的「プラグ」を紹介し、これによりこうした誘導弾がより精密かつ柔軟になり、現在のADCが運べるものよりはるかに多くのタイプのがん薬を搭載できる可能性が開けることを説明します。
なぜ現在の標的化薬はまだ制約があるのか
ADCは三つの要素で構成されます:がん細胞上のマーカーを認識する抗体、毒性のある薬(「ペイロード」)、そしてそれらをつなぐ化学的リンカー。承認されている多くのADCは、DNAを損傷させるか細胞分裂を阻害するような限られた種類のペイロードに依存しています。その主な理由の一つがリンカーです:リンカーは血流中では薬を確実に保持し、腫瘍細胞内に入ったときにきれいに薬を放出しなければなりません。既存のリンカーは主にアミンなど特定の化学基を持つ薬とよく適合し、アルコール基(–OH)を含む多くの薬ではうまく機能しないことが多いのです。そのため、安全かつ効率的に現在のADC設計で運べない多くの有望ながん薬が棚上げされています。
抗ウイルス薬のトリックを借りる
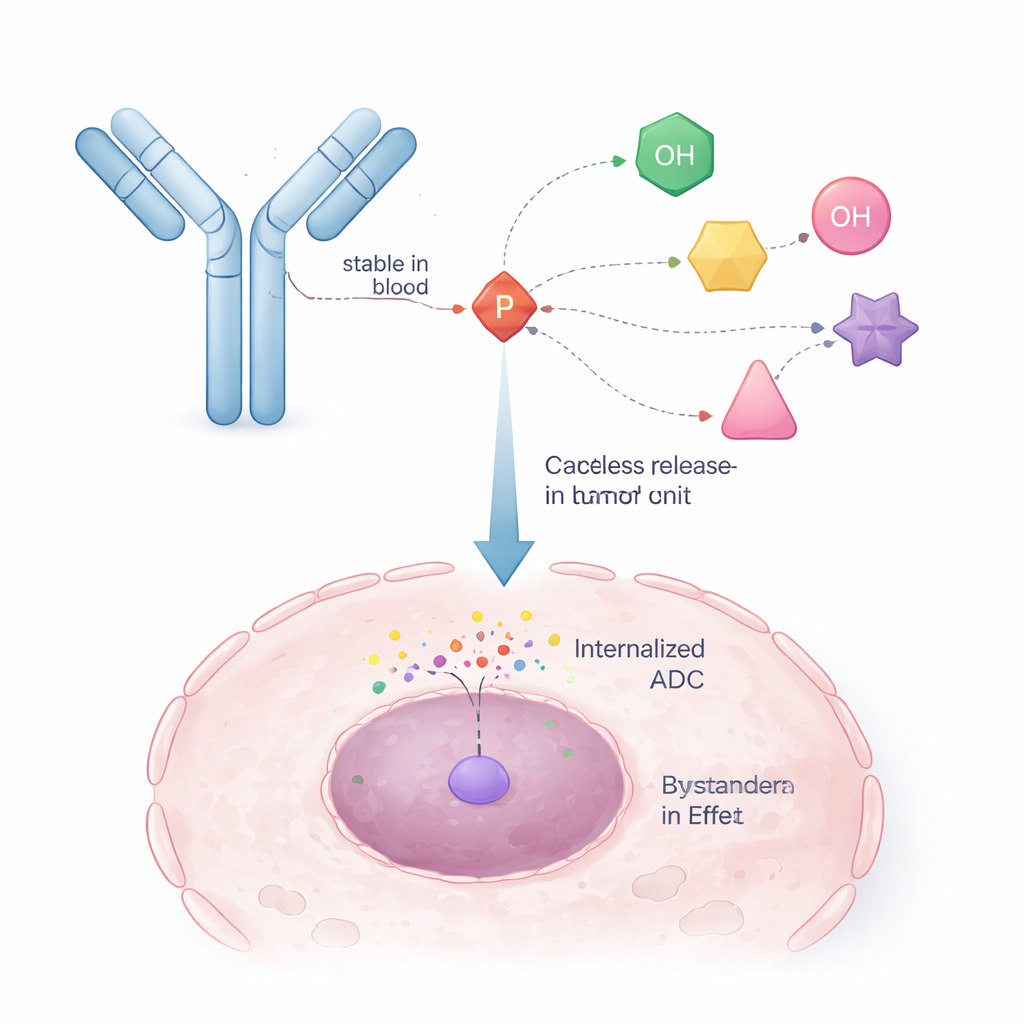
研究者たちは、抗ウイルス薬で既に実証されている戦略であるProTideに目を向けました。これらの薬では、リン酸基の電荷を一時的に覆い隠すリン(リン)を含む化学ユニットを用い、細胞内に入りやすくしてから内部で分解して活性体を放出します。著者らはこの概念を再設計し、リン原子コアの一つの腕を抗体に結合させ、他の腕でがん薬を保持するようにしました。これにより「自己崩壊性」リンカーが生まれます:腫瘍細胞内の酵素などの内部トリガーが構造の小さな部分を切断すると、リンのユニットが制御された形で崩壊して元のアルコール基を持つ未修飾の薬分子を放出します。
汎用性のある化学的プラグの構築
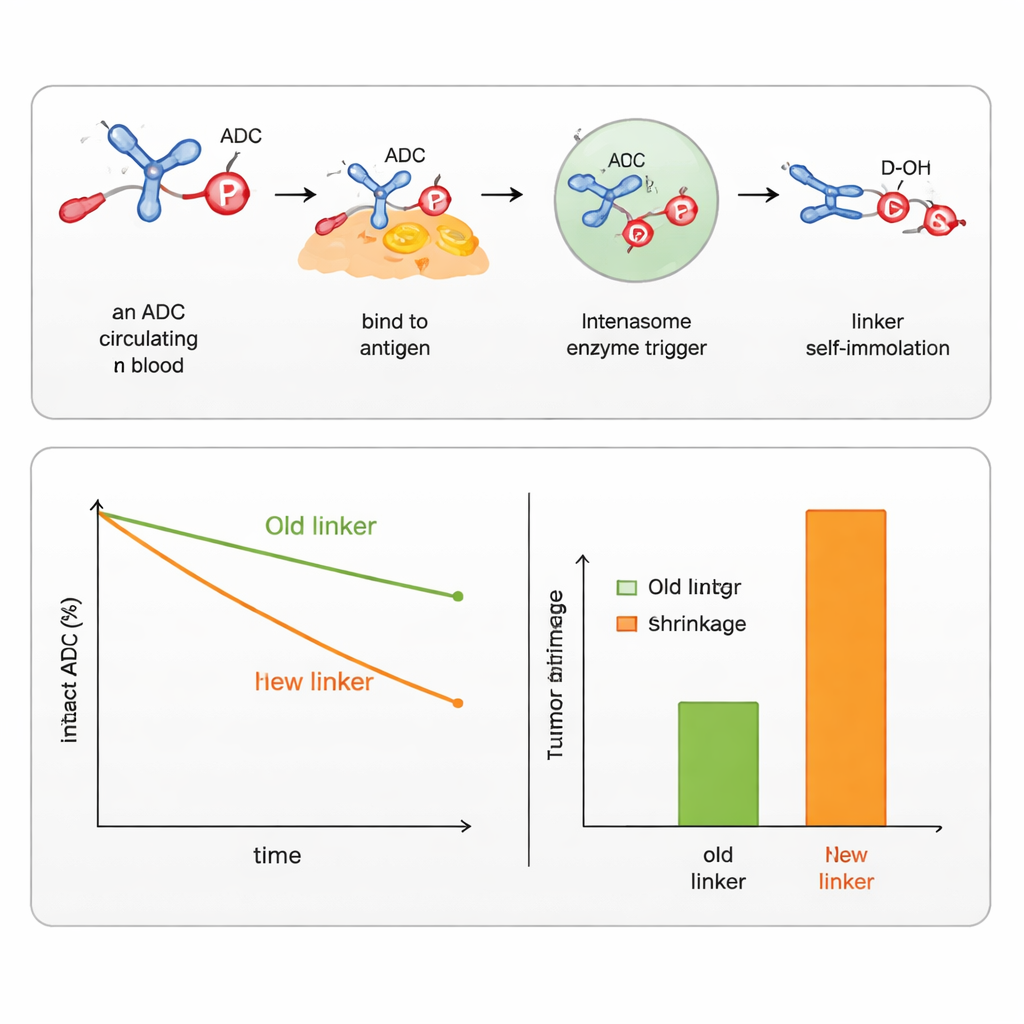
研究チームは、リン原子まわりの置換基を調整することで、血中でのリンカーの安定性や細胞内での分解速度を微調整できることを示しました。彼らは、エステラーゼやプロテアーゼ(特定の結合を切断する酵素)をはじめ、糖基を認識する酵素や細胞内区画の還元環境に応答するものなど、がん細胞内で一般的な複数のトリガーに反応するバージョンを設計しました。これらの設計を用いることで、芳香族アルコール(化学療法薬SN38のような)や脂肪族アルコール(承認済み乳がんADCのペイロードであるDXdのような)を同様に結合・放出することに成功しました。SN38およびDXd用の既存の市販リンカーと比較すると、新しいホスホラミド酸リンカーは血清中で薬をより長く保持し、腫瘍への薬の送達量を増やし、マウスにおける腫瘍縮小効果が強く、健康な細胞への影響が少ないことが示されました。
多くの新しいがんペイロードの解放
リンカーの汎用性を試すために、研究者たちは少なくとも一つの–OH基を持ち、がん細胞内で非常に異なる作用をする10種類の薬を搭載したADCを組み立てました。これらには、DNA合成阻害剤、タンパク質フォールディング(HSP90)阻害剤、エネルギー代謝(NAMPTおよびDHODH)阻害剤、翻訳阻害剤、さらにはパクリタキセルやゲムシタビンといったよく知られた薬剤が含まれます。構造が多様であるにもかかわらず、彼らはすべて高い薬物搭載量の均一なADCを作製できました。複数のがん種にわたる細胞実験では、これらのADCの多くがナノモーラーあるいはサブナノモーラーの高い活性を示し、抗体の標的を発現する細胞に対する明確な選択性を示しました。これはリンカーが一貫して適切な細胞内で活性薬を放出できることを確認する結果です。
展示例としてのゲムシタビン
ゲムシタビンは広く用いられる化学療法薬ですが、従来の形では体内から非常に速やかに消失するため、患者は大量を繰り返し投与する必要があり、安全に投与できる量が制限されます。ホスホラミド酸リンカーを用いて、著者らはゲムシタビンをHER2標的抗体の二つのアルコール位置のいずれかに結合させ、どちらのバージョンもがん細胞内では完全な活性を取り戻すことを示しました。HER2陽性腫瘍のマウスモデルでは、典型的な遊離薬の用量のおよそ千分の一の総量のゲムシタビンしか含まない単回投与のゲムシタビンADCが、強力かつ選択的な腫瘍制御をもたらしました。ADCの血中での挙動は裸の抗体のそれとほぼ一致し、高用量でもラットでよく許容されたことから、広い安全マージンが示唆されます。
今後のがん治療にとっての意味
専門外の方への主要メッセージは、本研究が抗体により広範な種類のがん薬を安全に搭載させうる、新しく非常に適応性の高い化学的コネクタを提供したということです。薬が循環中に結合したままであり、ADCががん細胞内に取り込まれた後にのみきれいに放出されることを保証することで、ホスホラミド酸リンカーは腫瘍に到達する薬の量を改善し、健康な組織への副作用を減らします。同様に重要なのは、形状や作用機序が大きく異なる既存の強力な低分子薬を標的療法として再利用できるようにする点です。これにより患者に提供できるADCの選択肢が大幅に拡大し、現在の限られたペイロード群に耐性を示す腫瘍への対処が進む可能性があります。
引用: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
キーワード: 抗体–薬物複合体, がん薬物送達, 自己崩壊性リンカー, ホスホラミド酸化学, 標的化化学療法