Clear Sky Science · ja
腎透明細胞癌におけるEPAS1発現の転写制御回路を維持するHIF
なぜ腎がんをより注意深く見る必要があるのか
透明細胞腎細胞癌は腎臓がんの中で最も一般的な型で、多くの患者は現在HIF‑2αというタンパク質を阻害する薬を受けています。これらの薬は腫瘍を縮小させることがありますが、すべての人に同じように効くわけではありません。本研究は単純だが重要な問いを投げかけます:なぜ一部の腎腫瘍が非常に多くのHIF‑2αを産生するのか、そしてその「オン・スイッチ」を理解することで誰が治療の恩恵を最も受けるか予測し、新たな治療法を設計できるのか?
暴走する酸素センサー
健康な腎細胞はVHLという安全装置タンパク質を使って、HIFと呼ばれる酸素感知因子を厳密に制御しています。十分な酸素があるとき、VHLはHIFタンパク質を破壊の標的にして、血管新生や細胞分裂を促す遺伝子のスイッチが入らないようにします。透明細胞腎がんでは、VHLが失われるか損なわれていることが多く、その結果、HIFファミリーの一員であるHIF‑2α(EPAS1遺伝子にコードされる)は分解を免れ蓄積します。以前の研究は、HIF‑2αの高い活性が腫瘍の増殖促進や予後不良と関連し、HIF‑2αを阻害することで一部の患者で腫瘍の進行を遅らせたり止めたりできることを示していました。しかし、腎腫瘍でEPAS1遺伝子活性を高める分子メカニズムは十分に理解されていませんでした。
がん遺伝子の隠れたDNAスイッチ
著者らは患者由来の腫瘍サンプル、単一細胞データ、がん細胞モデルを用いて、HIF‑2αのメッセンジャーRNAが正常な腎組織や他の腎腫瘍型と比べて透明細胞腫瘍で著しく高いことを示しています。次に、EPAS1領域のゲノムを化学的・構造的マーカーでスキャンし、活性化された調節DNAを示す領域を探しました。すると、EPAS1の約7万塩基上流に位置する強力なエンハンサー(遠位の遺伝子スイッチの一種)が、透明細胞腫瘍特異的に活性化していることが明らかになりました。腫瘍細胞ではこのエンハンサーのクロマチンは開いており、活性化マークで飾られ、物理的にEPAS1プロモーターとループで接触していますが、正常な腎細管細胞ではこの領域は概ね沈黙しています。このエンハンサーの活性は、大規模ながんデータセットにおけるEPAS1レベルの上昇と相関します。 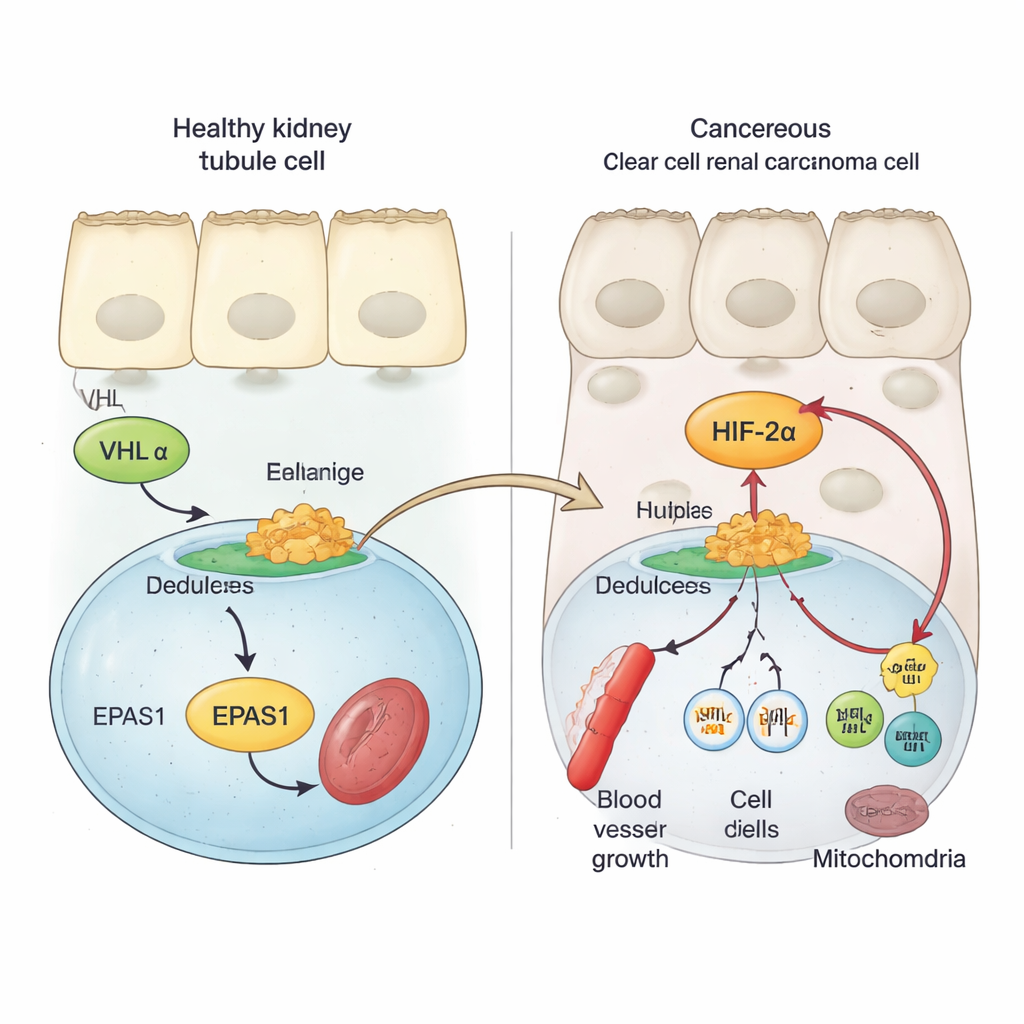
腎の同一性因子によって駆動される自己増強ループ
研究は、HIFタンパク質が低酸素に応答するだけでなく、自らの産生を促進していることを示します。研究者がVHLを回復させるか主要なHIFのパートナー(HIF‑1β)を除去すると、EPAS1レベルは低下し、エンハンサーのアクセス可能性は減少します。タンパク質–DNA接触の直接マッピングにより、HIFがEPAS1上流の二つのエンハンサー領域(透明細胞特異的エンハンサーを含む)に結合することが示されました。腎腫瘍細胞では、このエンハンサーはPAX8やHNF‑1βといった腎細胞の同一性を定め腫瘍増殖を支持する転写因子にも占有されています。PAX8やHNF‑1βを破壊するか、エンハンサー内のそれらの結合部位を変異させると、HIF‑2αのRNAおよびタンパク質が減少し、エンハンサー活性が弱まります。これらの発見は自己制御回路を明らかにします:HIF‑2αは腎の系統因子と協働してEPAS1エンハンサーの活性を高め、それがさらにHIF‑2αの産生を駆動するのです。
遺伝的リスクと腫瘍挙動が同じ回路に収束する
EPAS1領域は、ゲノムワイド研究で長く腎がんリスクのホットスポットとして指摘されており、特定の遺伝的多型が高いがん発生率や腫瘍中のVHL変異と関連しています。遺伝データと遺伝子発現測定を組み合わせることで、著者らは主要なEPAS1変異体の高リスクアレルを持つ個人は腫瘍中でHIF‑2αレベルが高くなる傾向があり、実験的にHIFが安定化されると正常な腎細管細胞でも同様に高くなることを示しました。これは、遺伝的なDNA差異がエンハンサーの応答性を調節し、VHLが失われたときに一部の腎がより強くHIF‑2αを増幅するように予め準備されることを示唆します。神経膠芽腫細胞での実験は、同じエンハンサーが一部の脳腫瘍でも利用されうることを示し、この調節モジュールがHIF‑2αが重要な他のがんでも再利用されうることを示唆しています。 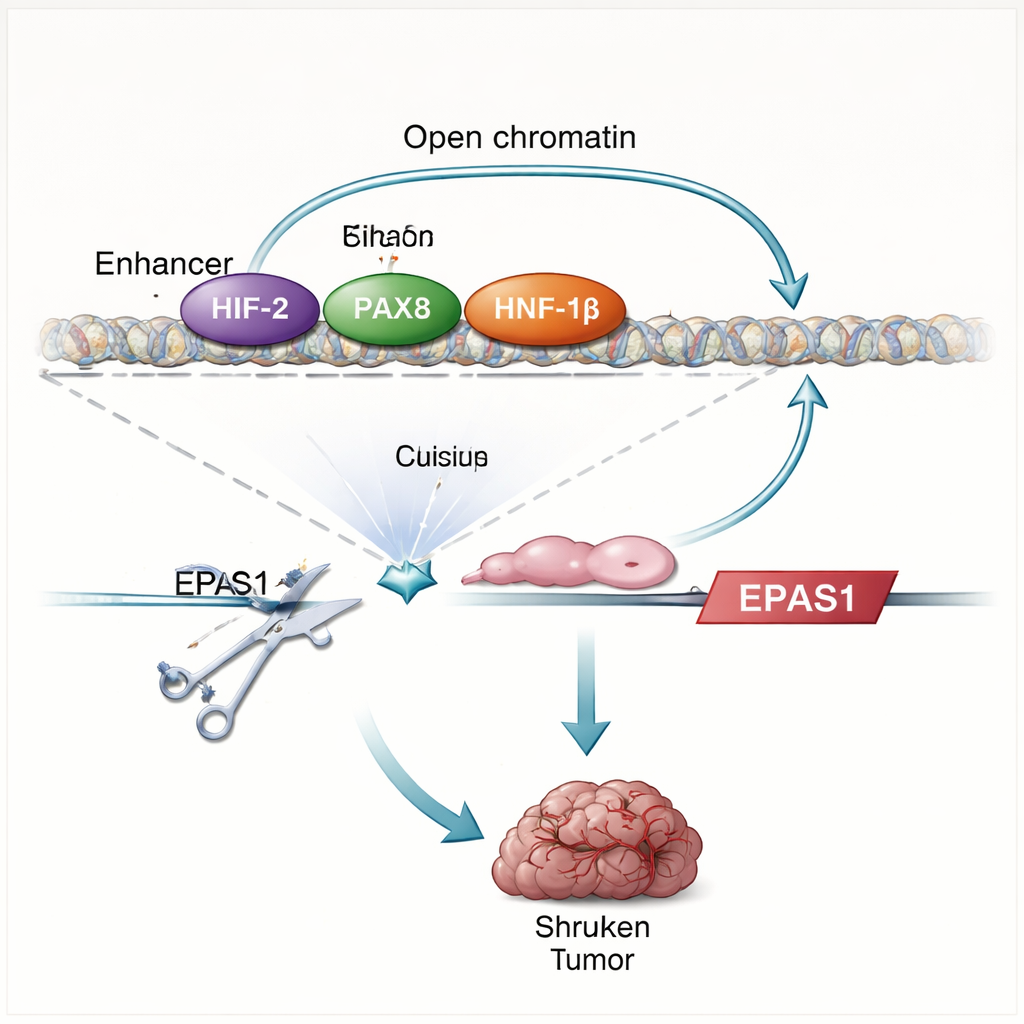
ループを断ち腫瘍成長を止める
このエンハンサーがどれほど必須かを試すために、研究チームはCRISPRゲノム編集を用いて腎がん細胞株と新鮮な患者腫瘍細胞のエンハンサー内のHIF結合モチーフを損傷させました。この切断によりHIF‑2αのRNAは約3分の1〜2分の1に低下し、CCND1やVEGFAといったよく知られたHIF‑2α標的遺伝子のレベルが下がり、より広範な低酸素応答プログラムが弱まります。編集した細胞をマウスに移植すると、対照細胞とは対照的にほとんど腫瘍を形成できませんでした。エンハンサー破壊後の遺伝子変化のパターンは、臨床用薬によるHIF‑2α直接阻害の効果とよく一致しており、この単一のDNA要素がこれらのがんにおけるHIF‑2α経路の主要な駆動因子であることを強調しています。
患者と治療への意義
専門家でない読者にとっての主要なメッセージは、著者らが透明細胞腎腫瘍で主要ながん促進タンパク質HIF‑2αを持続的にオンに保つ自己増幅型のDNAスイッチを明らかにしたことです。このスイッチはVHLという安全ブレーキの喪失と腎特異的な補助因子の両方に依存しており、遺伝的多型にも影響されます。多くの透明細胞腫瘍でこのエンハンサーが高く活性化しており、HIF‑2α経路の強さと密接に結びついていることから、その活性を測定することやエンハンサー自体を標的とすることは、現在のHIF‑2α阻害薬から最も恩恵を受ける患者を特定する助けになり得ますし、腫瘍が薬剤耐性になった場合にこの経路を遮断する新たな方法を提供する可能性があります。
引用: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
キーワード: 透明細胞腎細胞癌, HIF-2α, EPAS1エンハンサー, VHL変異, 腎がんの遺伝学