Clear Sky Science · ja
いくつかのテロメアDNA反復付加サイクル段階でのヌクレオチド結合ヒトテロメラーゼの構造
なぜ染色体の末端が重要なのか
細胞が分裂するたびに、染色体の末端にある保護キャップ(テロメア)は少しずつ短くなります。これらが極端に短くなると、細胞は分裂を停止したり機能不全を起こし、老化や疾患に寄与します。テロメラーゼと呼ばれる分子機械はこれらのキャップを再構築でき、ほとんどのがんで異常に活性化しています。本研究は、ヒトのテロメラーゼがテロメアを一歩ずつどのようにつかみ伸ばすかを前例のない詳細で明らかにし、老化関連障害やがんにおいてこの酵素を将来どのように微調整できるかについての手がかりを示します。
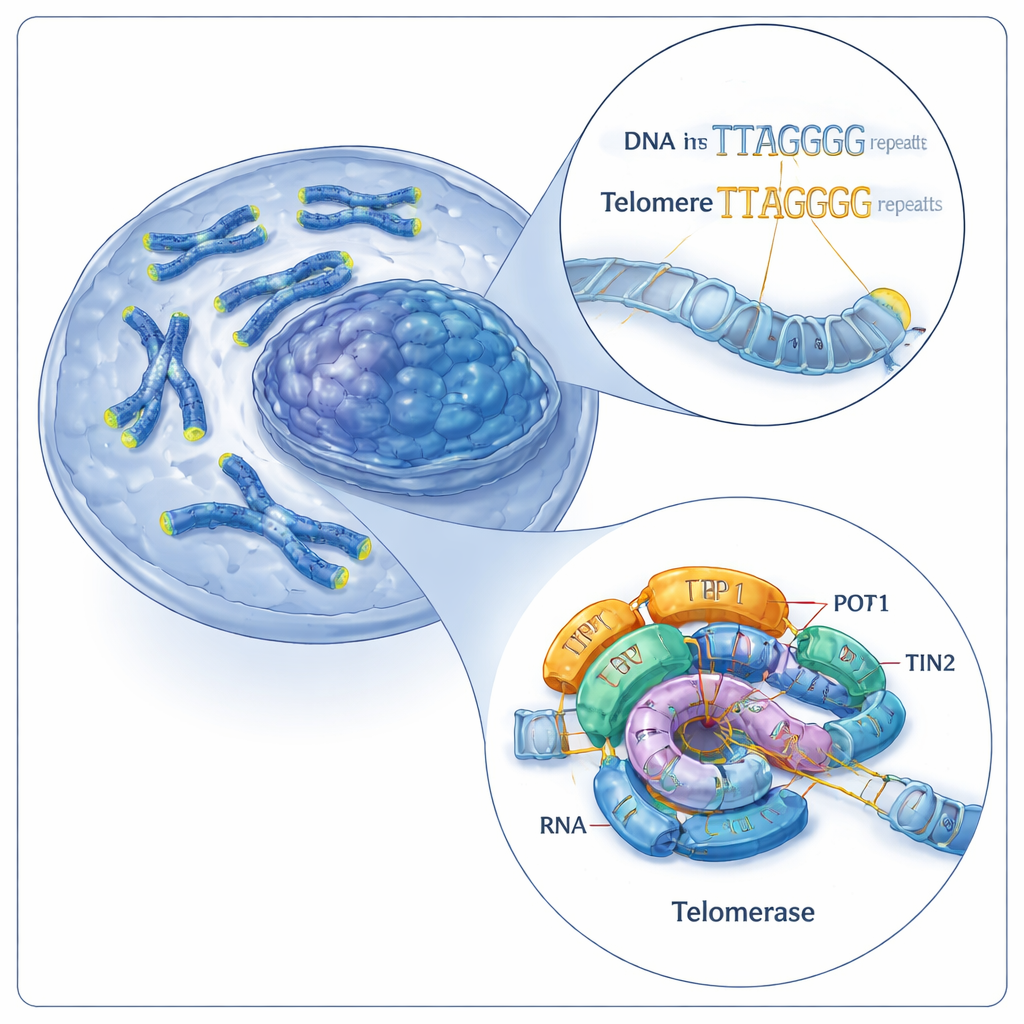
染色体末端の修復チーム
テロメアは短い反復配列からできており(ヒトでは6塩基の配列:TTAGGG)、テロメラーゼはこれらの反復を染色体末端に付け加えてテロメアを伸長します。テロメラーゼは主に2つの要素で働きます:タンパク質のテロメラーゼ逆転写酵素(TERT)と、鋳型として働く内在性のRNA分子(hTR)です。これらは触媒コアを形成し、さらにTPP1–POT1–TIN2のトリオを含むシェルタリンなどの補助タンパク質群が助けます。これまでの研究ではヒトのテロメラーゼは単一の作業状態しか可視化されておらず、機械が繰り返し反復を付加しつつDNAから離れないようにする仕組みという重要な疑問が残されていました。
作動中のテロメラーゼを凍結する
研究者たちはヒト細胞内でヒトテロメラーゼを再構築し、意図的に設計したテロメアDNA断片と反応しないヌクレオチド類縁体(DNAの文字に似ているが完全には組み込まれない分子)と組み合わせました。高分解能クライオ電子顕微鏡を用いて、反復付加サイクルの三つの主要段階、開始(イニシエーション)、複製の途中(伸長)、反復を終える直前(プレ終結)のスナップショットを捉えました。各スナップショットは、テロメラーゼの触媒コアが短いDNA–RNAハイブリッドを抱え込み、活性部位に次に付加されるべきヌクレオチドが配位している様子を示していました。
大きな過程を制御する小さなジッパー
三つの段階すべてに共通して驚くべき特徴が見られました:テロメラーゼ内部のDNA–RNAハイブリッドは本質的に同じ長さ、すなわち常に4塩基対であり、新しいヌクレオチドが入ると一時的に5塩基対に伸びるだけだということです。TERTの特定のアミノ酸残基は「ジッパーヘッド」とあだ名され、この短いハイブリッドの端を一貫して示し、それ以上伸びるのを防ぎます。新しいDNAの塩基が付加されると、遠位端の一塩基対が解離するため、ハイブリッドはこの厳密な4〜5塩基対の窓を超えて延長されません。このコンパクトな設計は鎖の分離と位置のずれを容易にし、酵素がDNAを完全に離さずに次の反復へ移動することを可能にしていると考えられます。短いハイブリッド内でどの塩基が占めるかの微妙な違いが、あるテロメア末端配列が他よりもテロメラーゼに強く結合する理由を説明します。
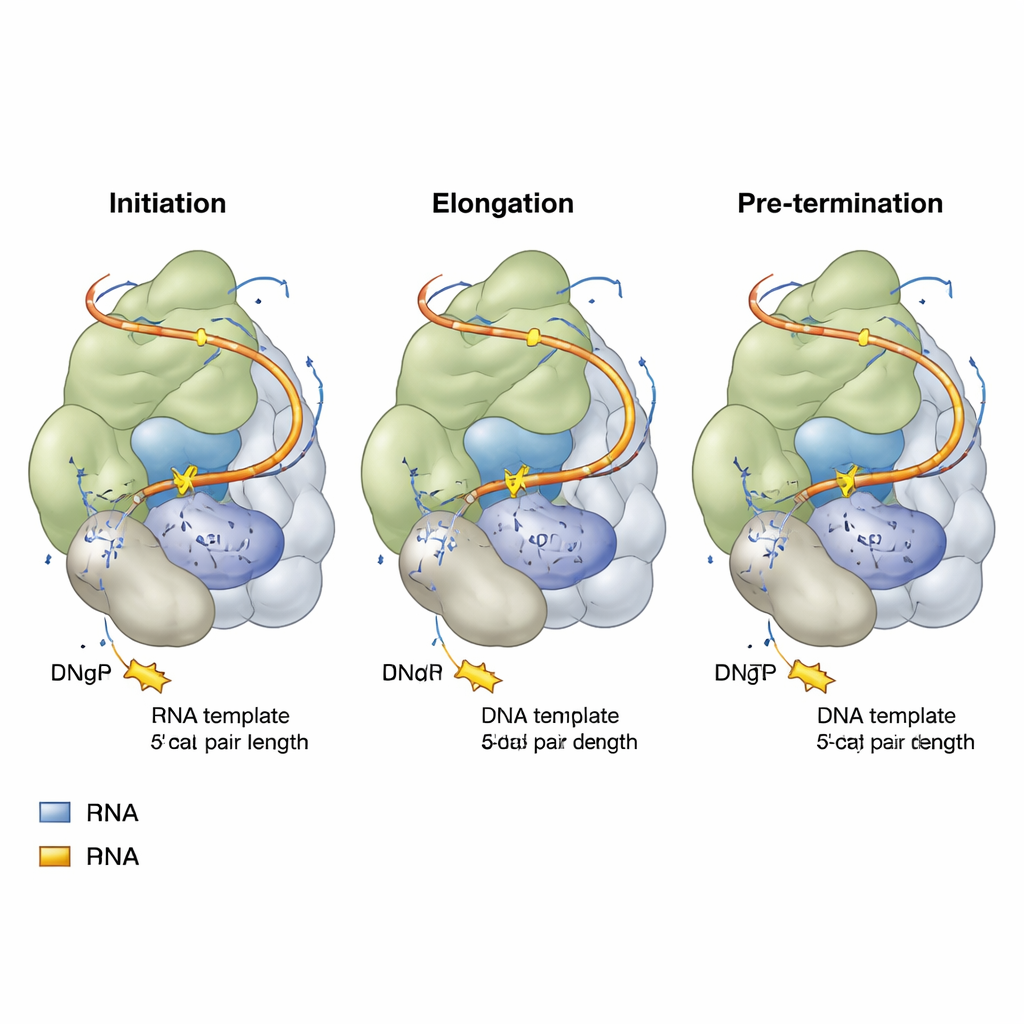
柔軟なRNAリンカーと可動部位
テロメラーゼ内のRNA鋳型は自由に浮遊しているわけではなく、5′および3′のテンプレートリンカーと呼ばれる両側の柔軟な伸長部で固定されています。テロメラーゼがイニシエーションからプレ終結へ進行するにつれて、上流側(5′)のリンカーはトランポリンのように引き伸ばされ、最終的に完全に伸びた状態に達して反復の終わりを知らせるのに寄与します。一方で下流側(3′)のリンカーは外側へ膨らみ、別のRNA構造(P6.1ステムループ)や近接するタンパク質領域に接近します。これらのリンカーが短すぎたり長すぎたり、あるいはP6.1が変化すると、テロメラーゼの反復付加能は急激に低下します。重要なのは、TENドメインやTRAPウェッジと呼ばれるテロメラーゼ特有の挿入部といったタンパク質領域が、DNAとこれらのRNAリンカーの両方に接触する調節可能なガイドとして働くことです。TRAPウェッジの体積を減らす変異は、逆に酵素をよりプロセッシブ(連続的)にする場合があり、このウェッジが通常は鋳型の移動のタイミングを制御する障壁として作用していることを示唆します。
治療標的への新たな洞察
構造的スナップショットと標的変異の機能試験を組み合わせることで、本研究はヒトテロメラーゼがどのように繰り返しテロメアを延長するかについての詳細な機械モデルを提案します。酵素は非常に短いDNA–RNAハイブリッドを保持し、ジッパー様の残基でその長さを強制し、柔軟なRNAリンカーと可動するタンパク質要素を利用して鋳型を前進させ、複数回の複製中もDNAを固定します。専門外の方への要点は、テロメラーゼは静的な複写機ではなく、幾何学と可動部がテロメアをどれだけ、どれくらい効率的に維持できるかを決める精密に調整されたバネ仕掛けの装置であるということです。この振る舞いを理解することは、がんでテロメラーゼを抑える薬や早老症などでその機能を安定化する薬の開発につながる可能性があります。
引用: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
キーワード: テロメラーゼ, テロメア, クライオ電子顕微鏡, ゲノム安定性, がん生物学