Clear Sky Science · ja
エーテル脂質は鉄の取り込みを調節してがん細胞の運命に影響を与える
ほとんど知られていない脂質ががんの弱点を露呈させる仕組み
がんはしばしば「遺伝子の病気」と表現されますが、本研究は細胞の外皮を構成する脂質が同じくらい重要になり得ることを示しています。研究者たちはエーテル脂質と呼ばれる特殊な脂質群が、どのようにして危険ながん細胞に周囲から鉄を取り込ませるかを明らかにしました—それは細胞の拡散能力を支えつつ、最近注目されている細胞死の形式に対する脆弱性も高めます。細胞膜、鉄、腫瘍の振る舞いの間に存在するこの隠れたつながりを理解することで、最も攻撃的ながん細胞を選択的に排除する新しい治療法への道が開けるかもしれません。
がん細胞を考える別の視点
多くのがん研究はDNAの変異とそれがコードするタンパク質に焦点を当てます。本研究は注意を細胞膜――すべての細胞を取り囲む薄い油状の殻――に向けます。その殻の中には形状や物理特性の異なる多種の脂質が存在します。著者らは多くの哺乳動物細胞のホスホリピドの約5分の1を占める一方で比較的研究が少なかったエーテル脂質に着目しました。高い転移能を持ち、幹様の性質を示すがん細胞は膜にエーテル脂質を多く詰め込み、膜の張力を低くし流動性を高めていることが見出されました。これらの物理的性質は、腫瘍の成長と鉄依存的な破壊過程であるフェロトーシスの双方を駆動しうる金属である鉄の取り込み方を変えます。
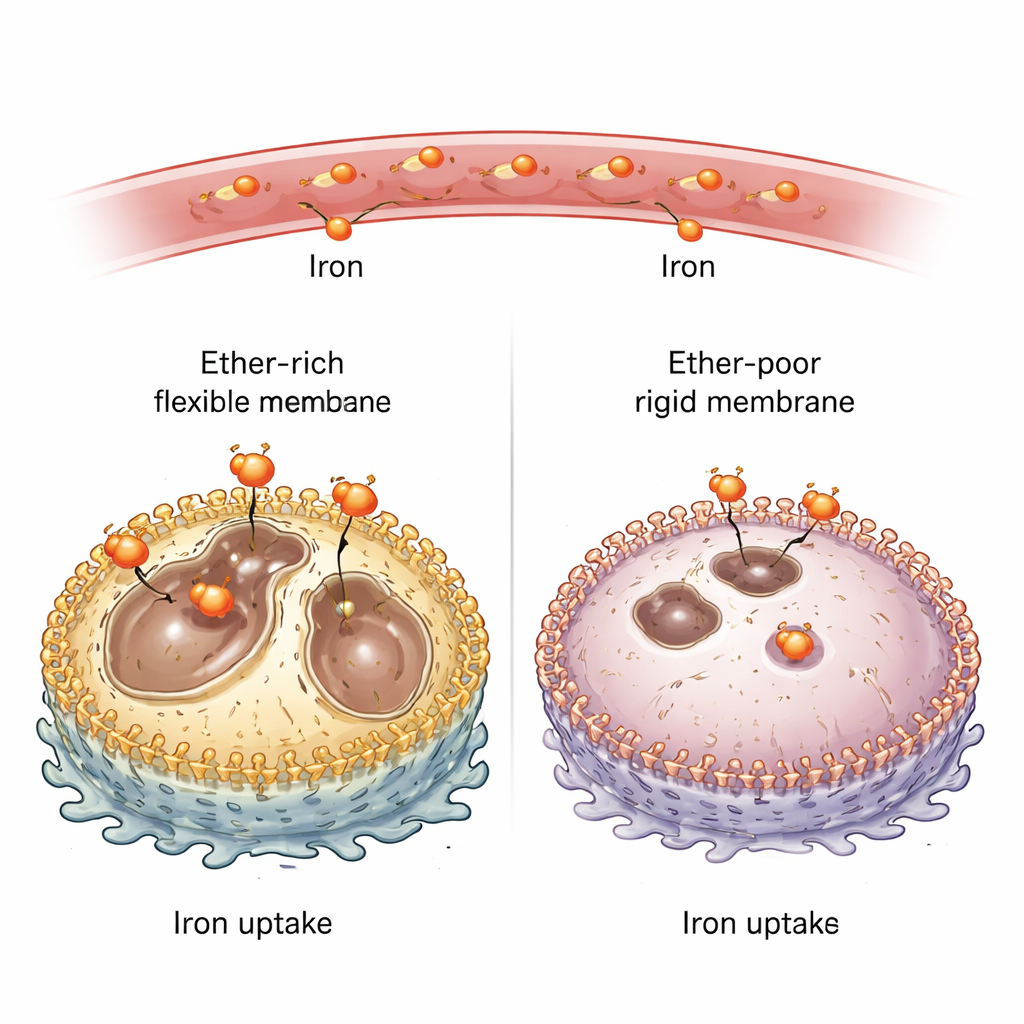
膜脂質と鉄の取り込みをつなぐ仕組み
エーテル脂質の役割を探るため、研究チームはマウスおよびヒトの複数のがん細胞株でそれらを合成するために必要な主要酵素を欠損させました。これらの酵素がないと、細胞膜中のエーテル脂質は全脂質の約4分の1から数パーセントへと急落しました。驚くべきことに、エーテル脂質が少ないこれらの細胞は、培養中でもマウスに移植した腫瘍でも、「酸化還元活性のある」鉄――酸化反応に関与する化学的に反応性の高い形態――を大幅に失っていました。外部から余分な鉄を与えると細胞内の鉄レベルは再び上昇し、フェロトーシスを誘導する薬剤に対する感受性を取り戻しました。これは、エーテル脂質が単に酸化の燃料として消費されるだけでなく、どれだけの鉄が細胞内に入るかを能動的に制御していることを示しています。
特殊な鉄の門:CD44経路
次に研究者たちは膜組成がどのように鉄の取り込みを変えるのかを問い直しました。細胞は通常、トランスフェリン受容体というよく知られたタンパク質を通じて鉄を取り込みますが、攻撃的で幹様のがん細胞はもう一つ別の経路にも依存しています:CD44という表面タンパク質で、ヒアルロン酸と呼ばれる糖分子に結合した鉄を引き込むものです。蛍光プローブを追跡することで、エーテル脂質を欠損させてもトランスフェリン受容体経由の取り込みにはほとんど影響しない一方で、CD44を介したエンドサイトーシス――クラシン依存でない代替的な物質取り込みルート――は著しく遅くなることが示されました。エーテル脂質を回復させるかリポソームとして付加すると、このCD44経路は再び機能を取り戻しました。CD44自体を阻害するかヒアルロン酸を分解すると細胞内鉄が低下し、このエーテル依存的な経路がこれらのがん細胞における主要な鉄の門であることが確認されました。
柔らかい膜が細胞の振る舞いを変える仕組み
なぜエーテル脂質が古典的な鉄受容体にはそれほど影響せず、CD44には大きな影響を与えるのでしょうか。答えは物理学にあります。細胞表面から小さなテザーを引き出す精密なツールを使って、著者らはエーテルに富む膜が張力が低く変形しやすいことを示しました。エーテル脂質を除去すると膜張力は増加し、脂質がより緊密に詰まり膜は硬くなりました。これらの変化は、柔軟でラフト様の膜パッチに依存する形態のエンドサイトーシスを著しく妨げます――まさにCD44が利用する種類の取り込みであり、クラシン依存の取り込みにはほとんど影響を与えませんでした。エーテル脂質はまた、CD44が内向きに引き込まれる前に集まる膜中の小さな秩序だった島である「リピッドラフト」を安定化するのにも寄与しました。要するに、エーテル脂質は膜の物理的な地形を調節してCD44駆動の鉄取り込みを促進しているのです。
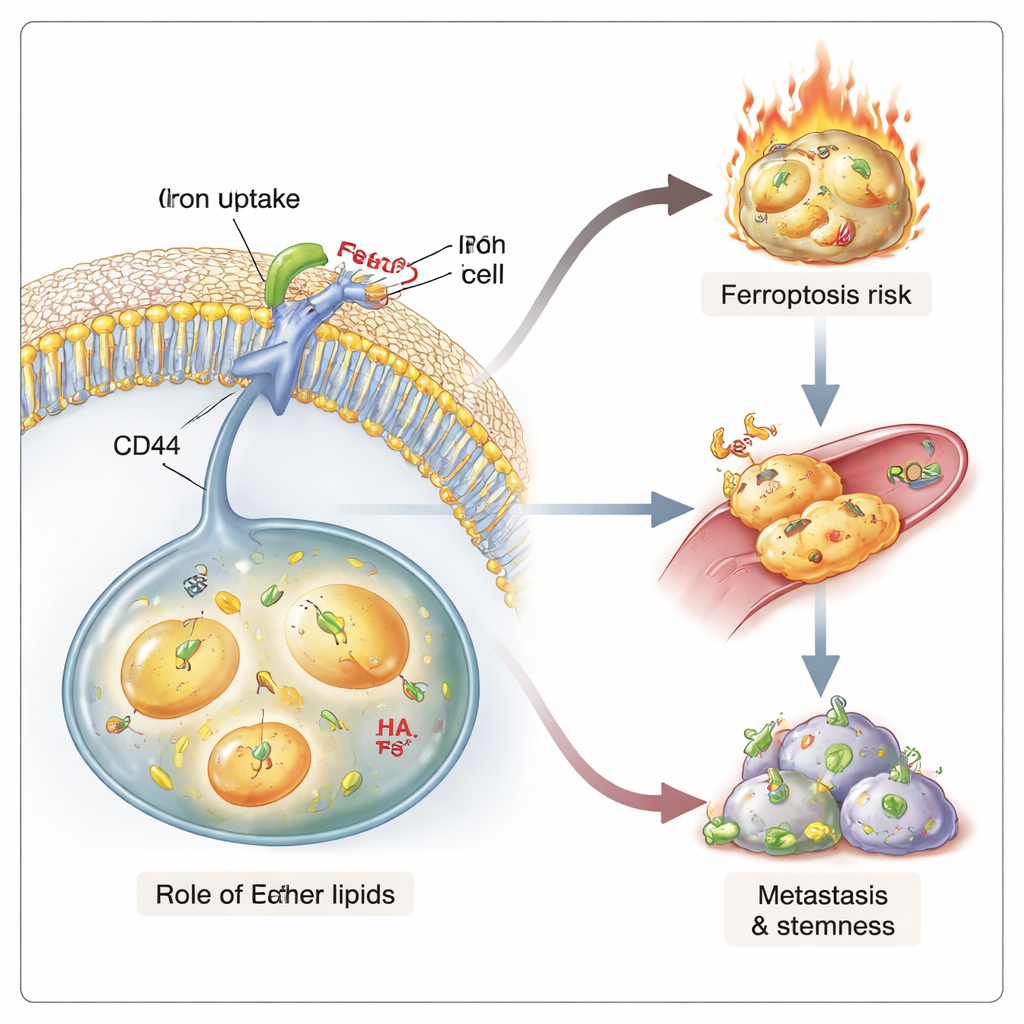
拡散と自己破壊の両方を促す燃料
高い鉄レベルと低い膜張力は、がんを致命的にする性質と結びついています:新しい腫瘍をまく能力や治療を生き延びる能力です。三次元の微小血管モデルでは、エーテルに富むがん細胞は血管様構造からより容易に押し出され――転移の早期段階――ました。マウスでは、エーテル欠損のがん細胞は原発腫瘍の増殖速度が同程度であっても転移が少なくなりました。これらの細胞は培養でのマンノスフェア形成能や限定希釈移植での腫瘍起始能の低下から示されるように、「幹様性」も低下していました。同時に、エーテルに富む細胞はより高い鉄負荷と酸化されやすい脂質を抱えているため、特定の薬剤や免疫シグナルで挑戦されるとフェロトーシスを受けやすくなっていました。したがって、エーテル脂質は二面性を作り出します:攻撃的で幹様の振る舞いを支える一方で、同じ細胞を鉄駆動の脂質損傷によって特異的に殺し得る状態にもしているのです。
将来のがん治療にとっての意義
専門外の方への要点は、すべてのがん細胞が同じように危険というわけではなく、その外膜がその危険度と脆弱性の双方を決める助けになるということです。エーテル脂質は細胞表面を再構築して、鉄が特殊な出入口を通じて流れ込みやすくし、転移性で幹様の細胞にエネルギーを与える一方で自己破壊の材料も蓄えさせます。エーテル脂質の生成を変える、CD44に基づく鉄取り込みを妨げる、あるいは慎重にフェロトーシスを誘導する治療は、正常組織を温存しつつ治療が難しい細胞集団を選択的に標的にする可能性があります。ほとんど知られていなかった脂質のクラスが膜の物理、金属代謝、細胞運命をつなぐことを明らかにすることで、本研究はより賢明で精密ながん介入に向けた新しい道を開きます。
引用: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
キーワード: エーテル脂質, がん幹細胞, 鉄の取り込み, フェロトーシス, 転移