Clear Sky Science · ja
パルミチン酸が引き起こすB7H3のパルミトイル化は免疫逃避を促進する
この研究ががん患者にとって重要な理由
新しい免疫療法薬が免疫系によるがん攻撃を助けると聞いたことがある人は多いですが、一般的な結腸直腸(大腸)がんの多くの患者はほとんど恩恵を受けていません。本研究は、結腸直腸腫瘍が免疫攻撃から身を守るために使う隠れた生化学的トリックを明らかにし、免疫療法の効果を高め得る新しいタイプの薬剤、短いペプチドを示唆します。
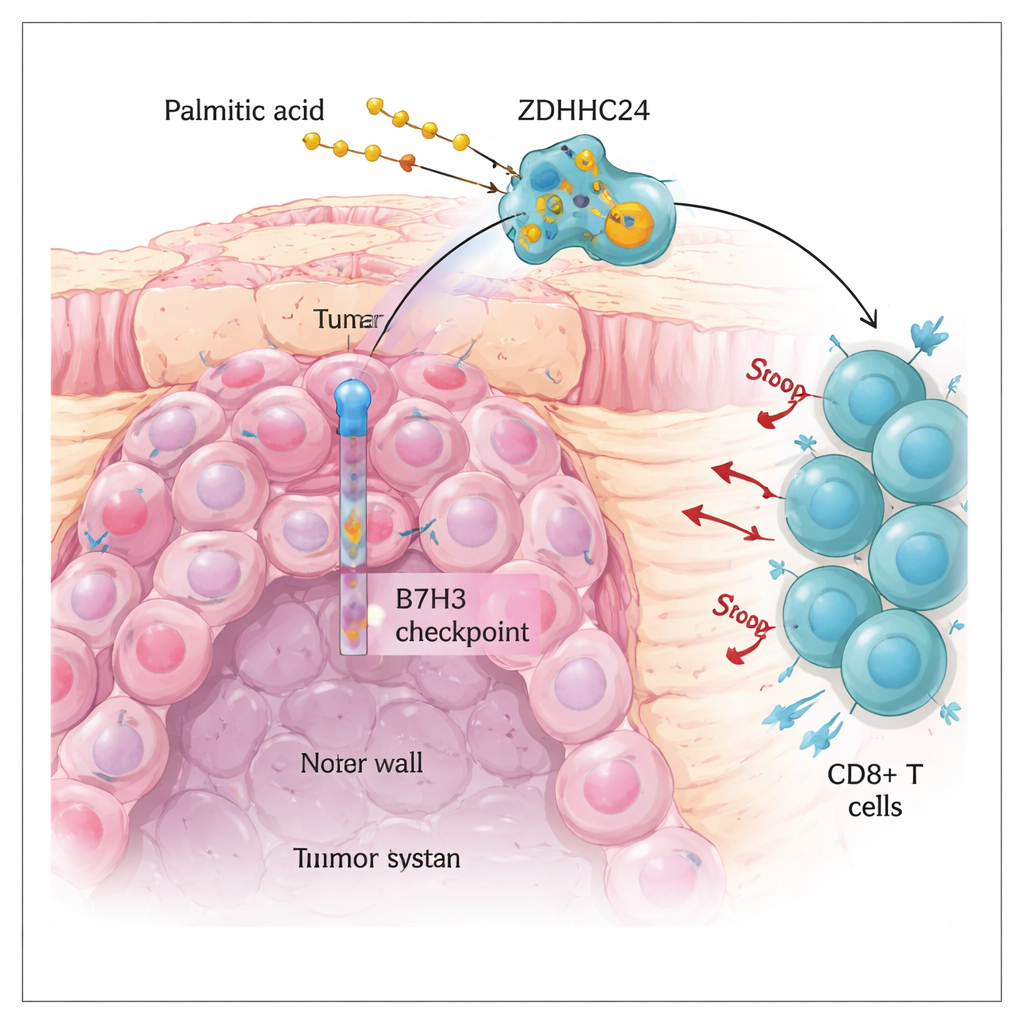
現在の大腸がん免疫療法における障壁
結腸直腸がんは世界で最も一般的ながんの一つです。PD-1やPD-L1阻害剤のような免疫の“ブレーキ”を解除する免疫療法は、DNA変異が多い、いわゆるMSI-H腫瘍を持つ一部の患者の治療を一変させました。しかし残念ながら、大多数の結腸直腸がんはマイクロサテライト安定型(MSS)であり、これらの治療に対する反応は乏しいです。著者らは、腫瘍細胞表面に存在してキラー免疫細胞、特にCD8+ T細胞の活性を抑える別のブレーキ分子B7H3に着目しました。彼らは、B7H3タンパク質がMSS腫瘍で強く上昇しており、生存率の悪化と結びついていることを見出しましたが、基になるB7H3遺伝子の発現は高くありませんでした。この不一致は重要な疑問を示しています:腫瘍細胞上でB7H3タンパク質がなぜこれほど豊富に保たれているのか?
一般的な脂肪が腫瘍の隠れ蓑を助ける仕組み
研究チームは、腫瘍代謝がB7H3の安定化に寄与しているのではないかと疑いました。MSSとMSI-Hの結腸直腸腫瘍の遺伝子発現と小分子プロファイルを比較したところ、多くの脂質関連経路に差があり、その中でパルミチン酸という脂肪酸が際立ちました。培養下で結腸がん細胞を複数の脂肪分解産物に曝露したところ、B7H3タンパク質レベルを明確に上昇させたのはパルミチン酸だけでした。追加実験により理由が示されました:パルミチン酸はパルミトイル化と呼ばれる化学修飾に供され、脂肪鎖が特定のタンパク質部位に付加されます。この修飾はZDHHC24という酵素によりB7H3の単一のシステイン残基で行われ、B7H3をより安定にし、腫瘍細胞表面での存在量を増やしました。
免疫ブレーキの“ゴミ捨てルート”を遮断する
細胞は通常、不必要や損傷したタンパク質をリサイクルやゴミ処理のようなシステムで除去します。研究者らは、B7H3が主にオートファジーと呼ばれる細胞の“自食”経路で分解され、SQSTM1/p62という受容体タンパク質が破壊対象のタグ付けに使われることを示しました。B7H3がパルミトイル化されると、この受容体への結合が弱まり、オートファジーによる分解を免れてしまい、免疫ブレーキが持続的に高いレベルで維持されました。パルミトイル化部位を変異させて脂肪タグを付けられなくしたり、ZDHHC24酵素を欠失させると、B7H3はより効率的に細胞の“ゴミ袋”へ送られて分解されました。マウスでは、パルミトイル化されたB7H3を欠く腫瘍は成長が遅く、免疫欠損動物では本来の増殖速度を変えず、腫瘍内に著しく多くのCD8+ T細胞と強い腫瘍殺傷活性を示しました。これはこの修飾が主に免疫を無力化することで作用し、がん細胞の増殖速度自体を変えるわけではないことを示しています。
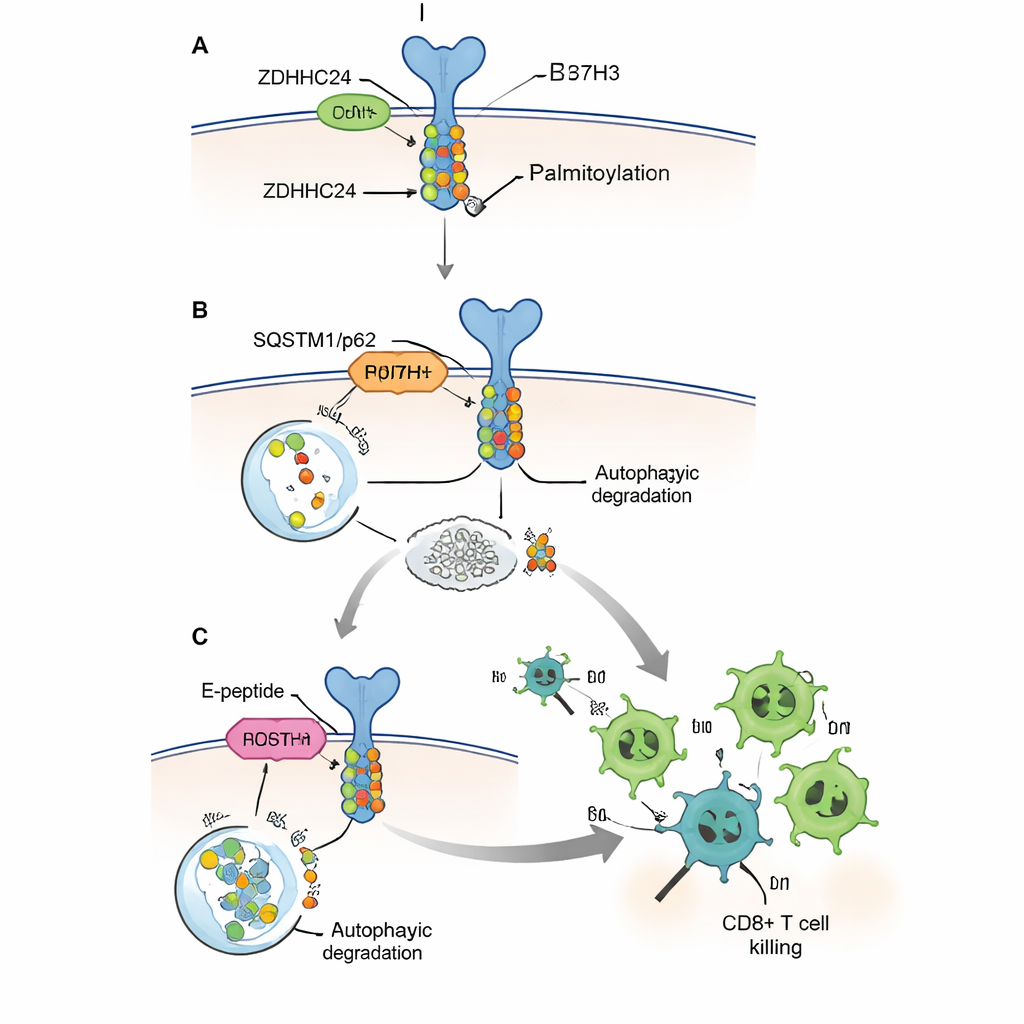
盾を弱め、T細胞を増強する
ZDHHC24やB7H3を遺伝学的に完全に除去することは患者治療には現実的でないため、著者らはEペプチドと名付けた短く細胞透過性のペプチドを設計しました。これは本来ZDHHC24に結合するB7H3の短い配列を模したデコイで、酵素が実際のB7H3分子を修飾するのを妨げます。培養細胞ではEペプチドはB7H3のパルミトイル化とタンパク質レベルを低下させ、オートファジー機構による認識を回復させ、人間のCD8+ T細胞が腫瘍細胞をより効率的に殺すことを可能にしました。ヒトの免疫細胞とヒトの結腸直腸腫瘍を持つヒト化マウスを含む複数のマウスモデルで、Eペプチド投与は腫瘍を縮小させ、腫瘍内のCD8+ T細胞数を増やし、グランザイムBやインターフェロンγなどの主要なキラーモレキュールの産生を高めました。
既存の免疫療法の新たな協働相手
最後に、著者らはこの戦略が標準のPD-1阻害と併用できるかを検討しました。大腸がんのマウスモデルでは、Eペプチド単独も抗PD-1抗体単独もある程度の腫瘍制御を示しました。しかし併用すると、両治療ははるかに強力で持続的な腫瘍抑制をもたらし、場合によっては腫瘍が消失し、平均生存が対照と比べて二倍以上に延長しました。これは脂肪の“錨”を切ってB7H3の盾を無力化することが、PD-1経路を標的とする既存のチェックポイント薬を補完し得ることを示唆しています。
将来のがん治療にとっての意味
端的に言えば、本研究は一般的な食事由来の脂肪であるパルミチン酸が結腸直腸腫瘍に乗っ取られ、免疫抑制タンパク質B7H3を化学的に装甲化してがんが隠れるのを助けうることを示しています。その単一の化学的付着を遮断することで、著者らは装甲を剥がし、細胞自身の廃棄システムにB7H3を除去させ、CD8+ T細胞が攻撃する道を再び開くことができました。Eペプチド自体は初期段階の実験ツールに過ぎませんが、本研究はB7H3のパルミトイル化とその酵素ZDHHC24を有望な薬剤標的として同定しています。同様の薬剤が人で安全かつ有効であることが示されれば、将来的により多くの結腸直腸がんを免疫療法に反応する“寒い”腫瘍から免疫が認識して破壊できる“熱い”腫瘍へと変える可能性があります。
引用: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
キーワード: 結腸直腸がんの免疫療法, B7H3チェックポイント, パルミチン酸代謝, タンパク質パルミトイル化, CD8T細胞の腫瘍免疫