Clear Sky Science · ja
急性骨髄性白血病におけるGPX4依存および非依存フェロトーシス監視を制御するマスターレギュレーターとしてのTET1
なぜこの研究ががん治療に重要なのか
多くの新しいがん薬は、悪性細胞を鉄と脂質損傷に駆動される細胞死の形態であるフェロトーシスへと誘導することを狙っています。しかし一部の腫瘍はこのアプローチに頑強に抵抗します。本研究は、TET1というDNAの化学的修飾を行うタンパク質が、白血病細胞を二つの別個の生化学的防御系を通じてフェロトーシスから逃れさせる仕組みを明らかにし、これらの防御を阻害すれば抵抗性のがんも脆弱にできることを示しています。
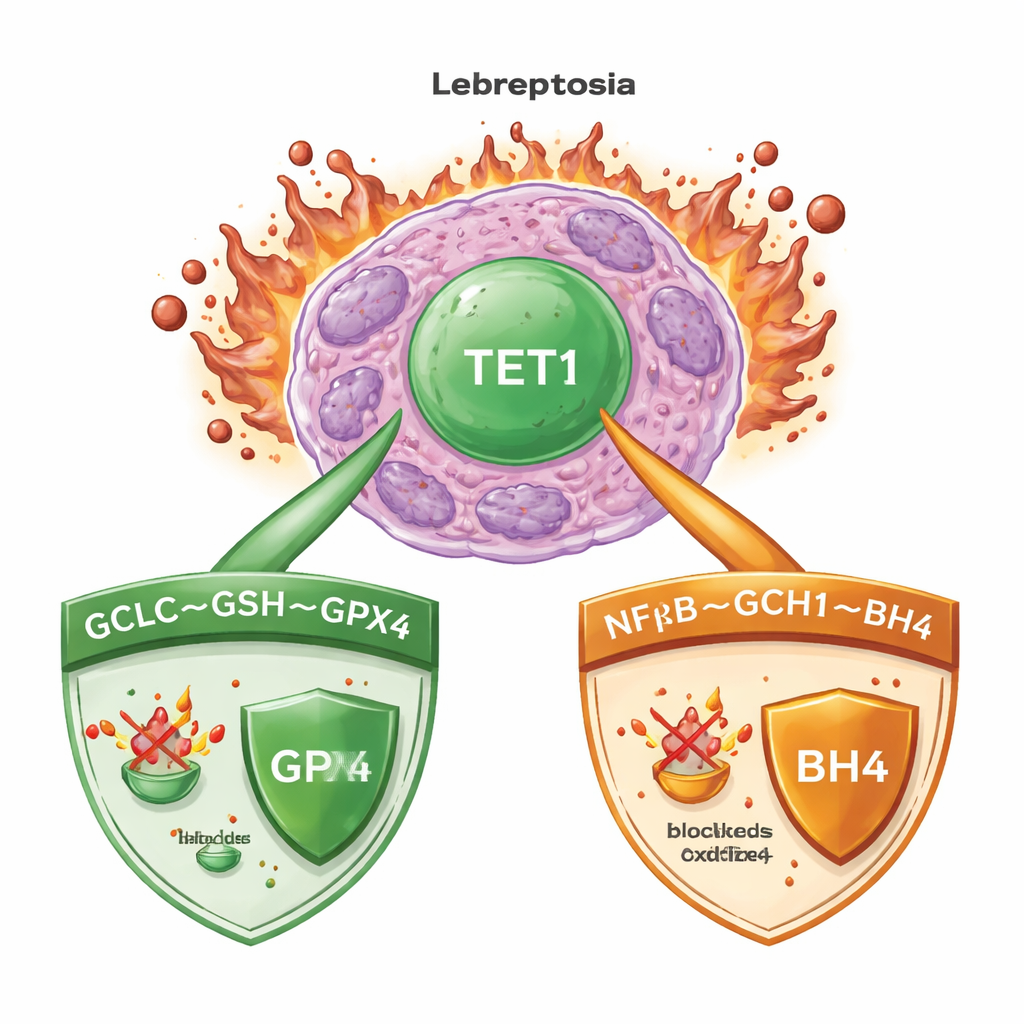
鉄と損傷した脂質の致命的な組み合わせ
フェロトーシスは、鉄が細胞膜の脂質の制御不能な酸化を促進し、最終的に細胞が破裂することで起こります。急性骨髄性白血病(AML)では、ほかの多くのがんと同様に、この過程を抑える強力な監視システムが働いています。主要な守護因子の一つが酵素GPX4で、これはグルタチオンという小分子を使って有害な脂質過酸化物を中和します。GPX4が損なわれた場合でも、代替のバックアップ系が抗酸化分子を生成して危険なラジカルを捕捉します。どのマスタースイッチがこれらの防御を統括するかを理解することは、正常組織を守りつつ確実にがん細胞でフェロトーシスを誘導する治療法設計にとって重要です。
TET1が中心的な制御ハブとして浮上する
研究者らは多数のがん細胞サンプル(多くのAML系統や患者由来細胞を含む)を比較し、明確なパターンを見出しました:フェロトーシスに抵抗する細胞はTET1の発現が高いということです。TET1はDNAの化学的マークを変化させ遺伝子発現に影響を与える酵素です。遺伝学的手法でTET1量を減らすか、低分子でその活性を阻害すると、がん細胞はフェロトーシス誘導薬に対して著しく感受性を増しました。これは培養皿内でもAMLマウスモデルでも同様でした。逆にTET1の発現を高めると、細胞はフェロトーシス性の死から保護され、膜損傷を引き起こす活性酸素種の蓄積が抑えられました。
主要な抗酸化シールドの強化
さらに解析を進めると、TET1がゲノム上のどこで働くかをマッピングした結果、TET1がGCLCという遺伝子を直接活性化していることが分かりました。GCLCはグルタチオン生合成を開始する重要な酵素をコードしています。TET1はGCLCプロモーター領域の特定のDNAマーク(5-ヒドロキシメチルシトシン)を増やすことでグルタチオン合成を上げます。通常の栄養条件下ではこれにより細胞の主要な抗酸化プールが増強されます。シスチン欠乏下では同じ酵素複合体が異常なγ-グルタミルペプチドを生成し、過剰なグルタミン酸を掃除してフェロトーシスを緩和します。培養細胞とマウスの双方で、TET1の喪失や薬理的なグルタチオン合成阻害はグルタチオンおよびこれらの保護ペプチドを急激に低下させ、白血病細胞をフェロトーシス誘導因子に対してはるかに脆弱にしました。
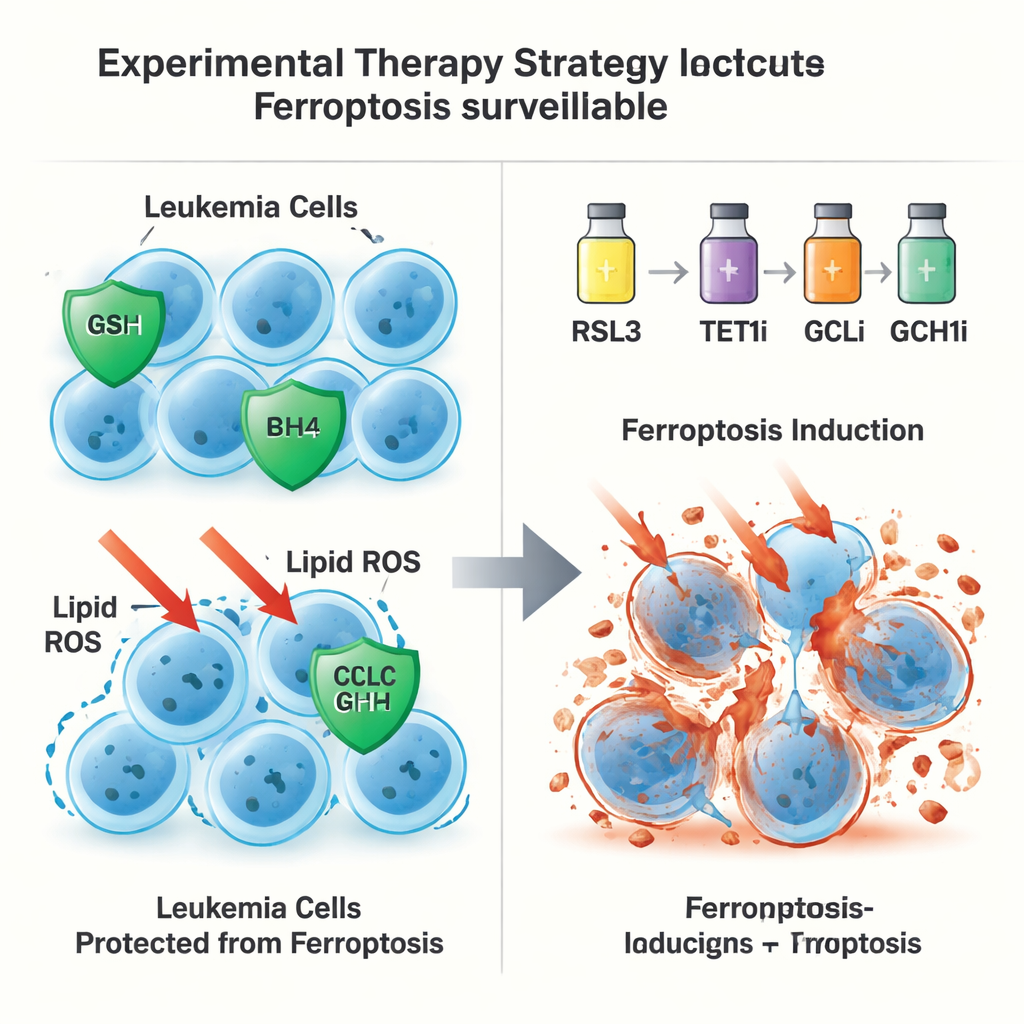
第二の、GPX4に依存しない逃避経路
驚くべきことに、TET1の保護的役割はグルタチオン–GPX4軸だけにはとどまりませんでした。GPX4自体を白血病細胞から除去しても、TET1を余分に持つと依然としてフェロトーシス死を防げる場合があり、第二の防御線の存在を示唆しました。著者らはこれをTET1がNFκBシグナル伝達経路、特にNFKB2という成分を活性化することに起因すると辿りました。これがさらにGCH1の発現を増加させ、GCH1は抗酸化分子BH4を生成します。BH4はGPX4に依存せずに膜脂質の酸化から保護できます。GCH1を遺伝的にサイレンシングするか化学的に阻害すると、TET1が細胞をフェロトーシスから守る能力は部分的に失われました。これらの結果は、TET1–NFKB2–GCH1経路がGPX4非依存のフェロトーシス監視システムを形成することを示しています。
弱点を治療機会に変える
この二重経路の地図を手に、研究者らはフェロトーシスを同時に促進しTET1制御の防御を弱めることで治療上の利点が得られるかを検証しました。マウスAMLモデルおよびマウスへの患者由来白血病移植片において、低用量のフェロトーシス誘導薬をTET1阻害剤、GSH合成阻害(GCLC経由)、またはGCH1阻害剤と組み合わせると、白血病負荷が劇的に減少し、生存が延長し、白血病始原細胞集団が枯渇しました。重要な点として、フェロトーシス誘導薬は以前の報告よりもはるかに低用量で用いられ、正常な造血幹細胞への毒性に関する懸念が軽減されました。
今後のがん治療に向けての意義
専門外の読者に対する主要メッセージは、白血病細胞はTET1により調整される二つの重なる抗酸化“盾”システムを運用して生き延びているということです:一つはグルタチオンとGPX4を中心とする系、もう一つはGCH1とBH4に基づく系です。本研究は、フェロトーシスを穏やかに活性化しつつTET1とその下流パートナーを阻害することで、抵抗性を克服し正常組織を過度に傷つけずにがん細胞を選択的に死に追いやる可能性があることを示しています。これらの戦略はまだ臨床適用には至っていませんが、本研究はTET1を強力な制御ノードかつAMLや他の治療困難ながんに対する組み合わせ療法の有望な標的として特定しています。
引用: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
キーワード: フェロトーシス, 急性骨髄性白血病, TET1, グルタチオン, がんエピジェネティクス