Clear Sky Science · ja
多段階ラジオ免疫療法を操る現場で自己組織化する細胞リザーバーゼリー(ハイドロゲル)
放射線をより賢いがん治療へと変える
放射線療法はがん治療で最も広く使われる手段の一つですが、腫瘍は免疫系から隠れることで生き残ったり、低酸素(低酸素状態)で増殖して放射線の効果を鈍らせたりします。本研究は、腫瘍内で直接形成される注入型の“スマート”ハイドロゲルについて記載します。これは小さな薬剤工場かつ酸素発生装置として機能します。放射線と、タイミングを制御した免疫刺激シグナルの双方を腫瘍に供給することで、治療が難しいがんを体自身の防御機構が認識して破壊できるようにすることを目指しています。
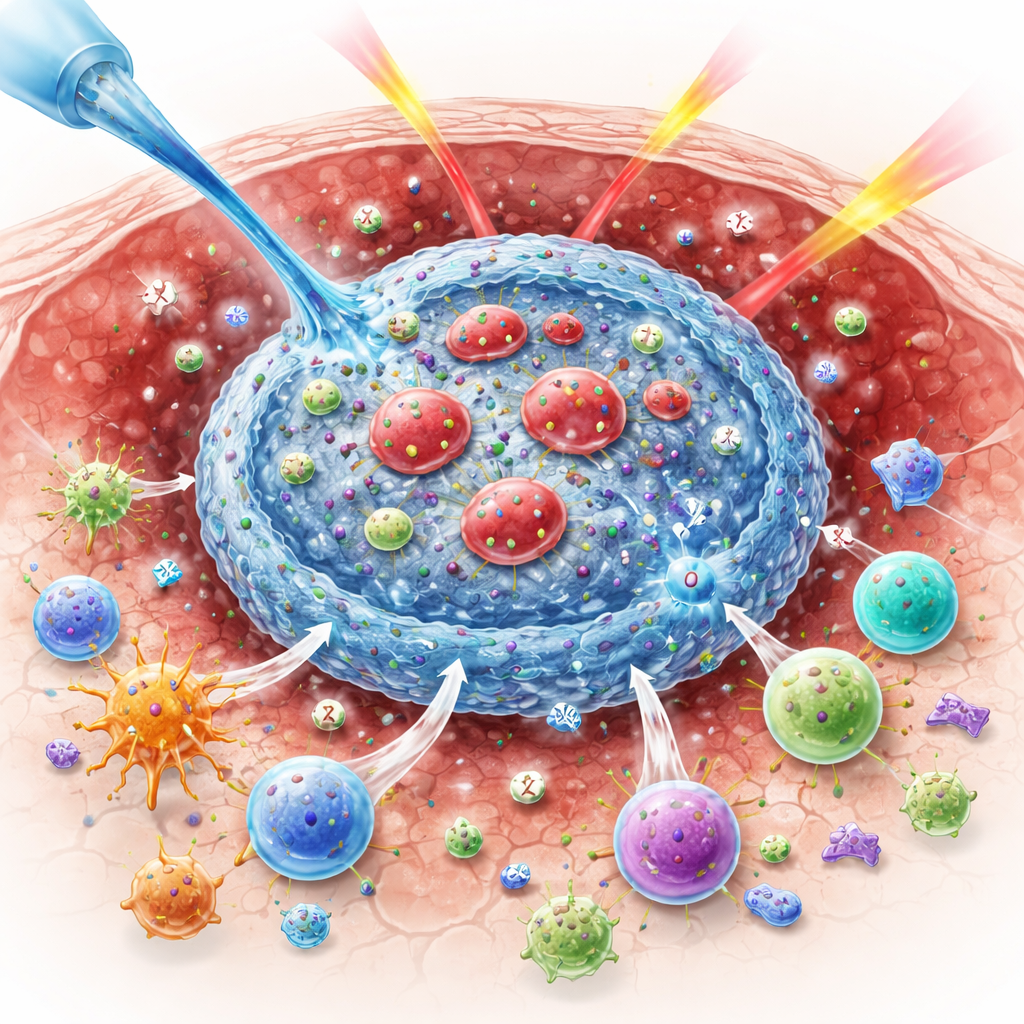
なぜ酸素が腫瘍制圧に重要なのか
放射線は、DNAを切断する反応性の高い酸素分子を生成することでがん細胞を死滅させます。腫瘍が酸素不足に陥るとこの化学反応は非効率になり、多くのがん細胞が生き残ります。同時に、放射線は免疫系に対して相反する信号を送ります。腫瘍タンパク質を露出させてがんを危険なものとして示す一方で、CTLA-4のような免疫細胞の“ブレーキ”を強めたり、攻撃を抑える制御性T細胞を優位にしたりもします。こうした相反する効果が、放射線と免疫薬の併用がマウスではうまくいっても患者では常に同様の効果を示さない理由を説明します。
腫瘍内で構築される生きたゲル
研究者らは、腫瘍の酸性環境でのみ自己組織化する材料を設計しました。これは三つの主要成分で構成されています:アルギン酸と呼ばれる天然の糖由来ポリマー、過酸化バリウムという無機粉末、そして二つの免疫薬を運ぶように穏やかに改変された赤血球です。混合物を腫瘍に注入すると、酸性条件によって過酸化バリウムが分解し、バリウムイオンと過酸化水素が放出されます。バリウムイオンは即座にアルギン酸を架橋して柔らかなハイドロゲルを形成し、改変赤血球をその場に閉じ込めて薬剤の流出を防ぎます。同時に、赤血球内に自然に存在する酵素が過酸化水素を酸素に変換し、腫瘍の低酸素状態を緩和して放射線の効果を高める準備をします。
二段階の免疫シグナルの時間差放出
このシステムの真の力は、二つの免疫因子の放出を段階的に行う点にあります:CTLA-4を阻害する抗体と、インターロイキン-12(IL-12)というサイトカインです。抗体は赤血球の内側に搭載され、IL-12は赤血球の表面に固定されています。酸素が生成されると赤血球膜に孔が開き、CTLA-4阻害抗体が速やかに放出されます。この早期の放出により免疫抑制が解除され、樹状細胞が腫瘍抗原を近傍のリンパ節へ運び、腫瘍特異的なT細胞の活性化を助けます。一方でIL-12はハイドロゲルの構造が徐々に緩むにつれてゆっくりと漏れ出します。この遅れて現れるシグナルはT細胞やナチュラルキラー細胞にインターフェロン-γ産生を促し、殺傷系細胞のさらなる腫瘍への動員を支え、免疫の監視役と効果役の間に正のフィードバックループを強化します。
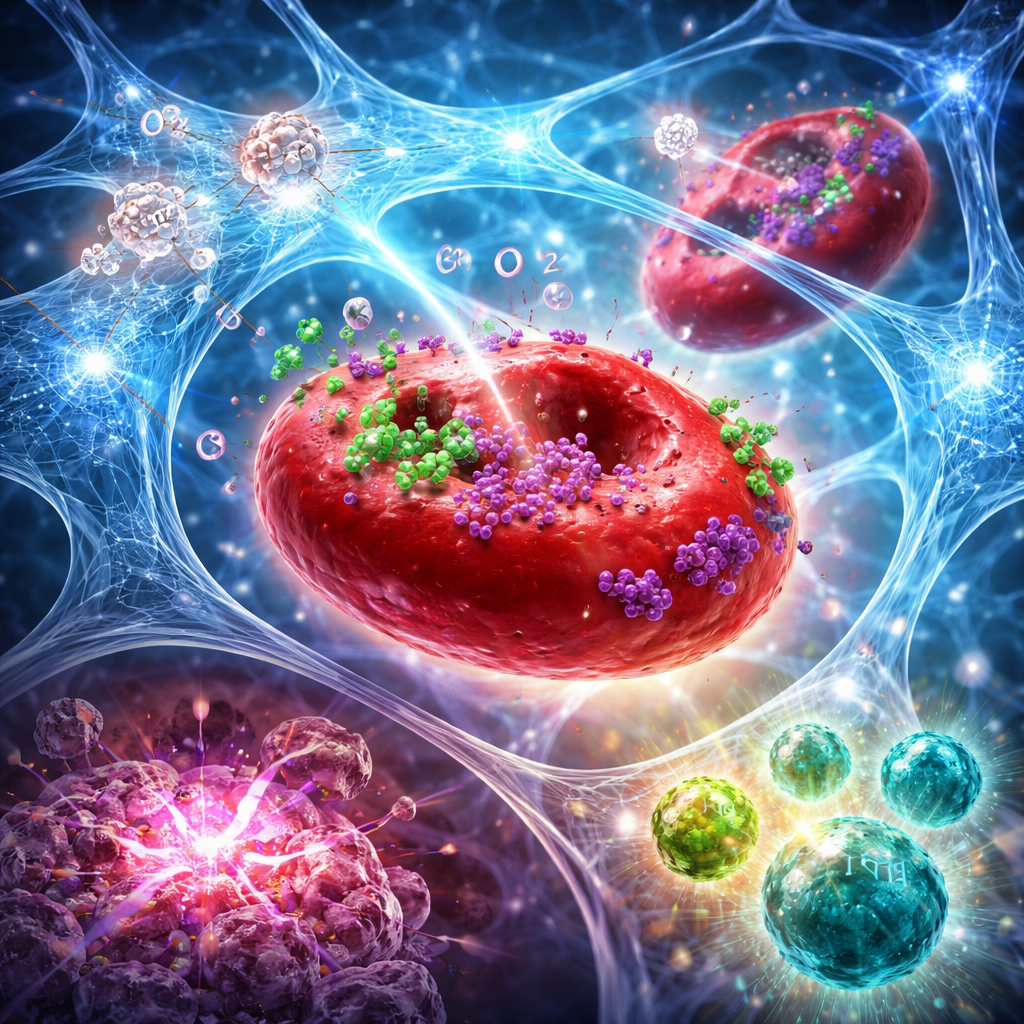
局所注入から全身の免疫攻撃へ
攻撃性の高い乳がんおよび膵臓がんのマウスモデルでは、このハイドロゲルと集中的な放射線を組み合わせることで、治療部位の腫瘍を縮小する以上の効果が得られました。結合治療は腫瘍内の酸素レベルを数日間上昇させ、放射線によるDNA損傷を増幅し、免疫による認識を誘う形の細胞死を強く誘導しました。フローサイトメトリーや組織染色は腫瘍微小環境の明確な変化を示しました:細胞傷害性のCD8陽性T細胞とナチュラルキラー細胞の増加、制御性T細胞の減少、そして“効果”細胞対“抑制”細胞の比率の上昇です。リンパ節における特殊な樹状細胞の増加は抗原提示の改善を示しています。多くのマウスで腫瘍が完全に退縮し、数週間後にがん細胞を再導入しても再発が抑えられる個体もあり、持続的な免疫記憶が形成されたことを示唆します。
安全性、実用性、今後の展望
ゲルは局所で形成され薬剤を保持するため、IL-12や抗CTLA-4が血流中に漏れる量はわずかであり、これらの因子が過去に問題にしてきたサイトカインストームや臓器障害のような重篤な副作用のリスクは低くなります。構成要素であるアルギン酸、赤血球、過酸化バリウムは比較的安価でスケールしやすく、この戦略が異なるがん種へ応用できる可能性を高めます。製造、品質管理、深部あるいは広範囲に広がる腫瘍への投与に関する課題は残るものの、本研究は放射線と精密に時刻を合わせた免疫活性化を同期させる有望な方法を示しており、物理的療法を全身性の抗腫瘍免疫を引き起こすトリガーへと変える可能性を示しています。
患者にとって何を意味するか
日常語で言えば、本研究は放射線と免疫薬を別々に投与して両者が協調することを期待するのではなく、それらを腫瘍内に置かれるスマート材料にまとめ、酸素を自ら作り、免疫シグナルを慎重に調整された順序で放出させることを示唆しています。動物実験では、このアプローチは放射線のがん細胞に対する致死性を高めただけでなく、免疫系に腫瘍を認識し記憶させることで再発を防ぐ手助けもしました。人間でも同様の成果が得られれば、このようなハイドロゲルは難治性の腫瘍を体自身の防御が確実に検出し破壊できる標的へと変える可能性があります。
引用: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
キーワード: ラジオ免疫療法, ハイドロゲル, がん免疫療法, 腫瘍微小環境, 放射線療法