Clear Sky Science · ja
DNA複製ネットワークにおける連続的に調節可能な多安定性
単純なスイッチから多数の可能な状態へ
分裂する細胞や発生中の胚に至るまで、生体システムは単にオンかオフかのライトスイッチのように動作することはまれです。むしろ、ディマー(調光)スイッチのように無数の位置で長時間留まれるような、多様な持続的状態をとることが多い。今回の論文は、まさにそのディマーに似た振る舞いを示すDNAベースの化学ネットワークを報告します。つまり、いくつかの離散的な状態だけでなく、実質的に連続的なスペクトルに沿った任意の組成を安定に保持できるのです。この能力は、将来のスマート材料、分子メモリ、デジタルだけでなくアナログ情報を処理する生化学的コンピューティングの強力な基盤になる可能性があります。
なぜ多重安定状態が重要か
幹細胞の分化、細胞の自殺(アポトーシス)、あるいは遺伝子ネットワークが過去の信号を記憶するかどうかといった多くの細胞の意思決定は、同じ条件下で複数の安定な活動パターンのいずれかに留まれる「多安定性」に依存しています。従来の合成的アプローチは、遺伝子回路、酵素、あるいは相互にオン・オフを切り替えるDNA鎖から構築されてきましたが、これらの設計は通常、二値の古典的な双安定スイッチのような限られた離散的な結果しか生みません。状態数Nのシステムを拡張するには概ねN×(N−1)個の慎重に調整された抑制結合が必要になり、しかもシステムは滑らかな連続体ではなく少数の固定点の間を跳ね回るだけになりがちです。
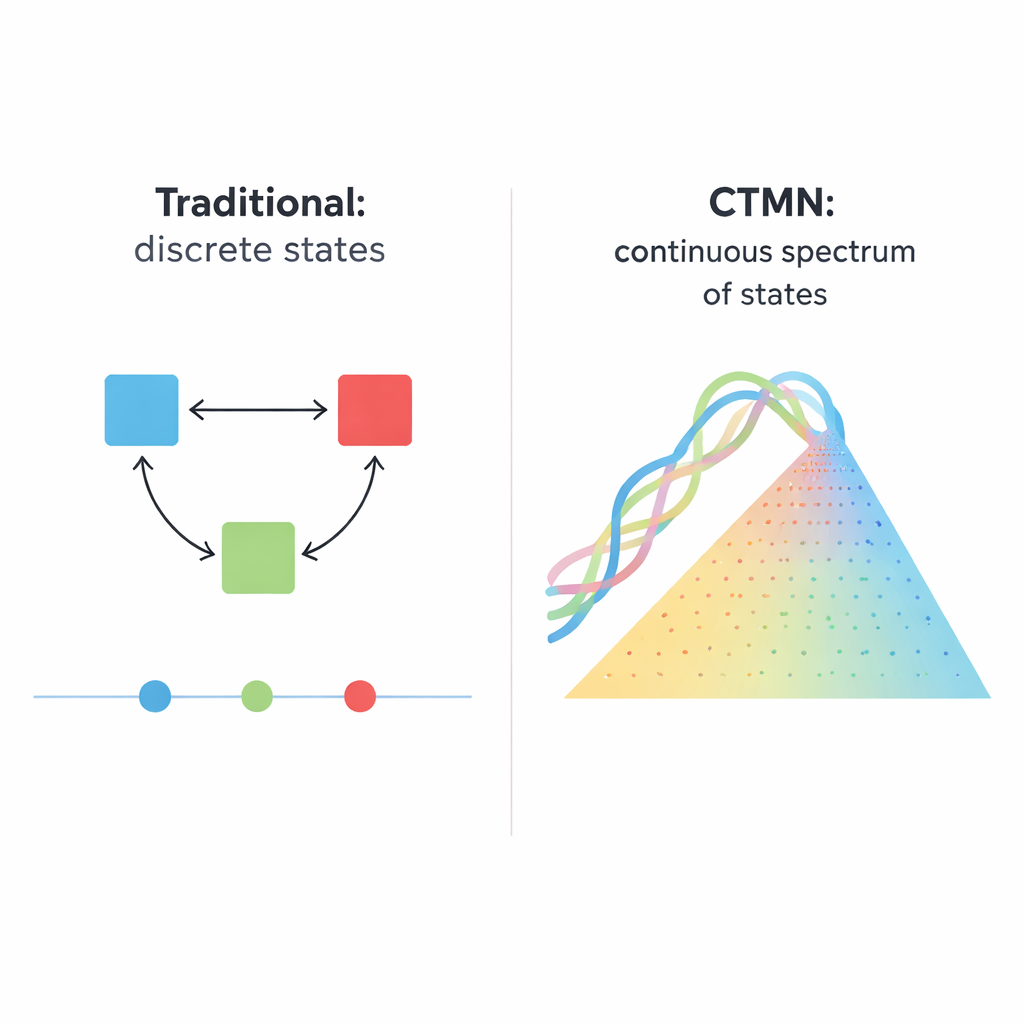
新しいタイプのDNAネットワーク:連続的に調節可能
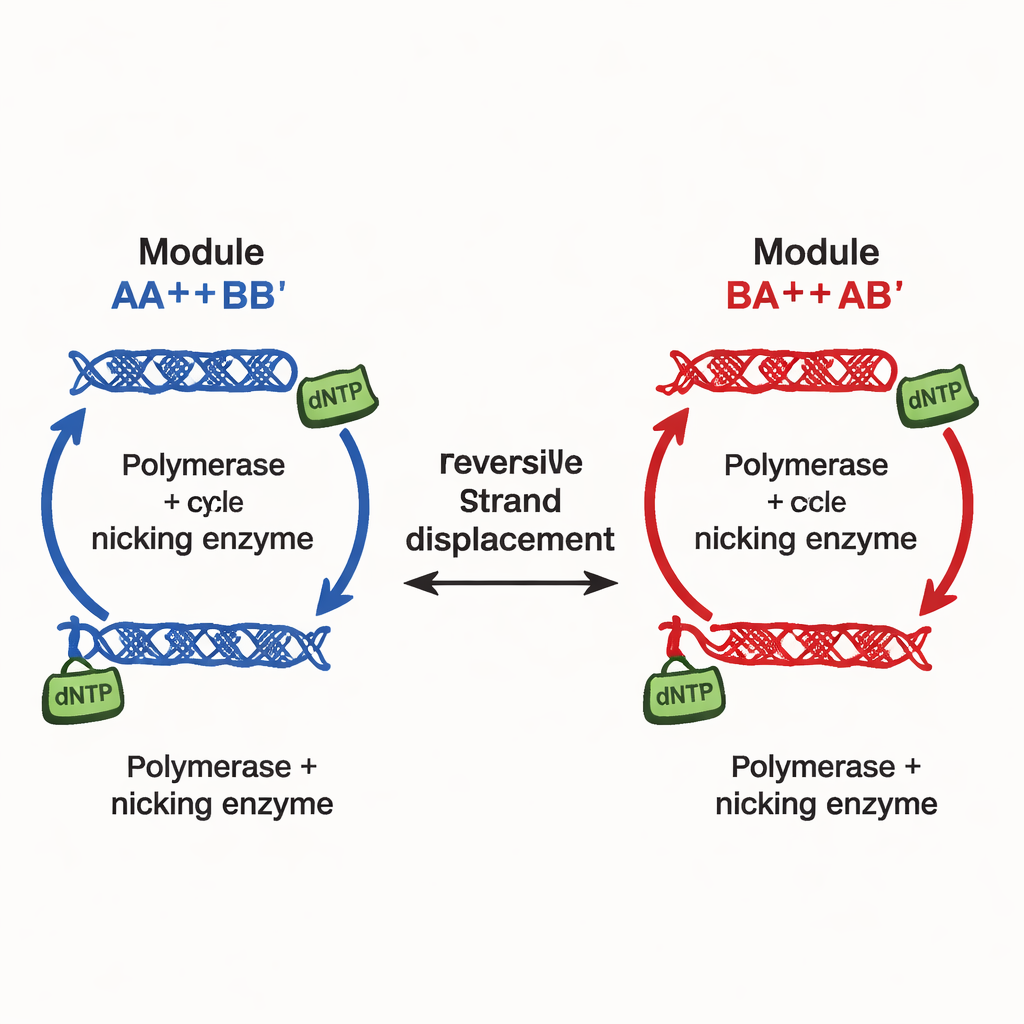
著者らは「連続的に調節可能な多安定性ネットワーク(CTMN)」と呼ぶ、異なる設計原理を導入しました。多数の個別抑制信号に頼る代わりに、可逆的なストランド交換反応で結ばれたDNA複製モジュール間の直接競合を利用します。各モジュールは設計されたDNA二本鎖からなり、ストランド置換に参加できるだけでなく、ニッキング酵素により切断・再生される重要な断片を伴ってDNAポリメラーゼの鋳型にもなります。化学的燃料であるdNTP(ヌクレオチドの供給)が重合とニッキングを駆動し、系を平衡から遠くに保ちます。この条件下で競合するモジュールは、初期の相対的割合に「凍結」するように振る舞い、二つや三つの結果ではなく、長寿命の状態の連続した線(モジュール数が増えれば平面)を生み出します。
分子機構が記憶を固定する仕組み
最も単純な二モジュールネットワークCTMN‑1では、実験と詳細な動力学モデリングにより、系が「モジュールAが主」から「モジュールBが主」までほぼ全範囲にわたる安定な混合の族に落ち着くことが示されました。重合は能動的な二本鎖を一時的にストランド交換競合から除外される伸長形へと変換し、ニッキングがそれらを復元して自己調節ループを閉じます。両モジュールがこのループを共有すると、相互変換が極めて強く抑制され、燃料が供給される限り系は出発時の組成の近くに何時間もロックされ続けます。基礎方程式の線形安定性解析は、酵素や燃料が除かれた場合に見られる単一の固定点とは対照的に、事実上の連続体である全体の多様体(マニフォールド)として定常状態の集合を明らかにします。
プログラム可能な応答と分子メモリ
ネットワークの状態はDNAの組成として格納されるため、プログラム可能な方法で操作および読み出しが可能です。著者らは短いRNA「トリガー」を設計し、特定のDNA鎖に一時的に結合させて競合を偏らせ、ネットワークを新たな組成へとシフトさせます。RNAが酵素により分解された後でも、新しい状態は持続し、分子メモリの一形態として機能します。繰り返しや強い刺激は、単純なオン/オフの切り替えではなく、状態を連続体に沿って滑らかに駆動します。さらに、DNA複製産物自体を下流プロセスのシグナルとしてカスタマイズでき、実証ではCTMN‑1の異なる状態が基盤となる多安定性を壊すことなく二つのDNA触媒のうち一方を選択的に活性化したり、二種類のメッセンジャーRNAのいずれかへの転写を偏らせたりする様子が示されました。
複雑な分子「調光器」へのスケールアップ
この戦略がスケール可能であることを示すために、研究者たちは共通の交換ドメインを共有しながら異なる複製鋳型を符号化する追加の設計DNA二本鎖を導入して、三モジュールネットワークCTMN‑2を構築しました。すると可能な定常状態は単純な線ではなく、三角形の相図上の点のように二次元領域を埋めます。ここでも、燃料と酵素が存在する限り多くの異なる組成が安定であることが実験により確認され、エネルギー供給が断たれるとすべて単一の平衡点に収束します。新しいモジュールを追加するには同じ置換フレームワークに差し込める新規DNAコンストラクトを用意するだけでよく、従来の設計のように配線の複雑さが爆発的に増すことはありません。
将来の分子技術にとっての意味
非専門家にとっての核心的なメッセージは、著者らがDNA複製ネットワークを非常に柔軟なアナログ記憶装置に変えた、という点です。いくつかの事前設定された選択肢の中から選ぶのではなく、彼らの系は各DNAモジュールの存在量によって定義される、実験的に識別可能な何十もの状態のいずれかを確実に保持でき、短時間の化学パルスをこの連続体に沿った長期的な変化へと変換できます。出力となるDNA鎖はプログラム可能であり、安定化機構から切り離されているため、同じ枠組みが原理的には下流のさまざまな生化学反応や材料特性を微妙に段階的に制御するのに用いられ得ます。本研究は、単純なデジタルスイッチではなく神経的・機械的なアナログ系に近い形で計算し、記憶し、適応する分子デバイスの可能性を示しています。
引用: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
キーワード: DNA多安定性, 分子メモリ, 合成生化学ネットワーク, DNAストランド置換, アナログ分子計算