Clear Sky Science · ja
空間トランスクリプトミクスデータから遺伝子マーカーと細胞型を頑健かつ解釈可能に予測する
日常的な組織スライドを分子マップに変える
生検が行われると、医師は通常顕微鏡が示すもの、つまりピンクと紫の染色で浮かび上がる細胞の形や配列しか見えません。しかしその色の下には、がんの成長や治療反応に影響を与える遺伝子のオン/オフという隠れた世界が存在します。本研究はSTimageという新しい人工知能(AI)システムを紹介し、標準的な病理画像からその分子的な“脚本”を直接読み取ることを目指します。これにより、追加の検査を行わずに、より速く、より安価に知見を得られる可能性があります。
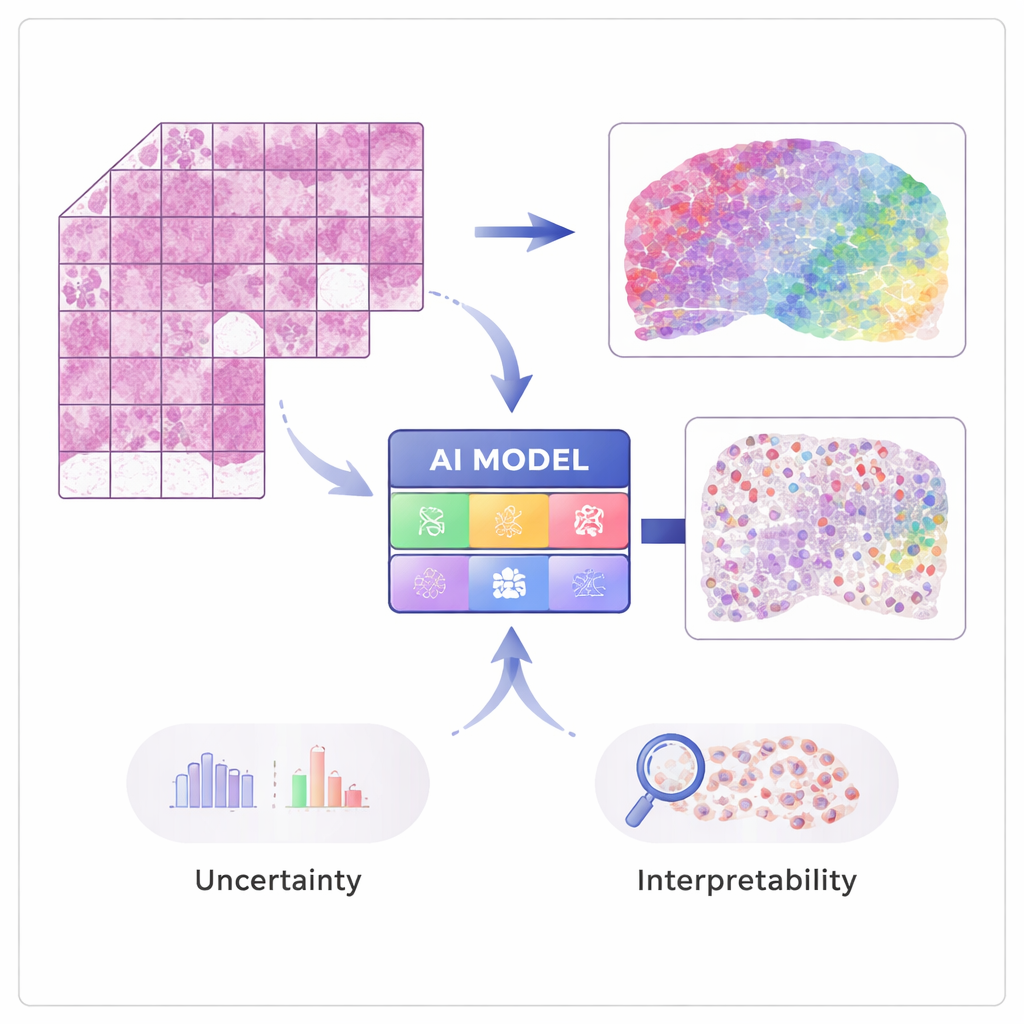
画像から遺伝子活性へ
“空間トランスクリプトミクス”の現代的技術は、各信号の発生位置を保持したまま数万に及ぶ遺伝子の活性を測定できます。これらの手法は強力ですが高価で、まだ病院で広く常用されているわけではありません。STimageはこのような空間データセットの限られた数を用いて学習され、各組織画像が多数の微小スポットでの詳細な遺伝子計測と対応付けられています。AIは、H&E(ヘマトキシリン・エオシン)スライド上の局所的な視覚パターン、たとえば核の密度や不整形さなどと基礎にある遺伝子活性とを関連付けて学習し、その結果、後に通常の画像だけから遺伝子発現や細胞型を予測できるようになります。
より信頼できるAI病理学者を構築する
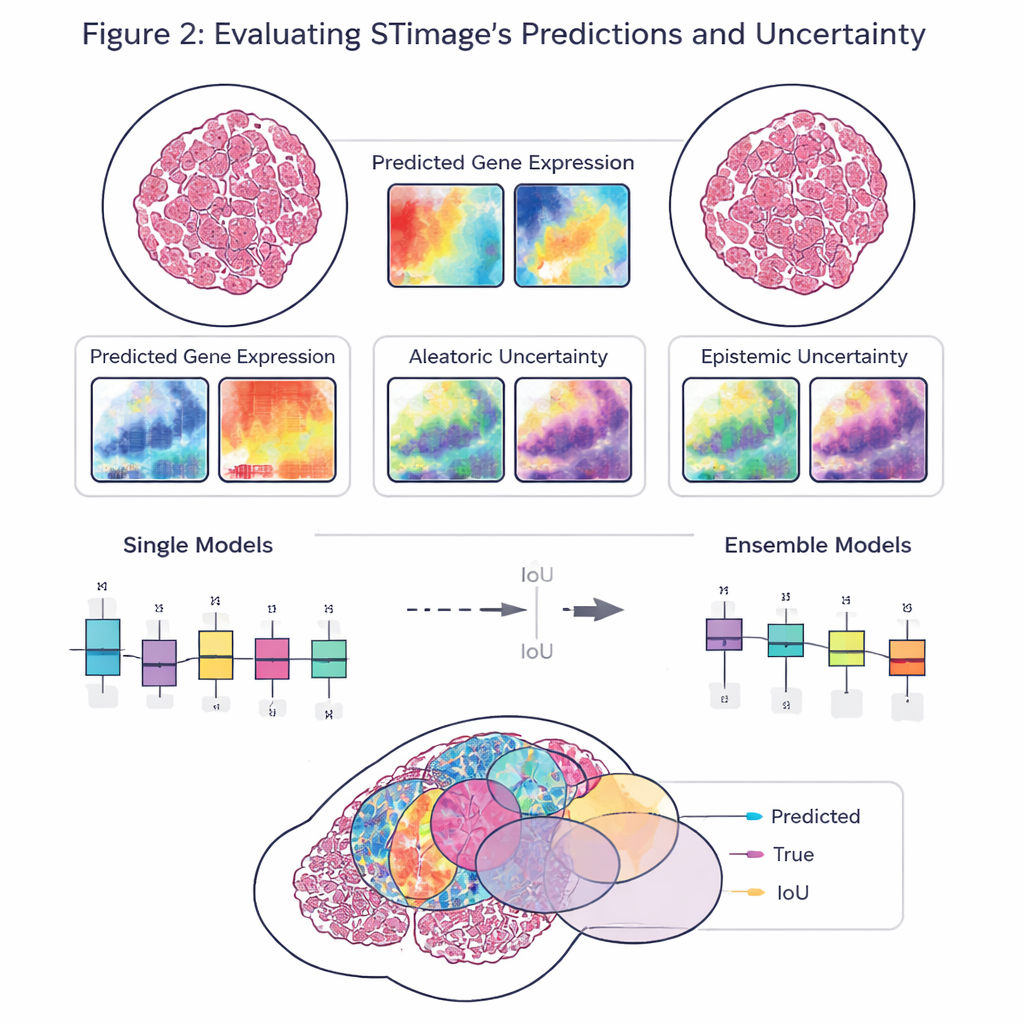
本研究の重要な目的は、単なる精度だけでなく信頼性と解釈可能性です。各遺伝子について単一の数値を出すのではなく、STimageは位置ごとの遺伝子活性のあり得る範囲を記述する確率分布を予測します。また、不確実性を2種類に分けます。ひとつはノイズやデータのばらつきによる不確実性、もうひとつはモデル自身の知識不足を反映する不確実性です。わずかに異なる多数のモデルを訓練してそれらを平均化する「アンサンブル」手法により、研究者たちは性能を向上させると同時に、システムがどこで自信を持っているか、どこで持っていないかをより明確に把握できます。これは臨床判断にとって重要です。
がん種、技術、病院を越えて検証
研究チームは、乳がん、皮膚がん、腎がん、さらに免疫関連の肝疾患を含む多様なデータセットでSTimageを評価しました。重要ながんマーカーや免疫マーカーの予測を学習し、独立した実験で観察された実際の空間パターンにしばしば一致しました。異なる研究室やサンプル調製法、さらには単一細胞解像度プラットフォームや古い低解像度システムなど異なる基盤技術を用いたデータでもモデルは耐えました。既存のいくつかのAIツールとの直接比較では、STimageとそのアンサンブル変種が概して優れており、特に予測されたパターンが組織全体の実際の遺伝子活性分布とどれだけ一致するかを評価する場面で顕著でした。
腫瘍の内部を覗く:細胞、予後、生存と薬剤反応
STimageは遺伝子予測を超えて、各領域にどの細胞型が存在するかを、高解像度データセットで各細胞の同定が分かっている場合に推定します。モデルはがん細胞を免疫細胞や支持細胞と区別し、スライド上での配置をマッピングできました。著者らは次にSTimageをThe Cancer Genome Atlasの大規模な日常的がん画像コレクションに適用しました。空間計測がなくても、AIの予測した遺伝子プロファイルは実際のバルク遺伝子データと密接に一致しました。これらの予測は、患者を高リスク群と低リスク群に分類するのに十分であり、特定の乳がん治療に完全に反応する可能性が高い患者の識別にも役立ちました。
将来の患者にとっての意義
患者や臨床医にとって、STimageの約束は馴染みのある病理スライドに重ねる「分子的オーバーレイ」のようなものです。複数の高価な検査を個別に注文する代わりに、スキャンした単一の画像が、攻撃的な遺伝子プログラムがどこで活性化しているか、免疫細胞がどのように分布しているか、どのマーカーがより良いまたはより悪い予後や薬剤反応を示すかを明らかにする日が来るかもしれません。手法はまだ改良途上であり実測との相関が完全ではないものの、空間パターンを捉え、自らの不確実性を見積もり、どの細胞が予測を駆動しているかを強調できる能力は、より情報量が多く透明性のあるデジタル病理学に向けた現実的な一歩です。
引用: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
キーワード: デジタル病理学, 空間トランスクリプトミクス, がんバイオマーカー, 深層学習, 腫瘍微小環境