Clear Sky Science · ja
ヒトGABAトランスポーターGAT3の選択的阻害に関する構造基盤
脳の鎮静信号が重要である理由
脳は興奮性の信号と鎮静性の信号との微妙なバランスに依存しています。主要な鎮静性伝達物質であるGABAは、てんかん、脳卒中による損傷、アルツハイマー病などに関連する暴走的な神経活動を抑えるのに重要です。本研究は、神経細胞周囲のGABAを除去するタンパク質であるGAT3に着目しています。新規分子がGAT3に結合してそれを阻害する様子を原子レベルで明らかにすることで、研究者たちは脳の自然な制御機構を穏やかに強化する次世代薬の設計に向けた構造的な設計図を示しています。
脳のブレーキペダル
GABAは中枢神経系における主要な抑制性、すなわち鎮静性の神経伝達物質です。GABAが神経末端から放出された後、脳回路がリセットされるために迅速に除去される必要があります。その掃除はGABAを細胞へ再取り込みするトランスポータータンパク質によって行われます。脳内で優勢な二つのトランスポーターは、主にニューロンに存在するGAT1と、アストロサイトと呼ばれる支持細胞に存在するGAT3です。GAT1を阻害する薬(チアガビン)は何十年もてんかん治療に用いられてきましたが、GAT3を標的とする同等の薬剤は遅れてきました。それでもGAT3は、シナプス外のGABA濃度を制御し、長時間持続する背景的な抑制を形作って脳活動を微調整するため、特に興味深い存在です。 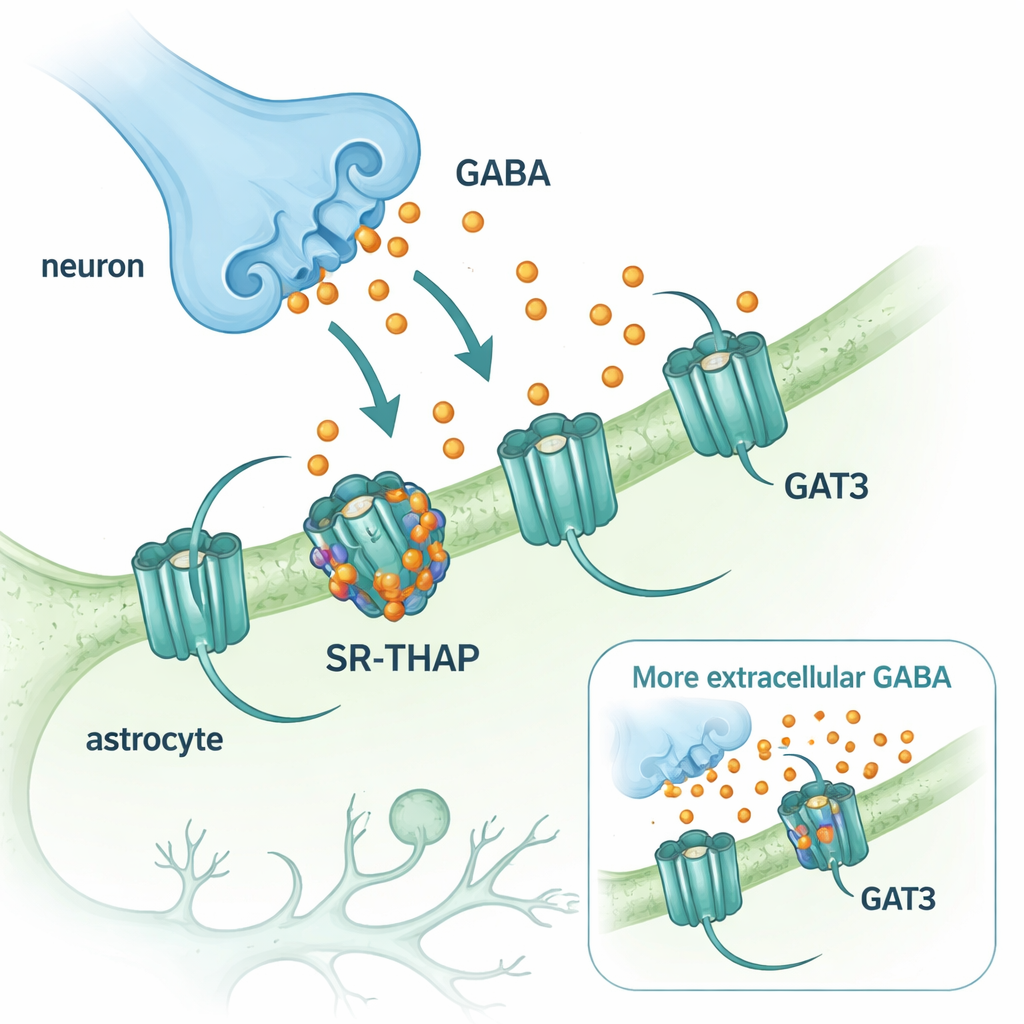
より精密な分子ロックの設計
GAT3を阻害する試みは詳細な構造情報の不足によって妨げられてきました。過去の多くの化合物は試行錯誤で作られ、しばしば既知のGABA類似分子をかさ増しした変化体が用いられました。よく知られた一つ、(S)-SNAP-5114は化学的に不安定で生体内で扱いにくいことが分かりました。本研究の著者らは、この化合物のより安定な近縁体を足がかりに、GAT3によりぴったり合い分解に強い新たな低分子SR-THAPを開発しました。ヒト細胞培養での実験は、SR-THAPがGAT3を強力に阻害し、その阻害様式が非競合的であることを示しました。すなわち、通常の結合部位でGABAと単に競合するのではなく、トランスポーターの働き方を変えて最大輸送能を低下させます。
GAT3を準原子分解能で観察する
SR-THAPの作用を正確に理解するため、研究チームはクライオ電子顕微鏡(クライオEM)に取り組みました。これはタンパク質を急速凍結して電子で撮像し、その三次元形状を再構築する手法です。彼らはSR-THAP結合型、GABA結合型、基質非結合型のヒトGAT3の三つの状態を解決しました。いずれの構造も関連する神経伝達物質トランスポーターに見られる典型的な構造を示しており、膜を横切る12本の密に詰まったヘリックスが中央の通路を形成し、GABAとともに運ばれるナトリウムや塩化物イオンの通り道を作っています。GABA結合構造では、トランスポーターは「内向き閉塞(inward-occluded)」状態にあり—GABAとナトリウムイオンが中央で固定され、外側と内側の双方から遮断されています。鍵となる芳香族アミノ酸はGABAのアミノ基と特殊な相互作用を形成し、GAT3が基質を認識する仕組みを説明する助けとなります。
SR-THAPがトランスポーターをどのように開かせるか
これに対して、SR-THAP結合構造は目を引くことにGAT3を「内向き開放(inward-open)」状態でとらえており、タンパク質の内側面が細胞内部に向かって大きく開いています。SR-THAPはこの内腔の深部に収まり、輸送サイクル中に通常動くいくつかのヘリックスの間に楔(くさび)のように入り込んでいます。SR-THAPは性質の異なる三つの小さなポケットを占有し、水素結合および疎な接触のネットワークに関与します。この位置取りによりトランスポーターは実質的に動きを止められ、GABAやイオンはもはや輸送を完了できなくなります。著者らは、この内腔に沿ういくつかの特定のアミノ酸がGAT3とその近縁体で異なることを示しており、これらの残基を入れ替えると輸送活性とSR-THAPの効力が変わることを確かめています。これが阻害薬がGAT1や関連トランスポーターよりもはるかにGAT3に選択的である理由の説明に繋がります。 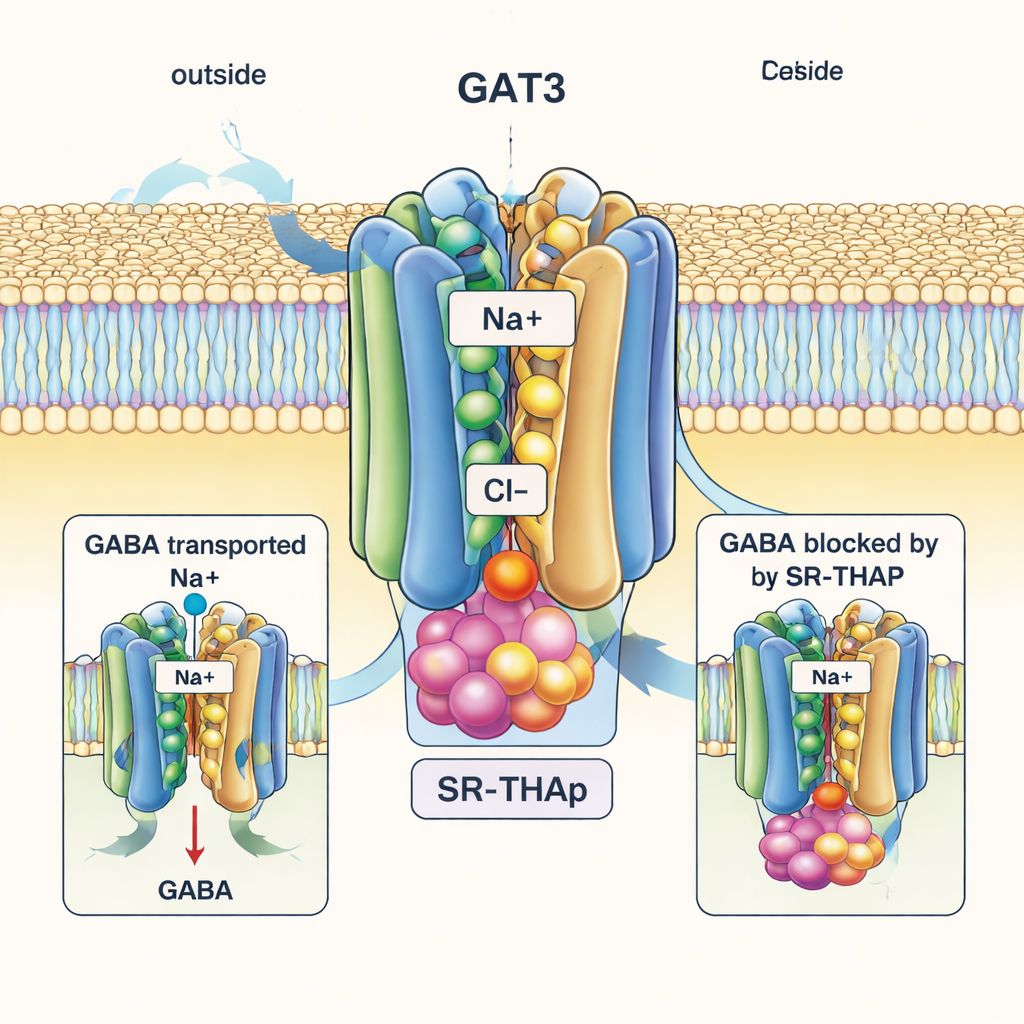
新たなてんかん・脳健康薬への道を開く
これらの構造により、GAT3がGABAを移動させるためにどのように形を変えるか、そしてSR-THAPがどのようにして保存度の低い内側ポケットを利用してそのサイクルを凍結させるかが明らかになりました。専門外の読者への主要な結論は、本研究がGAT3を高度に選択的にオフにするための詳細な分子設計図を提示したことです。この種の化合物は既存薬よりも微細にGABAの鎮静効果を高める可能性があり、てんかん、脳卒中からの回復、アルツハイマー病など、抑制性シグナルが乱れている疾患に対する新しい治療法や研究ツールに繋がる可能性があります。
引用: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
キーワード: GABAトランスポーター, GAT3, てんかん, クライオ電子顕微鏡, 神経伝達物質の抑制