Clear Sky Science · ja
ヒト小伝導性Ca2+活性化カリウムチャネルSK2の阻害と活性化に関する構造的機構
なぜ小さなカリウムチャネルが重要なのか
あなたの思考や心拍の一つひとつは、細胞内の電気信号に依存しています。これらの信号は、荷電原子が出入りする微視的な孔であるイオンチャネルによって形作られます。その一群である小伝導性カルシウム活性化カリウムチャネル(SKチャネル)は、神経細胞の発火や心臓のリズム制御に寄与します。本論文は、これらのうち重要な一員であるヒトSK2チャネルが、さまざまな薬剤や蜂毒によってどのように抑制または促進されるかを原子レベルで明らかにしており、心房細動や振戦、記憶障害などの治療開発に役立つ示唆を与えます。
SK2チャネルが細胞のブレーキとして働く仕組み
SK2チャネルは細胞膜に埋め込まれて電気活動に対する小さなブレーキとして機能します。電気的な信号の間に細胞内が一時的にカルシウムイオンで満たされると、カルモジュリンという補助タンパク質がその上昇を感知します。カルモジュリンはSK2の内側に結合しており、カルシウムを結合すると紐を引くようにチャネルの一部を引っ張って、カリウムイオンが外へ流れるゲートを開きます。この外向きの電流は発火後に細胞を鎮め、ニューロンの信号発射頻度や心筋細胞のリズムの安定性を形作ります。SK1–3は脳や心臓に広く存在し、SK2は特に重要なサブタイプであるため、これらがどのように開閉し薬剤に応答するかを正確に理解することは、的確な薬剤設計に不可欠です。
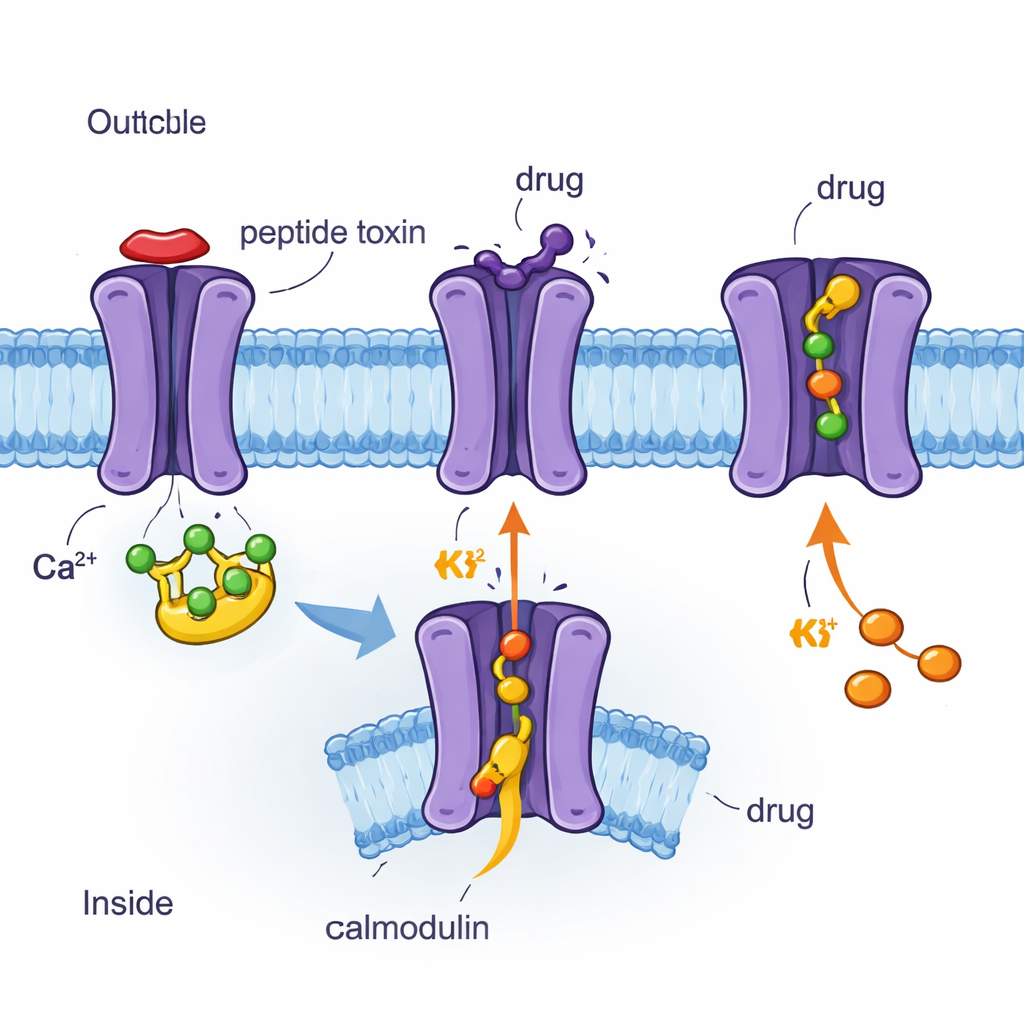
クライオ‑EMでチャネルと薬を原子単位で見る
著者らはクライオ電子顕微鏡(cryo‑EM)を用い、フラッシュ凍結したタンパク質を準原子分解能で撮像して、カルモジュリンと各種分子が結合したヒトSK2チャネルの3次元構造を4種類決定しました。対象は、蜂毒ペプチドのアパミン、合成阻害剤UCL1684、臨床候補の阻害剤AP30663、および臨床用活性化剤CAD‑1883です。いずれの構造でもSK2は膜を貫く四量体として描かれ、カルモジュリンが内側に結合しています。これらのスナップショットを比較することで、チャネルのどの部分が剛直でどの部分が柔軟か、閉状態と開状態でカルモジュリンがどのように動くかが明らかになりました。研究者らはこれらの構造解析を細胞での電気生理学的測定と組み合わせ、特定のアミノ酸変化が各化合物に対する反応にどう影響するかを検証しました。
外側の入口を塞ぐ蜂毒と合成薬
アパミンは蜂毒由来の小さなペプチドで、研究で広く使われる非常に強力かつ選択的なSK2阻害剤として知られてきました。新しい構造は、アパミンがSK2の孔の外側の口を栓のように塞ぐことを示しています。アパミンは、S3–S4リンカーと呼ばれる二つのヘリックス間の短いループが作る杯状の前庭に収まり、このループはSK2では秩序立っている一方で関連するチャネルSK4では不安定であるため、SK4がアパミンに対して感受性を示さない理由が説明されます。アパミン上の正に帯電した重要残基はチャネルの四つの芳香族側鎖の間に届き、強い静電的およびスタッキング相互作用を作ってカリウム経路を完全に封鎖します。合成のビスキノリニウム化合物UCL1684も本質的に同じ外側ポケットを占めてイオンの出口を遮りますが、より小さいため深く入り込み、アパミンの重要な正電荷の位置を模倣します。前庭を形作るチャネル側の残基を変異させるとアパミンへの感受性が大きく低下し、UCL1684への影響はやや小さく、こうした彫られた外側ループが毒素や薬剤の作用を決める主要因であることが裏付けられました。
活動を調整する中央の栓と内側のくさび
これに対して、臨床候補のAP30663は選択性フィルターのすぐ下にあるSK2の中央キャビティ内に結合し、物理的な栓として振る舞います。そこでは孔の内壁を形作る特定の側鎖の間にくさび状に挟まります。これらの内壁残基を変えるとAP30663による阻害能は低下し、配列の比較からはAP30663の近縁体がSK1–3とSK4を識別できる理由が説明されます。一方、運動障害向けに開発された正の調節剤CAD‑1883は別の戦略を取ります。CAD‑1883はカルモジュリンのNローブと、カルモジュリンの動きをゲートに伝える短いリンカー(S4–S5)との界面にあるポケットに滑り込みます。このポケットでの接触を強化することで、CAD‑1883はカルモジュリンとSK2を特定の構成に効果的に“接着”し、内側のゲートを引き開いて孔を拡げます。構造比較は、CAD‑1883結合状態が完全に開いたチャネルに類似していることを示しますが、選択性フィルターは長時間開いた後に不活性化様の形をとる可能性も示唆されます。
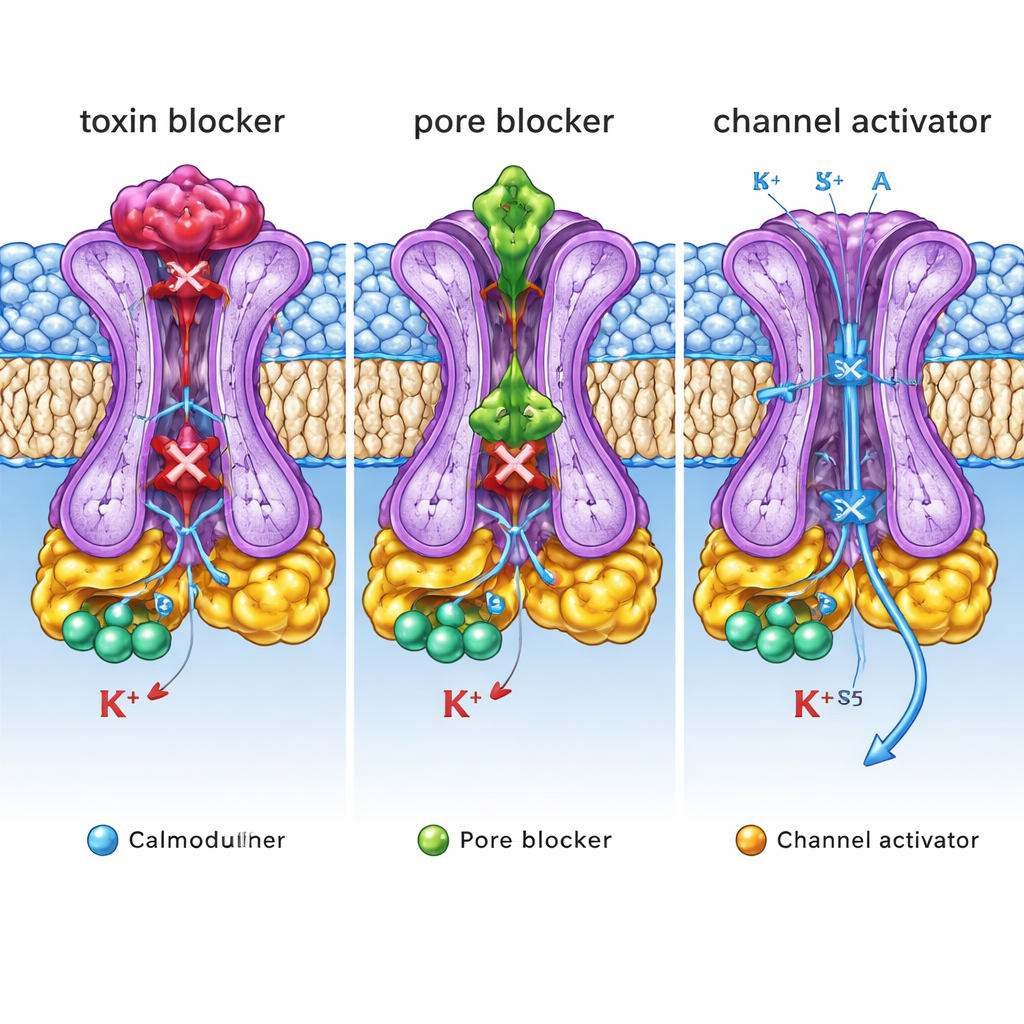
医薬への示唆となる構造設計図
総じて、これらの構造は単一のSK2チャネル上に三つの異なる「調整ノブ」が存在することを明らかにします:毒素や一部の阻害剤が座る外側の蓋、他の阻害剤が流れを塞ぐ内側の孔キャビティ、そして活性化剤が開放を安定化する側面ポケットです。専門外の読者への要点は、同じイオンチャネルが非常に異なる構造的把手を薬剤が掴むことで上げたり下げたりできるということです。これらの把手を原子精度で写像し、それを機能効果に結びつけることによって、本研究はSK2活性を選択的に抑制または促進する次世代分子設計の詳細な設計図を提供します。このようなオーダーメイド薬は、将来的に異常な脳リズムの正常化、振戦の緩和、あるいは心拍異常の是正を、副作用を抑えつつ実現する可能性があります。
引用: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
キーワード: SK2 カリウムチャネル, カルシウム活性化チャネル, クライオ電子顕微鏡構造, イオンチャネル調節薬, 心房細動と振戦