Clear Sky Science · ja
コイルドコイルヘテロダイマー媒介の分割ベース編集システムは柔軟で強力な塩基置換を可能にする
副作用を減らしてDNAを修復する
多くの病気は私たちのDNAにある小さな誤り—一文字のミス—が原因で発生し、生命を脅かすことがあります。ベース編集という強力な道具は、DNAを切断せずにこうした誤りを訂正できますが、装置が大きく体内へ安全に届けるのが難しいという問題があります。本論文は、ベース編集因子を小さくて賢い断片に分割しつつ、元の装置と同等あるいはそれ以上の性能を維持する新しい方法を紹介しており、肝臓や筋肉などでの遺伝病治療に向けた新たな道を開きます。
なぜサイズが遺伝子修復ツールの問題になるのか
ベース編集はCRISPRの一部と、AをGに、あるいはCをTに置換するような酵素を組み合わせたものです。これらの精密な置換は、高コレステロールや筋ジストロフィーのような疾患治療に有望です。しかし、遺伝子治療で主要な送達手段の一つであるアデノ随伴ウイルス(AAV)は約4.7千塩基しか運べない一方で、標準的なベース編集装置はそれより大きいサイズです。これまでの研究では、インテインと呼ばれるタンパク質の“はさみ”で分割したり、酵素を小型化したりする試みがありましたが、効率が落ちたり設計が複雑になったり、作用できるゲノム領域が制限されたりすることがありました。
分子用ベルクロでエディターを組み立て直す
この問題を解決するために、研究者たちはコイルドコイルヘテロダイマーとして知られる小さなタンパク質ジッパーを用いて“分割”ベースエディターを結合させる設計を行いました—まるで分子レベルのベルクロのように。編集因子を二つに分け、一方はDNAを標的とするCas9ニッカーゼを、もう一方は編集酵素を担います。各断片には短いコイルドコイルペプチドが付けられており、両方の断片が同じDNA配列に到達すると互いを見つけて結合します。これによりコイルドコイルベースエディター(CC‑BE)が生まれ、Cを編集するCC‑CBE、Aを編集するCC‑ABE、さらにさまざまな塩基変換を行える複合型も含まれます。 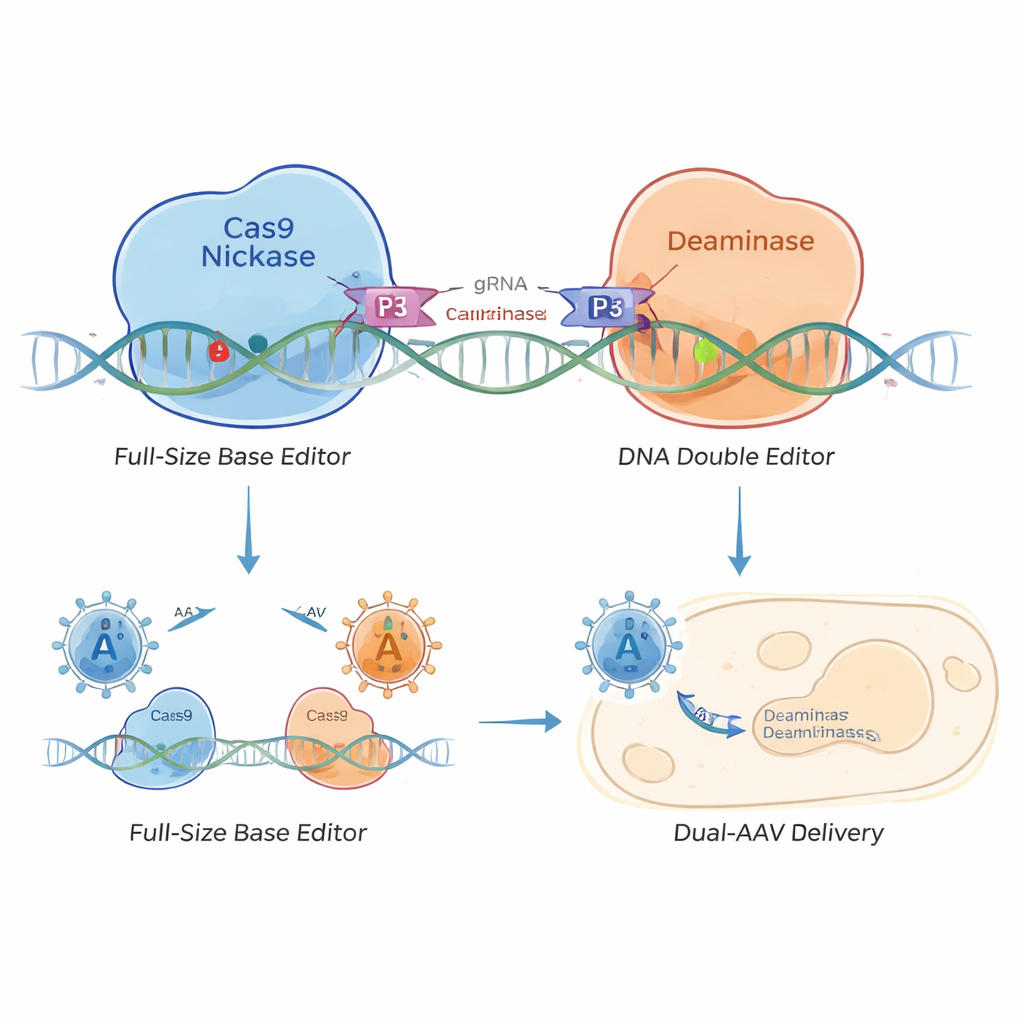
柔軟で強力、かつ正確な編集
研究チームはヒト細胞やブタの一次細胞など複数の細胞種、およびより広いDNA配列を認識するCas9の変異体を用いてCC‑BEを検証しました。CC‑CBEは多くの部位で安定した動作を示すだけでなく、より広い“編集ウィンドウ”を持ち、ターゲットとなる塩基を広い範囲で変更できるため、ガイドRNAの選択に柔軟性を与えました。CC‑ABEは既存の最良のアデニンエディターに匹敵する効率を達成し、しばしば副生成物を減らしました。また研究者たちはこのコイルドコイル戦略を、より小型のTadCBEや高精度のABE9といった新しいエディター設計にも応用し、分割しても性能が維持または向上することを確認しました。
シャーレから生体マウスへ
重要なことに、著者らは二重AAV送達を用いて生体内でもこれらの分割エディターが機能することを示しました。各ウイルス粒子がエディターの半分を運ぶ方式です。マウスでは、肝臓のPcsk9遺伝子を標的としたCC‑ABEがA→G置換を約70%まで達成し、Pcsk9タンパク質と血中LDLコレステロールを大きく低下させつつ、肝障害の兆候は見られませんでした。 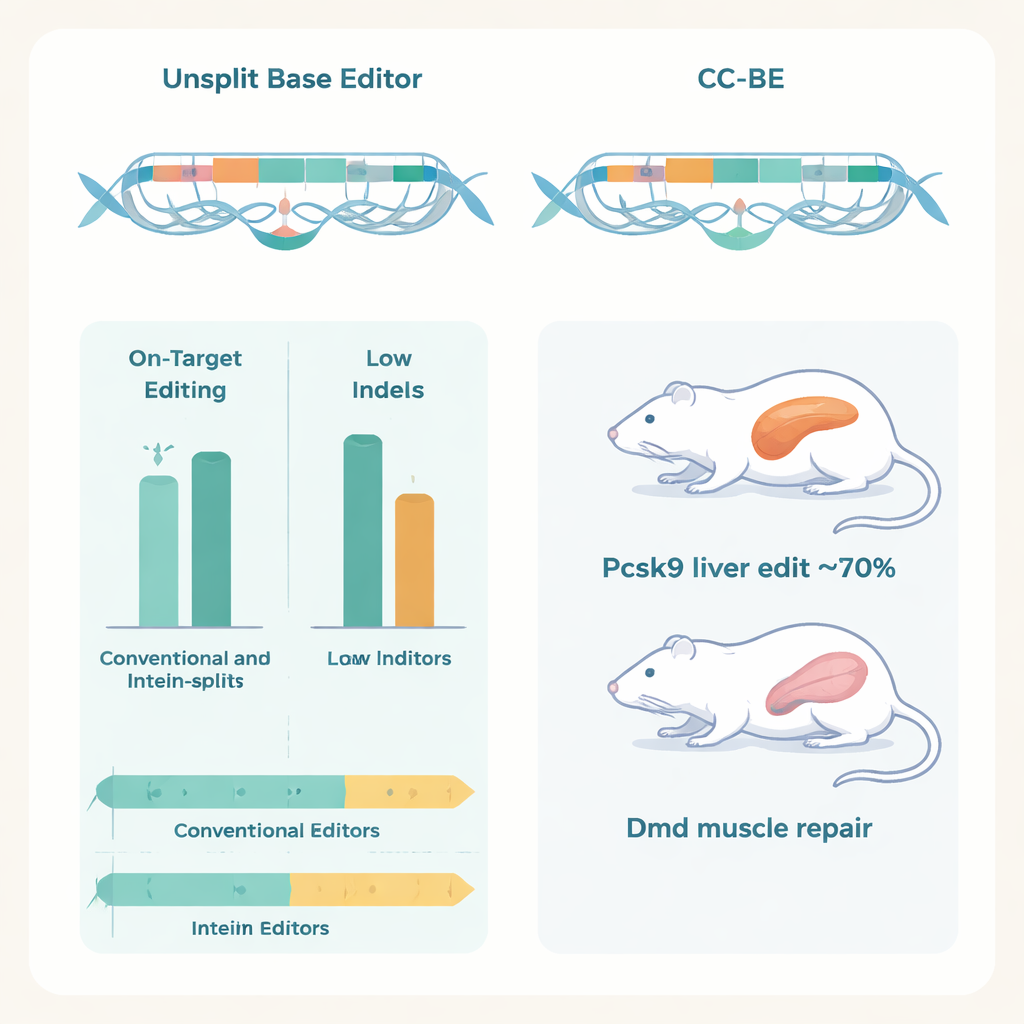
実用的なDNA修復への新たな道
本研究の本質はシンプルだが強力な工学的発想にあります:小さなコイルドコイルの“フック”を使って大きなベースエディターをAAVサイズのモジュールに分割し、必要な場所でのみ再結合させることです。専門外の人向けに要約すると、研究者はもはや高性能なDNA修復ツールを正確さや効果を犠牲にせずに臨床で実績のあるウイルスキャリアに梱包できるようになった、ということです。このコイルドコイル方式は、肝臓、心臓、筋肉などの臓器における単一塩基の遺伝病に対する治療設計を容易にし、精緻な遺伝子修正を現実の治療へと一歩近づける可能性があります。
引用: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
キーワード: ベース編集, 遺伝子治療, CRISPR, AAV送達, 遺伝性疾患