Clear Sky Science · ja
生体内CRISPRスクリーニングが造血の主要調節因子としてSAGA複合体成分を同定
血液産生のバランスを保つことが重要な理由
毎日、体内では静かに数千億もの新しい血球が作られ、酸素を運び、感染と戦い、出血を止めています。この休むことのない産生は、骨髄に存在する希少な「母」細胞、すなわち造血幹細胞に依存しています。これらの細胞を制御する仕組みが乱れると、貧血や免疫低下、白血病のようながんが生じることがあります。本研究は単純だが力のある問いを投げかけます:私たちのゲノムにある何千もの遺伝子のうち、血液の産生を健全かつバランスよく保つために真に不可欠なものはどれか?
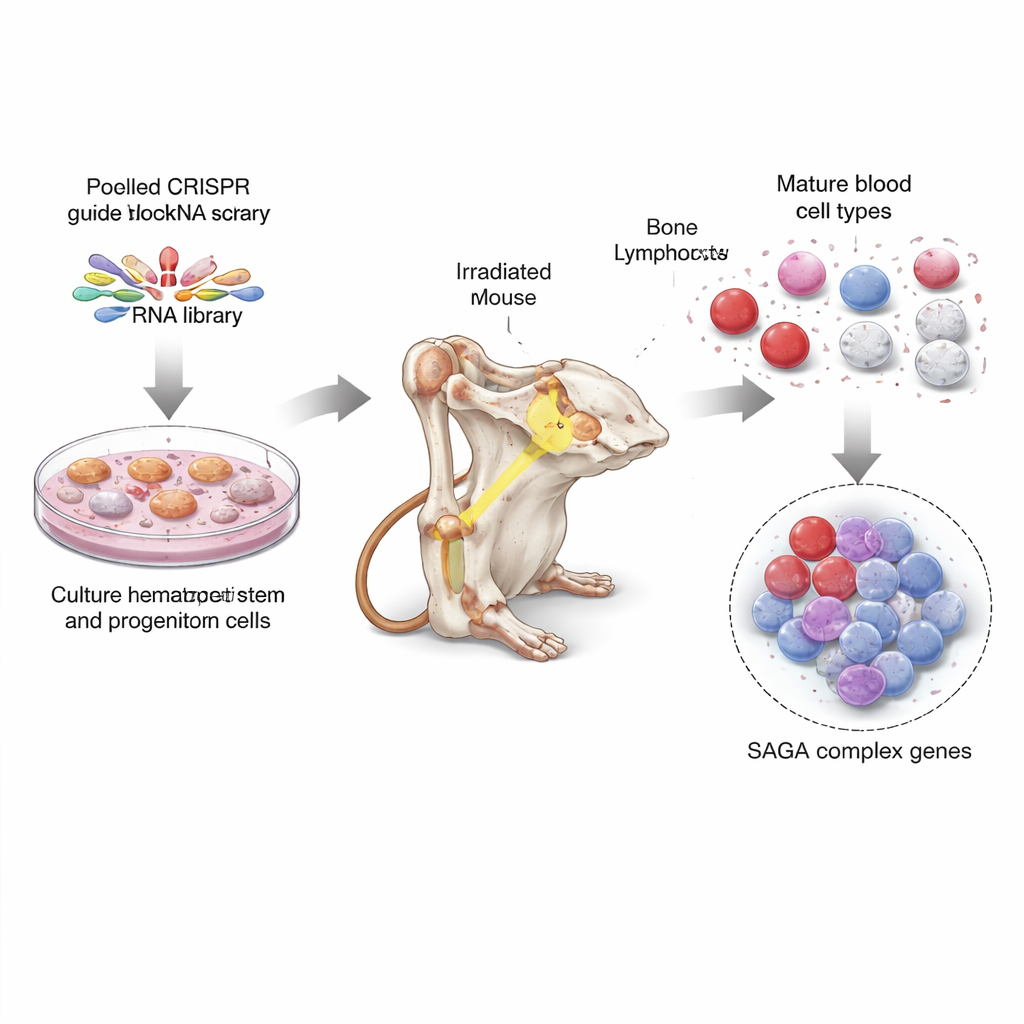
マウス幹細胞での全ゲノムトレジャーハント
この問題に取り組むため、研究者たちはCRISPR—分子はさみになぞらえられる遺伝子編集ツール—を用いてマウスのゲノム上のほぼ全ての遺伝子を、遺伝子ごとに10本のガイドで無効化しました。まず骨髄の幹および前駆細胞を大量に特別な培養条件下で増やし、これらの細胞にプール化したCRISPRガイドを感染させて各細胞が異なる遺伝子のノックアウトを持つようにしました。次にこの混合編集細胞を多数の照射処理したマウスに移植し、編集された細胞が動物の血液系を再構築するのを待ちました。数か月後、骨髄からさまざまな成熟血球型や幹様細胞を精製し、どのCRISPRガイドが過剰または欠損しているかを読み出しました。これにより、どの遺伝子の喪失が未熟な細胞の蓄積を促し、どの遺伝子が完全に形成された血球の産生を支えているかが明らかになりました。
SAGAと呼ばれる隠れた制御ハブが浮かび上がる
既知の造血調節因子の中に、驚くべきヒット群が現れました:SAGA複合体と呼ばれる大型タンパク質集合体のいくつかの構成要素、具体的にはTada2b、Taf5l、Tada1と名付けられた遺伝子です。SAGAは直接血球を作るわけではなく、ヒストンと呼ばれるDNA包装タンパク質に化学的な印を付けることで他の遺伝子のオン・オフを助けます。研究チームがこれらのSAGA構成要素を個別にノックアウトして編集細胞をマウスに移植すると、一貫したパターンが観察されました。未熟な骨髄細胞が蓄積する一方で、循環する白血球や赤血球、特定の免疫細胞へと成熟する能力は著しく低下しました。本質的に、幹および前駆細胞はボトルネックに詰まり、完全に機能する血球へ到達できなくなっていました。
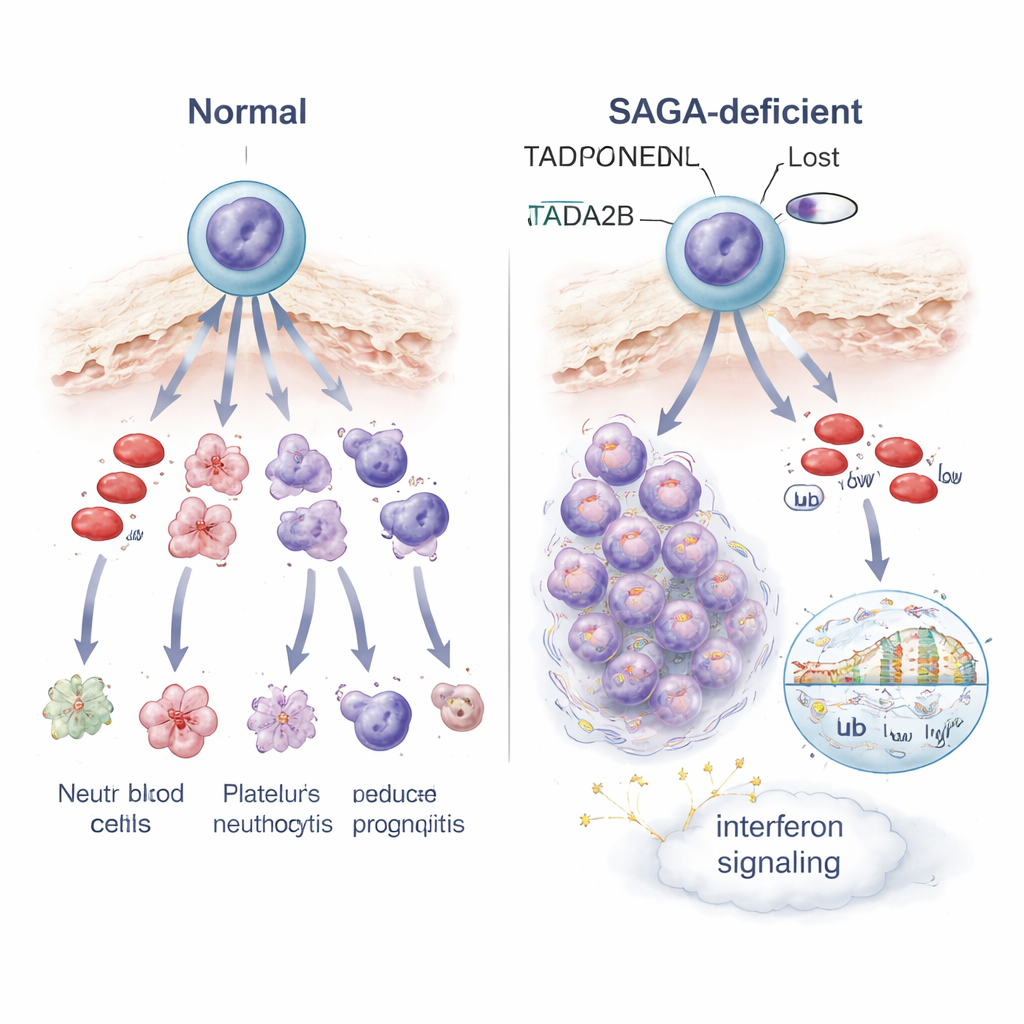
制御の乱れが細胞運命とストレス信号をどう変えるか
この詰まった細胞内で何が起きているかを理解するために、研究者たちは単一細胞レベルとバルクで遺伝子発現をプロファイリングしました。Tada2bやTaf5lの喪失は幹細胞内の多くの遺伝子の活動を書き換え、二つの顕著なテーマが浮かび上がりました。第一に、通常は抗ウイルス防御の一部であるインターフェロンシグナルに関与する遺伝子群が活性化し、内部アラームあるいはストレス状態を示していました。第二に、細胞の仕事を支える小さな発電所であるミトコンドリアの機能が低下し、これらの変化した細胞はミトコンドリアのエネルギー生産を標的とする薬剤に対してより感受性が高くなりました。DNA包装のレベルでは、Tada2b欠損細胞で開いた活性クロマチンに関連するヒストン修飾が減少し、遺伝子の読み出しに関わる別の修飾にも変化が見られました。これらのクロマチン化学の変化は、正しい血液成熟を導く遺伝子群を含め多くの遺伝子が誤制御される理由を部分的に説明するものと考えられます。
基礎メカニズムから疾患モデルへ
研究チームは次に、SAGA活性を上げ下げすることでこれらの影響を逆転できるかを検証しました。細胞に余分なTada2bを作らせるとインターフェロン関連遺伝子の活動は低下し、幹様細胞の割合も減少しました—ノックアウトの鏡像のような結果です。正常な幹細胞にSAGAの主要な酵素サブユニットを阻害する薬剤を投与すると、Tada2b喪失のシグネチャの多くが再現され、SAGAのクロマチン修飾活性がその役割の中心であるという考えが強まりました。最後に、研究者たちは血液産生が障害され、インターフェロン経路がしばしば上昇する前白血病性障害である骨髄異形成症候群のヒト細胞モデルに着目しました。これらのヒト細胞でSAGA成分をノックアウトして免疫不全マウスに移植すると、編集された細胞は増殖上の優位性を獲得し、再びインターフェロンや骨髄系遺伝子プログラムが活性化しました。これはこの制御ハブが疾患の挙動にも影響を与えることを示唆しています。
血液の健やかさと将来の治療への意義
一般読者にとっての核心的メッセージは、本研究が造血幹細胞において「いつ未熟なままでいるか、いつ成熟するか、そして有害なストレス応答を回避するか」を決める強力な制御センター—SAGA複合体—を明らかにしたことです。主要なSAGA成分が欠けると、幹細胞は蓄積するが十分な働く血球を作れなくなり、ストレスや抗ウイルス様のシグナルが高まり、ミトコンドリア機能が低下します。これらの発見は、健康な血液産生が一生にわたってどう維持されるかの理解を深めるだけでなく、SAGA活性の微妙な変化が加齢に伴う血液の問題や骨髄異形成症候群のような疾患に寄与している可能性を示唆します。長期的には、この制御回路の地図化が、欠陥のある幹細胞をバランスの取れた回復力ある血液産生へと導く治療の設計に役立つかもしれません。
引用: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
キーワード: 造血幹細胞, CRISPRスクリーニング, SAGA複合体, インターフェロンシグナル, 骨髄異形成症候群